近期,華南理工大學王小英教授團隊和暨南大學查振剛教授、張還添副教授團隊在科愛創辦的期刊Bioactive Materials上聯合發表論文:通過模擬膠原形成納米粒子,并通過粒子間光交聯制備了一種可注射、軟而韌、且抗溶脹的納米纖維水凝膠用于促進傷口愈合。通過小鼠創面愈合實驗發現,與對照組(65.2%)相比,該凝膠治療組在第7天便可實現90.8%的愈合率,并且在第11天實現完全愈合。
1、研究內容簡介
軟的水凝膠因其與軟組織相似的低模量(<10 kPa),有利于干細胞分化為軟組織的細胞系,常用于軟組織修復。傳統水凝膠主要是合成聚合物,盡管它們的硬度低、強度適當,但是其生物降解性差、過度溶脹和潛在的毒性大大限制了它們的臨床應用。最近,天然聚合物,如多糖等,已被用于制造生物相容性好、可降解的軟水凝膠。然而,仍需解決不可控溶脹和機械強度較差的問題。此外,作為植入材料,可注射水凝膠比預制水凝膠具有更多優勢。因而,具有可注射、軟而韌和抗溶脹等功能的天然聚合物水凝膠是軟組織修復的理想材料,但目前很少有研究致力于開發此類水凝膠。基于此,本課題組通過模仿膠原原纖的納米結構和兩親性,提出了一種結合自組裝和化學交聯的策略,用于制備可注射、生物相容、可生物降解、低硬度、高抗壓強度和抗溶脹的水凝膠,而無需合成聚合物。同時證實了其在3D打印和促進傷口愈合中的巨大潛力。
圖1. HML納米復合水凝膠的制備及應用示意圖
HML納米復合材料的制備及其相互作用機制
該研究使用甲基丙烯酰化羥丙基殼聚糖(HM)與鋰皂石(LAP)進行物理混合,獲得HML納米復合材料。研究發現,隨著LAP加入量的增加,所得納米復合材料的尺寸逐漸變小。
圖2. HML納米復合材料的表征
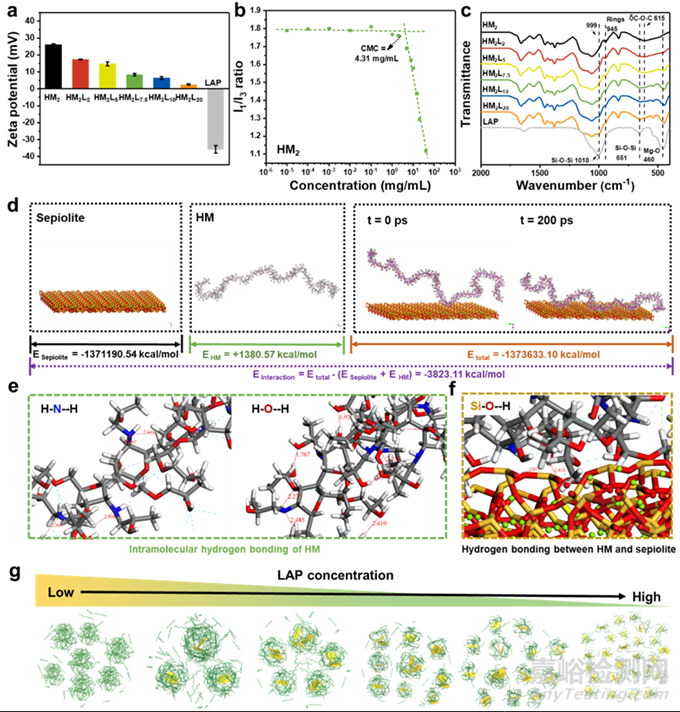
通過實驗以及分子動力學模擬的結果,我們推測LAP通過靜電和氫鍵作用與HM發生自組裝并被包覆,同時在LAP上吸附的HM通過氫鍵自組裝形成緊密的HM聚合物層,進而形成表面帶光交聯基團的納米粒子。在一定濃度的HM溶液中,低濃度的LAP可被足夠的HM高度覆蓋LAP表面,并完全屏蔽LAP的自然電荷,從而產生大尺寸的納米顆粒。而隨著LAP的含量增多,每個LAP中可吸附的HM鏈數量因相互競爭而減少,導致納米顆粒變小。
圖3. HML納米復合材料的相互作用機制
HML納米復合水凝膠的結構及性能表征
HML納米復合材料可以填充復雜的形狀并在紫外光照射下原位形成水凝膠。通過冷凍掃描電鏡可以發現,HM基水凝膠均顯示出三維多孔的納米結構。當鋰皂石的含量為5 g/mL時,水凝膠內部網絡的納米纖維直徑增加到50 nm,并且形成的結構明暗相間,與膠原原纖的納米結構相似。這表明,紫外光照射后,納米顆粒的雙鍵發生交聯形成納米纖維交織的三維交聯網絡。
圖4. HML水凝膠的微觀結構特征及溶脹行為
可原位形成的水凝膠可用于填充缺陷,因此抗溶脹性能非常重要,其可防止水凝膠過度溶脹導致凝膠破裂。通過測試發現,HML復合水凝膠在生理環境下均具有良好的抗溶脹性能。
圖5. HML水凝膠的機械性能
通過對不同交聯時間、HM取代度以及LAP加入量制備的水凝膠進行機械性能測試發現,隨著LAP含量和化學交聯的增加,納米復合水凝膠的抗壓強度呈現出先上升后下降的趨勢。其中,HM2L5水凝膠表現出快速制備(2 min)、大應變(76%)、低模量(1.83 kPa)和最高壓縮強度(709.9 kPa)的優異性能。與現有可注射的天然聚合物軟水凝膠相比具有明顯優勢。
納米復合微凝膠的3D打印性能
為了使水凝膠獲得可打印以及先進制造的能力,本研究利用預交聯及機械擠壓的方式制備了HML納米復合微凝膠墨水,使其實現了保真度較高的3D打印,拓寬了該凝膠在3D打印及個性化定制組織工程中的應用。
圖6. 復合海綿的體內外止血性能
納米復合水凝膠的體外生物相容性和生物效率
由于原位形成的水凝膠作為凝膠前驅體接觸細胞/缺陷部位,因此對凝膠前驅體和形成凝膠的生物相容性均進行了評價。結果表明,光交聯前后的納米復合材料具有良好的生物相容性,在組織工程應用中是安全的。同時我們發現,LAP加入后可顯著促進L929細胞的遷移以及內皮細胞的成管效率。
圖7. 納米復合水凝膠的體外生物學評價
復合海綿的降解及促傷口愈合能力
水凝膠在體外和體內的降解特性對于生物材料和組織工程至關重要。我們發現所有水凝膠體內外均具有良好的降解能力,在皮下植入7天后即可完全降解。
為了評估復合納米水凝膠的促傷口愈合性能,在小鼠背部建立了創傷模型。與對照組和HM2水凝膠相比,使用HM2L5微凝膠和HM2L5水凝膠治療的傷口在第3天愈合已展現出更快的愈合速度。通過對第7天和第11天的組織進行H&E、Masson和免疫熒光染色發現,HM2L5微凝膠和HM2L5水凝膠組在第7天的新生肉芽組織更多,在第11天時創面完全愈合,同時顯示出更高的膠原密度和更多的成熟血管。這些結果表明,HM2L5水凝膠可加快細胞遷移和新生血管形成,從而促進傷口愈合。此外,微凝膠處理不會損害HM2L5水凝膠原有的促創面愈合能力,進一步證明HM2L5微凝膠在個性化定制傷口敷料方面的巨大潛力。
圖8. 納米復合水凝膠的體內降解及創面愈合能力
結論
本研究通過利用自組裝和化學交聯結合的策略,開發出了一種具有低硬度、高抗壓強度、抗溶脹、可載藥和生物降解的膠原纖維狀可注射水凝膠。為了制造這種新型水凝膠,HM和LAP首先通過靜電和氫鍵作用自組裝成納米顆粒,然后通過光交聯進一步相互交聯,形成膠原纖維狀網絡。這種網絡由HM分子鏈的熵彈簧行為、聚合物-粘土的可逆物理交聯和強韌的化學交聯組成,使得應力有效耗散,從而形成一種柔韌的水凝膠。由于自組裝引起的分子鏈運動受限和HM兩親性的協同作用,納米復合水凝膠在不同的溶劑中表現出顯著的抗溶脹行為。此外,納米復合水凝膠可加工成三維打印的微凝膠,且形狀保真度高,因此有望成為大尺寸和復雜構造的生物材料。同時,HM2L5水凝膠和微凝膠在體外表現出很高的生物相容性,在體內也具有出色的傷口愈合能力和生物降解性。這些結果共同證明了這種新型仿生水凝膠在傷口敷料等各種軟組織工程應用中的巨大潛力,并為仿生納米纖維軟水凝膠的開發提供了一個通用的策略。
2、原文信息
Shanshan Li, Xiaoyun Li, Yidi Xu, Chaoran Fan, Zhong Alan Li, Lu Zheng, Bichong Luo, Zhi-Peng Li, Baofeng Lin, Zhen-Gang Zha, Huan-Tian Zhang*, Xiaoying Wang*.
CollagenFibril-like Injectable Hydrogels from Self-assembled Nanoparticles for Promoting Wound Healing.
Bioactive Materials, 32(2024) 990-1003.
https://doi.org/10.1016/j.bioactmat.2023.09.012