您當(dāng)前的位置:檢測資訊 > 科研開發(fā)
嘉峪檢測網(wǎng) 2025-06-19 16:52
本文討論了一種特殊藥物,窄治療窗藥物的生物等效性要求。
一、窄治療指數(shù)藥物定義
根據(jù)2020年12月31發(fā)布的《窄治療指數(shù)藥物生物等效性研究技術(shù)指導(dǎo)原則》的定義。窄治療指數(shù)(Narrow therapeutic index,NTI)藥物或窄治療窗藥物一般是指劑量或血藥濃度的微小變化即可能導(dǎo)致治療失敗和/或嚴(yán)重不良反應(yīng),進(jìn)而危及生命,或者導(dǎo)致永久或嚴(yán)重的殘疾或功能喪失的藥物。
窄治療指數(shù)藥物通常具有以下特點(diǎn):有效劑量與中毒劑量(或有效濃度與中毒濃度)接近;血藥濃度低于有效濃度可能導(dǎo)致治療失敗,高于有效濃度可能導(dǎo)致嚴(yán)重不良反應(yīng);需要基于藥動學(xué)或藥效學(xué)指標(biāo)進(jìn)行治療藥物監(jiān)測;具有較低或中等程度的個體內(nèi)變異;臨床應(yīng)用中,劑量調(diào)整幅度通常較小等。
2019年11月8日的征求意見稿《已上市化學(xué)藥品藥學(xué)變更研究技術(shù)指導(dǎo)原則》附錄三,公布了窄治療指數(shù)藥物目錄,氨茶堿、茶堿、膽茶堿、雙羥丙茶堿、苯妥因鈉、丙戊酸、炔雌醇/孕酮制劑、地高辛、洋地黃毒甙、華法令鈉、甲磺酸異他林吸入氣霧劑、卡馬西平、可樂定透皮貼劑、磷酸丙吡胺、硫酸胍乙啶、硫酸奎尼丁、硫酸哌唑嗪、硫酸異丙腎上腺素、米諾地爾、撲米酮、碳酸鋰、鹽酸克林霉素、鹽酸可樂定、鹽酸普魯卡因胺、divalproex鈉、左甲狀腺素鈉、環(huán)孢霉素A、他克莫司、西羅莫司、丙戊酸/丙戊酸鈉。以上藥物如無特別標(biāo)明,一般指口服給藥制劑。
二、窄治療指數(shù)藥物BE設(shè)計
與高變異藥物不同的是,窄治療指數(shù)藥物BE研究總體設(shè)計只能是完全重復(fù)(兩制劑、兩序列、四周期)交叉設(shè)計。而高變異藥物研究總體設(shè)計可以是完全重復(fù)交叉設(shè)計,也可以是部分重復(fù)(兩制劑、三序列、三周期)交叉設(shè)計,特殊情況下(如長半衰期)還可以采用平行組設(shè)計。這是因為只有完全重復(fù)設(shè)計才能求出窄治療指數(shù)藥物BE判定的第三條指標(biāo),即比較受試制劑與參比制劑的個體內(nèi)標(biāo)準(zhǔn)差。完全重復(fù)交叉設(shè)計,同一個受試者既吃兩次參比制劑,又吃兩次受試制劑,如下圖。而部分重復(fù)交叉設(shè)計的受試制劑沒有被吃兩次,所以無法計算受試制劑的個體內(nèi)標(biāo)準(zhǔn)差。

三、窄治療指數(shù)藥物BE判定標(biāo)準(zhǔn)
與一般化學(xué)藥物相比,窄治療指數(shù)藥物進(jìn)行生物等效性評價時,應(yīng)采用更嚴(yán)格的等效性判定標(biāo)準(zhǔn),以保證有效性和安全性。窄治療指數(shù)藥物等效性判定標(biāo)準(zhǔn)需要同時滿足以下三個標(biāo)準(zhǔn)。
3.1、采用參比制劑標(biāo)度的平均生物等效性方法(RSABE)評價等效性,即(YT-YR)2-θSWR2的單側(cè)95%置信區(qū)間上限≤零。這一條判定標(biāo)準(zhǔn)與高變異藥物相同,是ABE公式的變換形式,只是θ值有變化,其中△=1/0.9≈1.11,σw0=0.1,即θ≈1.11。

因為判定公式(YT-YR)2-θSWR2是平方形式,為正值,去掉平方后,會出現(xiàn)正負(fù)值。當(dāng)受試比參比大時,為正值,當(dāng)受試比參比小時,為負(fù)值。所以判定公式評價的仍然是經(jīng)過參比制劑個體內(nèi)變異校正的置信區(qū)間范圍,即在90.00%-111.11%(變異10%時)的基礎(chǔ)上調(diào)整,如下表和下圖所示,變異越小的藥物得到的置信區(qū)間范圍越窄,分界線在CV%約為21.5%的地方。
| 分類 | 幾何均值比 | 取對數(shù) | 等效區(qū)間范圍 |
|---|---|---|---|
| ABE | a/b | Ln(a/b) = Y<sub>T</sub>-Y<sub>R</sub> | (Y<sub>T</sub>-Y<sub>R</sub>)<sup>2</sup> < (Ln1.25)<sup>2</sup>,即:80.00% ≤ a/b ≤ 125.00% |
| RSABE | a/b | Ln(a/b) = Y<sub>T</sub>-Y<sub>R</sub> | (Y<sub>T</sub>-Y<sub>R</sub>)<sup>2</sup> < (Ln1.11)<sup>2</sup>(S<sub>WR</sub>/σ<sub>wo</sub>)<sup>2</sup>,即:90.00%·S<sub>WR</sub>/σ<sub>wo</sub> ≤ a/b ≤ 111.11%·S<sub>WR</sub>/σ<sub>wo</sub> |

3.2、采用平均生物等效性方法評價等效性。這一條判定標(biāo)準(zhǔn)與高變異藥物不完全相同,高變異藥物要求的是點(diǎn)估計,而窄治療窗藥物要求的是區(qū)間估計。窄治療指數(shù)藥物這一條與常規(guī)藥物評價標(biāo)準(zhǔn)一致,即受試制劑與參比制劑的主要藥動學(xué)參數(shù)幾何均值比的雙側(cè)90%置信區(qū)間應(yīng)在80.00%~125.00%范圍內(nèi)。為什么增加這一條限定?主要目的是不希望擁有較大σWR的產(chǎn)品(≥0.213)置信區(qū)間超出80.00%~125.00%的范圍。如下表所示,當(dāng)變異系數(shù)CV%≥21.5%時,窄治療指數(shù)藥物采用參比制劑標(biāo)度的置信區(qū)間范圍將超限,若僅有等效性判定第一條,將無法保證窄治療窗藥物(變異大于21.5%產(chǎn)品)的安全性和有效性。
|
等效區(qū)間范圍
|
SWRSWR? | CV% | 參比標(biāo)度的置信區(qū)間 |
|
(YT−TR)2<(ln1.11)2×(SWR/σwo)2(YT?−TR?)2<(ln1.11)2×(SWR?/σwo?)2 即:90.00% SWR/σwo<a/b<111.11% SWR/σwoSWR?/σwo?<a/b<111.11% SWR?/σwo? |
0.294 | 30 | 73.40%-136.24% |
| 0.213 | 21.5 | 79.93%-125.10% | |
| 0.198 | 20 | 81.17%-123.20% | |
| 0.149 | 15 | 85.46%-117.02% | |
| 0.1 | 10 | 90.00%-111.11% | |
| 0.05 | 5 | 94.87%-105.41% |
為什么針對這一條,高變異藥物可以使用點(diǎn)估計,而窄治療窗藥物卻采用區(qū)間估計?這是因為高變異藥物第二條標(biāo)準(zhǔn)如果采用區(qū)間估計,會讓第一條標(biāo)準(zhǔn)失去意義。如果高變異藥物第二條標(biāo)準(zhǔn)的區(qū)間估計在80.00%~125.00%范圍內(nèi),則和普通藥物完全一致,第一條也一定能通過,也就失去了參比制劑標(biāo)度的意義。
3.3、比較受試制劑與參比制劑的個體內(nèi)標(biāo)準(zhǔn)差。相比高變異藥物,這一條為新增標(biāo)準(zhǔn)。高變異藥物僅要求與文獻(xiàn)報道值的變異進(jìn)行比較,并未明確差異的可接受度。而窄治療窗藥物除了要求與文獻(xiàn)報道值進(jìn)行比較外,還對受試制劑和參比制劑個體內(nèi)標(biāo)準(zhǔn)差的比值進(jìn)行了限定,即σWT/σWR的雙側(cè)90%置信區(qū)間上限應(yīng)≤2.5。

因為分母為F分布值,查表可得。樣本量越大, 越小,因為
越小,因為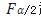 和
和 互為倒數(shù)關(guān)系,即
互為倒數(shù)關(guān)系,即 ,所以
,所以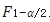
越大,即置信區(qū)間上限越小。這就是為什么增大樣本量,也更容易等效的原因。
雖然高變異藥物有兩條判定標(biāo)準(zhǔn),但是僅有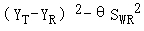 的單側(cè)95%置信區(qū)間上限計算會用到參比制劑和受試制劑的標(biāo)準(zhǔn)差,能滿足上限≤零的前提下,哪怕受試制劑的的標(biāo)準(zhǔn)差大一些,并不會引起安全性和有效性問題,所以可以不要求比較受試制劑和參比制劑的個體內(nèi)標(biāo)準(zhǔn)差。
的單側(cè)95%置信區(qū)間上限計算會用到參比制劑和受試制劑的標(biāo)準(zhǔn)差,能滿足上限≤零的前提下,哪怕受試制劑的的標(biāo)準(zhǔn)差大一些,并不會引起安全性和有效性問題,所以可以不要求比較受試制劑和參比制劑的個體內(nèi)標(biāo)準(zhǔn)差。
而窄治療指數(shù)藥物的前兩條判定標(biāo)準(zhǔn)計算都會用到參比制劑和受試制劑的標(biāo)準(zhǔn)差。在兩條標(biāo)準(zhǔn)都滿足的前提下,如果受試制劑的變異明顯比參比制劑大,受試制劑也有可能會引起安全性和有效性風(fēng)險。這是因為窄治療窗藥物通常具有較低或中等程度的個體內(nèi)變異,且對安全性和有效性的要求更高。
以樣本量24為例,針對不同變異情況的藥物,估算受試制劑與參比制劑個體內(nèi)標(biāo)準(zhǔn)差理論最大差異,見下表。
|
CV% |
SWR |
SWT |
SWT-SWR |
置信區(qū)間上限(應(yīng)<2.5) |
|---|---|---|---|---|
|
5 |
0.050 |
0.087 |
0.037 |
2.513 |
|
10 |
0.100 |
0.174 |
0.074 |
2.512 |
|
15 |
0.149 |
0.259 |
0.110 |
2.507 |
|
20 |
0.198 |
0.344 |
0.149 |
2.508 |
|
21.5 |
0.213 |
0.340 |
0.156 |
2.506 |
|
30 |
0.294 |
0.470 |
0.215 |
2.503 |
由上表可知,隨著變異系數(shù)的增加,能夠接受的受試制劑和參比制劑差異也越大。這一結(jié)論與高變異藥物一致。
四、窄治療指數(shù)藥物BE計算步驟
4.1 計算參比制劑的個體內(nèi)標(biāo)準(zhǔn)差
與高變異藥物一樣,采用以下公式計算,需要采用自然對數(shù)轉(zhuǎn)化后的藥動學(xué)參數(shù)計算。受試制劑的個體內(nèi)標(biāo)準(zhǔn)差SWT計算方法相同。

 為受試者總?cè)藬?shù)(例如32例受試者),ni為第i個序列中受試者人數(shù)(總?cè)藬?shù)除以2,第1序列16人,第2序列16人),m為序列數(shù)(窄治療窗為2序列),i為研究中的序列編號(第1序列和第2序列),j為序列內(nèi)受試者編號(如編號001、002……032),Dij=Rij1-Rij2表示參比制劑前后吃兩次的差值(對數(shù)轉(zhuǎn)換后),
為受試者總?cè)藬?shù)(例如32例受試者),ni為第i個序列中受試者人數(shù)(總?cè)藬?shù)除以2,第1序列16人,第2序列16人),m為序列數(shù)(窄治療窗為2序列),i為研究中的序列編號(第1序列和第2序列),j為序列內(nèi)受試者編號(如編號001、002……032),Dij=Rij1-Rij2表示參比制劑前后吃兩次的差值(對數(shù)轉(zhuǎn)換后), 表示求該序列內(nèi)前后吃兩次差值的平均值(1和2序列應(yīng)分別計算)。
表示求該序列內(nèi)前后吃兩次差值的平均值(1和2序列應(yīng)分別計算)。
4.2 計算以下算式的單側(cè)95%置信區(qū)間上限:

(YT-YR)2-θSWR2的單側(cè)95%置信區(qū)間上限應(yīng)≤零。其中YT和YR分別表示受試制劑和參比制劑自然對數(shù)轉(zhuǎn)換后的AUC或Cmax的均值。θ已知約為1.11,SWR在上步已經(jīng)求出。在上篇文章《如何讓高變異藥物更容易BE等效》中介紹了計算方法,置信區(qū)間上限U的計算參照下面公式,U=點(diǎn)估計值+估計誤差。需要知道三個數(shù)據(jù):受試制劑和參比制劑Cmax/AUC取自然對數(shù)后的平均差(YT-YR)、參比制劑和受試制劑的個體內(nèi)標(biāo)準(zhǔn)差SWR和SWT、參比制劑和受試制劑的樣本量nR和nT。

按照3.3項下,將受試制劑和參比制劑的個體內(nèi)差異取到上限附近,假設(shè)樣本量24,滿足等效情況下,受試樣品和參比制劑藥動參數(shù)幾何均值比的最大取值范圍見下表。
|
CV% |
SWR |
SWT |
SWT/SWR 置信區(qū)間上限(應(yīng)<2.5) |
幾何均值置信區(qū)間 |
|---|---|---|---|---|
|
5 |
0.050 |
0.086 |
2.485 |
98%-102% |
|
10 |
0.100 |
0.173 |
2.497 |
95%-105% |
|
15 |
0.149 |
0.258 |
2.497 |
93%-107% |
|
20 |
0.198 |
0.343 |
2.500 |
91%-110% |
|
21.5 |
0.213 |
0.368 |
2.499 |
90%-111% |
|
30 |
0.294 |
0.508 |
2.498 |
87%-115% |
由上表可知:如果受試制劑和參比制劑兩者的個體內(nèi)變異相差較大(一般是制劑質(zhì)量因素導(dǎo)致),與正常變異情況的3.2項表對比,受試制劑和參比制劑藥動參數(shù)的比值范圍將縮小,這就增加了BE等效難度。
4.3 計算平均生物等效置信區(qū)間:
與常規(guī)藥物的計算方法一致,采用ABE方法計算受試制劑和參比制劑的主要藥動學(xué)參數(shù)幾何均值比的雙側(cè)90%置信區(qū)間,應(yīng)在80.00%~125.00%范圍內(nèi)。需要注意的是,對數(shù)轉(zhuǎn)換后,仍然不能按照求平均值的方式用excel直接計算,需要采用混合效應(yīng)模型的最小二乘法計算,通常需要專業(yè)的統(tǒng)計軟件,如Phoenix WinNonlin或SAS。
最小二乘法,我們做分析方法學(xué)的線性時會用到,只不過分析方法只有一個變量,就是濃度因素,屬于一元線性回歸;而BE試驗有多個變量,如制劑、周期、序列、受試者等因素,屬于多元線性回歸。
4.4 計算受試制劑與參比制劑個體內(nèi)標(biāo)準(zhǔn)差比值置信區(qū)間:
受試制劑與參比制劑個體內(nèi)標(biāo)準(zhǔn)差比值(σWT/σWR)的雙側(cè)90%置信區(qū)間(即α=0.1)計算如下式:

SWT和SWR在4.1步中均已經(jīng)求出來, 值可以通過查表得到,
值可以通過查表得到, 。不同例數(shù)的F理論值見下表,最后一列作為分母用來求置信區(qū)間上限,因為分母小于1(在0.5附近),所以受試制劑的變異通常不會比參比制劑的變異大1.5倍。
。不同例數(shù)的F理論值見下表,最后一列作為分母用來求置信區(qū)間上限,因為分母小于1(在0.5附近),所以受試制劑的變異通常不會比參比制劑的變異大1.5倍。

自由度一般是總例數(shù)減去2,需要注意的是,在正式試驗中,因受試者脫落的影響,受試組和參比組的自由度可能會不相同。
4.5 判定等效性:
只有主要藥動學(xué)參數(shù)(AUC0-t、AUC0-∞和Cmax)同時符合上述三個等效性判定標(biāo)準(zhǔn)(即采用RSABE方法評價等效性、采用ABE 方法評價等效性和比較受試制劑與參比制劑的個體內(nèi)標(biāo)準(zhǔn)差),才可判定受試制劑與參比制劑具有生物等效性。
五、結(jié)語
對于藥學(xué)開發(fā)人員來說,對BE試驗和數(shù)據(jù)接觸的相對較少,為了便于理解,我們拿溶出曲線做個類比。當(dāng)溶出曲線各時間點(diǎn)數(shù)據(jù)RSD符合要求時,采用f2比較相似性,f2比較采用的是每個時間點(diǎn)的均值,就是點(diǎn)估計。當(dāng)RSD不符合要求時,推薦采用bootstrap法比較相似性,bootstrap法比較,通過模擬重復(fù)抽樣,得到每個時間點(diǎn)圍繞均值的上下波動限度,也就是置信區(qū)間。f2法和bootstrap法基于相同的統(tǒng)計邏輯,而多變量置信區(qū)間法(MSD)邏輯則不同。受參比制劑批次限制,采用MSD方法,很多時候參比制劑自身也很難相似,這也是為什么ICH《M13B:其他規(guī)格的生物等效性豁免》中已經(jīng)不再提到MSD法的原因。有興趣了解細(xì)節(jié)的朋友,可以閱讀往期文章《溶出曲線RSD偏大之“多變量置信區(qū)間法”》。
一般藥物BE試驗的ABE判定標(biāo)準(zhǔn),我們可以理解為點(diǎn)估計和區(qū)間估計都要在80.00%~125.00%范圍內(nèi)。高變異藥物BE試驗的RSABE判定標(biāo)準(zhǔn),可以理解為點(diǎn)估計在80.00%~125.00%范圍內(nèi),區(qū)間估計在參比制劑校正后的范圍內(nèi)。窄治療指數(shù)藥物BE試驗的RSABE判定標(biāo)準(zhǔn),可以理解為區(qū)間估計既要在ABE的范圍內(nèi),又要在參比制劑校正后的范圍內(nèi),且兩制劑的變異情況不能相差太大。通過高變異藥物和窄治療窗藥物BE邏輯分析,我們發(fā)現(xiàn)BE難度隨著變異系數(shù)減小而上升,這是因為變異系數(shù)越小,要求受試制劑和參比制劑之間的差異也越小。這如同壓片一樣,片重越小的藥片,對物料屬性和壓片機(jī)精度要求越高,越難控制。理解BE試驗數(shù)據(jù)統(tǒng)計的底層邏輯,有助于藥品開發(fā)人員提升質(zhì)量源于設(shè)計(QbD)理念的理解,提高自己對藥品質(zhì)量的把控度,真的做到仿制藥與參比制劑質(zhì)量和療效一致性。

來源:藥知曉


