您當(dāng)前的位置:檢測資訊 > 科研開發(fā)
嘉峪檢測網(wǎng) 2022-01-27 10:39
更多醫(yī)藥技術(shù)資訊,請點擊醫(yī)藥專欄:http://drug.anytesting.com/ 歡迎關(guān)注文末微信公眾號:藥研檢測drugtest
今日頭條
國內(nèi)藥訊
1.百時美施貴寶FIC貧血新藥在華獲批。百時美施貴寶旗下新基公司開發(fā)的“first-in-class”紅細胞成熟劑注射用羅特西普(luspatercept)獲NMPA批準(zhǔn)上市,用于治療需要定期輸注紅細胞的成人β-地中海貧血患者。luspatercept已在美國、加拿大和歐盟獲批上述適應(yīng)癥,并在美國和歐盟獲批治療某些血液疾病患者出現(xiàn)的貧血。此外,luspatercept用于治療非輸血依賴性β地中海貧血成人患者的補充上市申請也于日前獲FDA授予優(yōu)先審評資格。
2.TROP-2 ADC啟動中國隊列III期臨床。阿斯利康與第一三共聯(lián)合開發(fā)的TROP-2 ADC藥物Dato-DXd在國內(nèi)登記啟動首項臨床。這是國際Ⅲ期臨床TROPION-Breast01研究的中國部分,擬在全球招募700人,其中國內(nèi)106人,評估在接受化療后出現(xiàn)疾病進展的無法手術(shù)或轉(zhuǎn)移性激素受體陽性、HER2陰性乳腺癌患者中比較Dato-DXd與研究者所選化療的有效性與安全性。試驗的雙重主要終點為BICR評估的PFS和OS。
3.泰它西普治療干燥綜合征Ⅱ期臨床積極。榮昌生物創(chuàng)新生物藥泰它西普(RC18)治療原發(fā)性干燥綜合征的中國Ⅱ期臨床結(jié)果積極。FAS集結(jié)果顯示,與安慰劑相比,泰它西普(160mg)使患者ESSDAI評分較基線的變化差異具統(tǒng)計學(xué)意義。PPS集結(jié)果顯示,泰它西普兩個治療組與安慰劑組相比,ESSDAI評分較基線變化值差異也具有顯著性。RC18是BLyS/APRIL雙靶點新型融合蛋白,去年3月獲批國內(nèi)上市,用于治療系統(tǒng)性紅斑狼瘡。
4.天士力NASH新藥在美獲批臨床。天士力旗下天士力生物開發(fā)的擬用于治療非酒精性脂肪性肝炎(NASH)的B1344注射液獲FDA臨床許可。B1344是聚乙二醇化的重組人成纖維細胞生長因子21突變體,通過與共受體β-klotho蛋白與成纖維細胞生長因子受體(FGFR)結(jié)合,激活下游信號分子通路,參與多個糖脂代謝疾病的病理生理過程。臨床前研究顯示,B1344可顯著降低模型動物的肝臟脂肪變性、氣球樣變性和肝小葉炎癥程度。
5.信達VEGF靶點眼科品種報IND。信達生物治療用生物制品1類新藥IBI324的臨床試驗申請獲CDE受理。據(jù)該公司公布于2022 JPM大會上的最新信息,這是一款VEGF/ANG-2雙抗,擬開發(fā)用于眼科疾病的治療。此次為該新藥首次申報臨床。據(jù)悉,信達目前擁有3款VEGF靶向雙抗,臨床進展最快的VEGF/C3補體雙特異性抗體IBI302,目前正在II期臨床中評估用于治療濕性年齡相關(guān)性黃斑變性和糖尿病黃斑水腫的潛力。
6.譽衡生物與藝妙神州開展聯(lián)合用藥研究。譽衡生物PD-1單抗賽帕利單抗注射液(譽妥®,zimberelimab)擬與藝妙神州在研IM83 CAR-T開展聯(lián)合用藥臨床研究,評估這一組合方案用于治療晚期肝細胞癌的有效性與安全性。譽妥已獲NMPA批準(zhǔn)治療二線以上復(fù)發(fā)或難治性經(jīng)典型霍奇金淋巴瘤;目前也正在臨床中評估治療晚期肝癌、宮頸癌等多種實體瘤的潛力。在肝癌小鼠模型中,IM83 CAR-T也顯示出顯著且持久的抑瘤效果。
國際藥訊
1.創(chuàng)新SGLT-2抑制劑Ⅲ期臨床積極。Daewoong公司SGLT-2抑制劑enavogliflozin治療2型糖尿病的2項Ⅲ期臨床結(jié)果積極。與安慰劑組相比,enavogliflozin單藥治療組24周后患者HbA1c水平較基線變化值差異為0.99%,具統(tǒng)計學(xué)顯著性(p<0.001)。與dapagliflozin聯(lián)合二甲雙胍治療相比,enavogliflozin與二甲雙胍聯(lián)用達到非劣效性標(biāo)準(zhǔn);而且enavogliflozin給藥組也表現(xiàn)出良好安全性特征。最終報告將在今年下半年發(fā)布。該公司計劃盡快遞交監(jiān)管申請。
2.雙重機制PD-L1單抗皮膚癌臨床積極。Checkpoint公司基于T細胞和自然殺傷細胞的雙重作用機制的PD-L1抗體cosibelimab在治療轉(zhuǎn)移性皮膚鱗狀細胞癌(cSCC)的關(guān)鍵臨床達到主要終點。cosibelimab在這類患者中達到47.4%(95% CI:36.0,59.1)的客觀緩解率;數(shù)據(jù)截止時,患者的中位緩解持續(xù)時間尚未達到;安全性和耐受性特征與既往研究一致。Checkpoint計劃在今年年底向FDA遞交生物制品許可申請。
3.NASH創(chuàng)新療法概念驗證臨床積極。89bio公司開發(fā)的“best-in-class”FGF21類似物pegozafermin(BIO89-100),在用于治療非酒精性脂肪性肝炎(NASH)的Ⅰb/Ⅱa期概念驗證臨床中獲得積極結(jié)果。在20例患者組成的患者隊列中,63%的患者達到NAS評分改善2分以上并且纖維化沒有惡化;32%的患者達到NASH癥狀清除并且肝纖維化沒有惡化的標(biāo)準(zhǔn),26%的患者達到肝纖維化改善一級并且NASH癥狀未惡化的標(biāo)準(zhǔn),47%的患者獲得NASH癥狀清除或肝纖維化改善。
4.新一代基因編輯公司完成B輪融資。Metagenomi公司宣布完成數(shù)額為1.75億美元的B輪融資。Metagenomi的基因編輯發(fā)現(xiàn)與開發(fā)平臺,使用人工智能的云計算,從大量宏基因組數(shù)據(jù)中發(fā)現(xiàn)天然核酸酶,再改造生成基因編輯療法。該公司開發(fā)的基因編輯工具包括CRISPR基因編輯系統(tǒng)、超小型堿基編輯系統(tǒng)、和CRISPR相關(guān)轉(zhuǎn)座酶(CAST)系統(tǒng)。此輪融資將用于推動該公司的主打體內(nèi)和體外基因編輯項目進入臨床。
5.吉利德撤回PI3K抑制劑兩項適應(yīng)癥。吉利德日前宣布從美國撤回PI3K抑制劑Zydelig在加速批準(zhǔn)途徑下獲得的兩個適應(yīng)癥,分別為用于治療復(fù)發(fā)性濾泡性淋巴瘤(FL)和復(fù)發(fā)性小淋巴細胞性淋巴瘤(SLL)。吉利德表示,目前這兩種惰性非霍奇金淋巴瘤亞型(FL和SLL)的治療格局已發(fā)生變化,招募患者參加Zydelig的確證性臨床研究成為挑戰(zhàn)。此前,由于安全問題,Zydelig與Rituxan聯(lián)合治療臨床試驗被提前終止。
6.強生2021年財報出爐。強生公布2021年業(yè)績,全年實現(xiàn)總收入937.75億美元,同比增長13.6%;其中制藥業(yè)務(wù)收入520.8億美元(+14.3%),醫(yī)療器械業(yè)務(wù)收入270.6億美元(+17.9%),消費者保健業(yè)務(wù)收入146.35億美元(+4.1%)。全年研發(fā)投入147.14億美元,同比增長21%。制藥業(yè)務(wù)增長主要來源于Stelara(烏司奴單抗,91.34億美元)、Darzalex(達雷妥尤單抗,60.23億美元)、Imbruvica(依布替尼,43.69億美元)等推動。此外,新冠疫苗銷售收入為24億美元。
醫(yī)藥熱點
1.中醫(yī)藥事業(yè)發(fā)展最新統(tǒng)計報告發(fā)布。國家中醫(yī)藥管理局日前印發(fā)《2020年中醫(yī)藥事業(yè)發(fā)展統(tǒng)計提要報告》。根據(jù)《報告》,在中醫(yī)醫(yī)療資源方面,2020年與2019年相比,全國中醫(yī)類醫(yī)療衛(wèi)生機構(gòu)達到7.2萬個(+9.9%),中醫(yī)類床位數(shù)為143.3萬張(+7.8%),全國中醫(yī)藥人員總數(shù)為83.1萬人(+8.3%),其中基層中醫(yī)類別執(zhí)業(yè)(助理)醫(yī)師達18.4萬人(+11.3%)。在中醫(yī)醫(yī)療服務(wù)方面,2020年全國中醫(yī)總診療量為10.6億人次(-9.1%),中醫(yī)總診療量占全國總診療量的16.8%(+0.4%)。
2.上海推出養(yǎng)老床位統(tǒng)籌及輪候試點。上海市日前發(fā)布《上海市養(yǎng)老床位統(tǒng)籌及輪候試點工作方案》,在區(qū)級及市級層面建立保基本養(yǎng)老床位統(tǒng)籌機制,有效保障老年人的入住需求,提供具有專業(yè)照護能力的養(yǎng)老機構(gòu)供老年人選擇。據(jù)悉,經(jīng)老年照護統(tǒng)一需求評估達到一定等級要求的60歲及以上戶籍老年人,可通過上海市養(yǎng)老服務(wù)平臺“入住養(yǎng)老機構(gòu)申請”入口,進行線上機構(gòu)查詢、入住申請或排隊入住保基本養(yǎng)老機構(gòu)床位。
3.上海公布超“黃線”掛網(wǎng)藥品名單。1月26日,上海陽光醫(yī)藥采購網(wǎng)發(fā)布《關(guān)于公布2021年11月份藥品掛網(wǎng)公開議價超“黃線”幅度較大采購品種名單的通知》,其中,共涉及15個掛網(wǎng)公開議價超“黃線”幅度排名靠前且有一定采購金額的品種,包括10個新申請品種 (15個新申請品規(guī))和5個原在庫品種。吉林津升制藥注射用二羥丙茶堿、海欣藥業(yè)注射用法莫替丁等“榜上有名”。
評審動態(tài)
1. CDE新藥受理情況(01月26日)
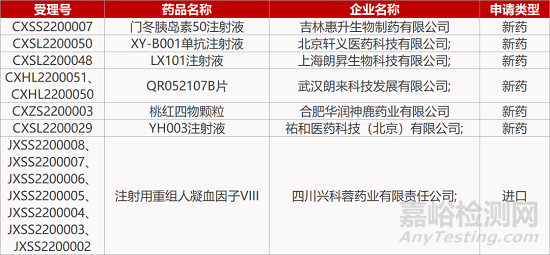
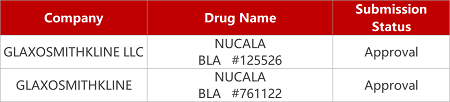

來源:藥研發(fā)


