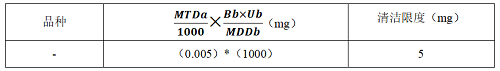引言
在《藥品共線生產質量管理指南(征求意見稿)》出臺之前,制藥企業常用的清潔限度的算法有最低日治療劑量的1/1000、10ppm、半數致死量LD50, 2021年11月,中國CFDI出臺了《藥品共線生產質量管理指南(征求意見稿)》,提供了更具有科學性和優勢的方法,即基于健康的暴露限度(ADE/PDE)。
本文就這四種清潔限度算法進行詳細解析,并舉例對比,為制藥企業科學合理的選擇清潔限度算法提供一些思考。
1、清潔限度算法詳解
1.1 最低日治療劑量的1/1000
(1)概念
最低日治療劑量的1/1000是指:下批產品的最高日服用劑量中含有上批產品的量不應超過上批產品的最低日治療劑量的1/1000,以此標準來確定殘留物限度。
(2)計算
MTDa:清潔前產品(目標化合物)最小每日給藥劑量中的活性成分含量(mg);
Bb:清潔后產品的批量(支/瓶);
Ub:清潔后產品的每支含量(mg);
MDDb:清潔后產品(目標化合物)最大每日給藥劑量中的活性成分含量(mg);
(3)公式解析
①a品種專用
MTDa對特定品種a是固定值,根據生產線所有品種,選擇 最小值,即為a品種專用限度。
最小值,即為a品種專用限度。
②全品種可用
根據生產線所有品種,選擇MTD最小值,選擇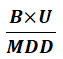 最小值,即為該生產線全品種皆可用限度。
最小值,即為該生產線全品種皆可用限度。
1.2 殘留物濃度10ppm
(1)概念
《藥品生產驗證指南》指出除高活性,高致敏性藥品外,10ppm是足夠安全的,衍生出了以10ppm為限度計算殘留物濃度,即,將10ppm簡化為最終淋洗水中樣品殘留物濃度限值為10ppm。
(2)計算
Bb:清潔后產品的批量(kg);
10ppm:10×10-6,即10mg/kg;
F:為安全因子系數,根據風險評估,一般取2-10;
(3)公式解析
①全品種可用
根據生產線所有品種,選擇最小批量進行計算,即為該生產線全品種皆可用限度。
1.3 基于毒理數據半數致死量(LD50)
(1)概念
半數致死量(LD50)相較于其他毒理數據是易于得到的,基于毒理數據半數致死量(LD50)計算清潔限度是指,通過將半數致死量(LD50)合理外推為NOEL(無可見作用水平),再進一步將NOEL(無可見作用水平)外推為ADI(日允許攝入量),從而計算產品的清潔限度。
(2)計算
ADI:每日允許攝入量(mg);
Bb:清潔后產品的批量(支/瓶);
Ub:清潔后產品的每支含量(mg);
MDDb:清潔后產品(目標化合物)最大每日給藥劑量中的活性成分含量(mg);
SF:由NOEL推導至ADI的安全因子,對于制劑,一般取1000;對于API,一般為100~1000;對于清潔劑的殘留計算,若為外用制劑為10~100,若為固體制劑為100~1000,若為注射劑為1000~10000;
BW:服用清潔后產品的患者體重,通常使用50kg;
2000為由LD50推導至NOEL的安全因子;
(3)公式解析
①a品種專用
根據生產線所有品種,選擇 最小值,即為a品種專用限度。
最小值,即為a品種專用限度。
②全品種可用
根據生產線所有品種,選擇LD50最小值,選擇 最小值,即為該生產線全品種皆可用限度。
最小值,即為該生產線全品種皆可用限度。
1.4 基于健康的暴露限度(ADE/PDE)
(1)概念
可接受日暴露劑量(ADE)或允許日接觸劑量(PDE)是指患者終生每天暴露于該濃度,但對健康的不良影響仍處可接受風險水平。CFDI發布的《藥品共線生產質量管理指南(征求意見稿)》中認可了活性物質殘留限度標準應當基于產品毒理試驗數據或毒理學文獻資料的評估建立,基于健康的暴露限度(HBEL)的可接受標準(如ADE/PDE值)在評估清潔殘留數據時比傳統方法更具有科學性和優勢。
(2)計算



(3)公式解析
①a品種專用
根據生產線所有品種,選擇 最小值,即為a品種專用限度。
最小值,即為a品種專用限度。
②全品種可用
根據生產線所有品種,選擇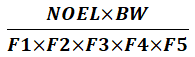 最小值,選擇
最小值,選擇 最小值,即為該生產線全品種皆可用限度。
最小值,即為該生產線全品種皆可用限度。
2、舉例計算某一生產線的清潔限度
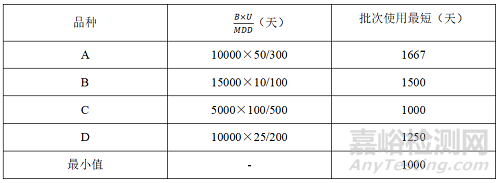
某一生產線已有在產品種3個分別為品種A、B、C,現計劃增加新品種D,需計算品種D的清潔限度。
2.1 生產線產品信息匯總

2.2 最低日治療劑量的1/1000
(1)MTD/1000
(2) 
(3)D品種專用
(4)全品種皆可用
2.3 殘留物濃度10ppm
(1)批量

(2)D品種專用

(3)全品種皆可用

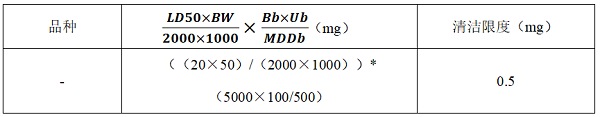
2.4 基于毒理數據半數致死量(LD50)
(1)LD50
(2) 
(3)D品種專用
(4)全品種皆可用
2.5 基于健康的暴露限度(ADE/PDE)
(1)PDE
(2)

(3)D品種專用

(4)全品種皆可用
3、上述計算方法的最小值
3.1 D品種專用

3.2 全品種皆可用
4、各國對清潔限度的要求
4.1 中國
參考《中國藥品GMP指南》、《藥品共線生產質量管理指南(征求意見稿)》、《GB/T36030-2018制藥機械設備CIP/SIP通用技術要求》采用了四種計算方式,即最低日治療劑量的1/1000、10ppm、半數致死量LD50、基于健康的暴露限度(ADE/PDE)。
《藥品共線生產質量管理指南(征求意見稿)》雖然明確指出基于健康的暴露限度(ADE/PDE)是更具有科學性和優勢的方法,但是制藥企業現下還需基于上述四種計算方式,選擇最低的限度作為清潔驗證的控制限度。
4.2 歐盟
EMA《Guideline on Setting Health Based Exposure Limits for Use in Risk Identification in the Manufacture of Different Medicinal Products in Shared Facilities(在共用設施中生產不同藥品使用風險辨識建立基于健康的暴露限度指南)》中明確指出,所有藥品均應建立基于健康的暴露限度,并指出傳統的最低日治療劑量的1/1000、10ppm未考慮到目標殘留物的毒理學數據,所得到的限度太嚴格或者控制不足,缺乏充足的科學依據。同時特別強調半數致死量LD50不能用于計算殘留限度。
4.3 美國
FDA的《GUIDE TO INSPECTIONS VALIDATION OF CLEANING PROCESSES(清潔工藝指南)》也未明確建立統一的清潔殘留方法,但提出了半數致死量LD50、基于健康的暴露限度(ADE/PDE)適用于高毒有害物質清潔殘留的計算,毒理學閾值1.5 μg/天適用于基因毒物質清潔殘留的計算,一般藥品(非高毒高活、非基因毒等藥品)則使用最低日治療劑量的1/1000、10ppm、基于健康的暴露限度(ADE/PDE)計算清潔殘留,選擇最低值作為清潔殘留限度。
5、科學合理的選擇
根據對主流國家清潔限度計算方法的分析,比較認可的計算方法有最低日治療劑量的1/1000、10ppm、基于健康的暴露限度(ADE/PDE),綜合計算分析選擇最低值作為清潔殘留限度。
6、對國內制藥企業的建議
CFDI并未摒棄半數致死量LD50,清潔殘留限度需綜合計算分析最低日治療劑量的1/1000、10ppm、半數致死量LD50、基于健康的暴露限度(ADE/PDE),選擇最低值作為清潔殘留限度。
7、對清潔限度算法選擇的思考
隨著毒理數據的完備,使用更加科學合理的基于健康的暴露限度(ADE/PDE)計算清潔限度會成為主流算法。
基于綜合分析,對清潔限度算法排序:基于健康的暴露限度(ADE/PDE)>最低日治療劑量的1/1000>10ppm>半數致死量LD50
對于未查出基于健康的暴露限度(ADE/PDE)的品種可基于上述排序選擇算法進行計算。
上述只是作者對怎么科學合理的選擇清潔限度算法的一些思考,在CFDI未發布明確的清潔限度算法指導原則前,制藥企業還需綜合計算分析最低日治療劑量的1/1000、10ppm、半數致死量LD50、基于健康的暴露限度(ADE/PDE),選擇最低值作為清潔驗證限度。
參考資料
1、《化學藥品注射劑仿制藥質量和療效一致性評價技術要求》
2、《藥品共線生產質量管理指南(征求意見稿)》
3、《中國藥品GMP指南》
4、《GB/T36030-2018制藥機械設備CIP/SIP通用技術要求》
5、《Guideline on Setting Health Based Exposure Limits for Use in Risk Identification in the Manufacture of Different Medicinal Products in Shared Facilities(在共用設施中生產不同藥品使用風險辨識建立基于健康的暴露限度指南)》
6、《GUIDE TO INSPECTIONS VALIDATION OF CLEANING PROCESSES(清潔工藝指南)》
7、《Cross-contamination control and Health Based Exposure Limits (HBEL) Q&As交叉污染控制與基于健康的暴露限(HBEL)問答》
8、ICH Q3C:殘留溶劑的指導原則
9、ICH Q3D(R2):元素雜質指導原則
10、ICH Q9 :質量風險管理
11、ICH M7:評估和控制藥物中的DNA活性(致突變)雜質以限制潛在的致癌風險
12、《關于在清潔驗證中引入HBEL的考量》
13、《APIC原料藥工廠中清潔驗證指南》


 最小值,即為a品種專用限度。
最小值,即為a品種專用限度。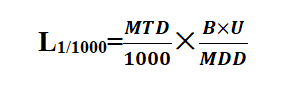
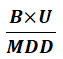 最小值,即為該生產線全品種皆可用限度。
最小值,即為該生產線全品種皆可用限度。
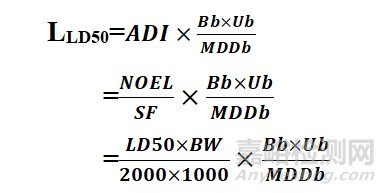
 最小值,即為a品種專用限度。
最小值,即為a品種專用限度。 最小值,即為該生產線全品種皆可用限度。
最小值,即為該生產線全品種皆可用限度。


 最小值,即為a品種專用限度。
最小值,即為a品種專用限度。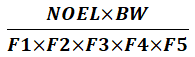 最小值,選擇
最小值,選擇 最小值,即為該生產線全品種皆可用限度。
最小值,即為該生產線全品種皆可用限度。