您當(dāng)前的位置:檢測資訊 > 科研開發(fā)
嘉峪檢測網(wǎng) 2022-08-05 05:58
本文將高壓微射流法與其他納米制備方法進行比較,概述了高壓微射流裝備的結(jié)構(gòu)與工作原理及其在藥物研究中的應(yīng)用,重點介紹了在納米混懸劑和納米乳制備中的應(yīng)用。納米技術(shù)作為新興技術(shù)之一,在現(xiàn)代藥劑學(xué)中 越來越成為研究的熱點。在醫(yī)藥領(lǐng)域中,藥物顆粒的粒徑大小和粒度分布是藥物藥理藥效及使用性能的重要影響因素。與傳統(tǒng)的藥物制劑相比,納米化 藥物具有粒徑小、比表面積大及宏觀量子隧道效應(yīng)等特性,可有效增大藥物尤其是難溶性藥物的飽和 溶解度和溶出速度、增強療效及靶向性、提高生物利用度及吸收穩(wěn)定性、減少藥物用量及降低不良反應(yīng),在醫(yī)藥領(lǐng)域中具有廣闊的應(yīng)用前景。
1 納米制劑制備方法及比較
目前納米制劑制備方法主要分為兩大類,即“自上而下( top down) ”和“自下而上( bottom up) ”。
“自上而下”是指通過機械手段將大的藥物顆粒粉 碎成小的藥物顆粒,常見的有球磨法、超聲法、高壓 均質(zhì)法等。“自下而上”是指將藥物溶解在一種溶劑中,用另一種含有穩(wěn)定劑的反溶劑進行沉淀,常見 的有蒸發(fā)沉淀法、超臨界萃取法等。
高壓均質(zhì)法有兩種均質(zhì)類型,一種是高壓微射 流法,即將大顆粒藥物分散于水溶液或其他溶劑(如乙醇)中,在高達4000bar 的壓力下懸液先通過 “Z”形腔,通過改變幾次液流方向碰撞產(chǎn)生剪切力,后通過通道直徑為 75 μm 的“Y”形腔,兩股液流高 速( > 1 000 m·s - 1 ) 相向碰撞,通過撞擊力、剪切力 及氣穴產(chǎn)生粒度均勻的納米粒。另一種是活塞-狹 縫式均質(zhì)法,即在 100 ~ 2 000 bar 的壓力作用下,含 大顆粒藥物的混懸液通過 5 ~ 20 μm 的狹縫,生成均 勻分散的納米粒。高壓微射流法是一種新型的 納米制劑制備方法,具有能在不破壞藥物活性成分情況下降低藥物的粒徑并使藥物的粒度分布均勻等 優(yōu)點,其處理后的懸浮粒子粒徑可達納米范圍。為 了避免納米藥物團聚,需要加入甘露醇等促進納米 顆粒的分散。將高壓均質(zhì)法的兩種均質(zhì)類型做 了相應(yīng)比較比較如表 1 所示,將高壓微射流法與其 他納米制劑制備方法進行比較如表 2 所示。

2 高壓微射流裝備的結(jié)構(gòu)及工作原理
2.1 高壓微射流裝備的結(jié)構(gòu)
高壓微射流裝備主 要由進料罐、單向閥、液壓泵、增壓器、壓力表、交互 容腔、輔助容腔、回流過濾器、熱交換器和出料口構(gòu)成。交互容腔和輔助容腔組成物料反應(yīng)器,對物 料粉碎起關(guān)鍵作用。物料反應(yīng)器的材質(zhì)金剛石,其具有堅硬、不易磨損、耐腐蝕等特性,可用于高硬度藥物。液壓泵內(nèi)的增壓柱塞采用氧化鋯陶瓷,具有 耐磨損、耐腐蝕且不易產(chǎn)生靜電。高壓微射流裝備的處理壓力可達到30000psi,故工藝流程很穩(wěn)定,其工藝流程如圖 1 所示。
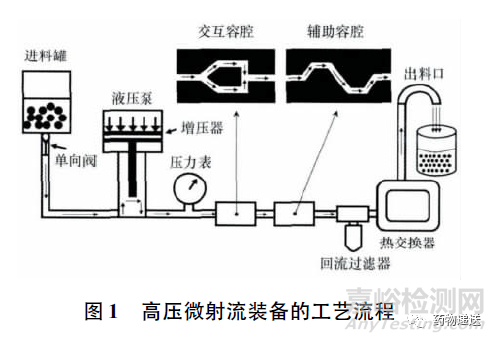
2.2 高壓微射流裝備的工作原理
高壓微射流裝備( MicrofluidicsTM Inc.,U.S.A.) 采用的是氣流粉碎原理,利用液壓泵使流體產(chǎn)生高壓,進而推動 裝有活塞的增壓器,液壓驅(qū)動增壓器內(nèi)的活塞推動 高壓往復(fù)活塞產(chǎn)生一個交替的抽吸,使流體加速,高速進入交互容腔內(nèi),在交互容腔內(nèi)的微孔道(75μm)中,流體被分散成兩股進行強烈的高速撞擊、高速剪切,再進入輔助容腔(200μm) ,在撞擊過程中瞬間轉(zhuǎn)化其大部分能量,從而產(chǎn)生巨大的壓力降,實現(xiàn)高速撞擊、高剪切力、空穴作用、高頻振動等綜合作用,來達到粉碎的目的,使得液滴或者晶體粒徑降低。
3 高壓微射流裝備的應(yīng)用
作為新型納米技術(shù),高壓微射流均質(zhì)技術(shù)具有改性藥物粒徑大小的性能。一般來說,應(yīng)用微射流儀處理藥物顆粒,影響藥物粒徑大小和粒度分布的因素主要有3個,它們分別是處理壓力、循環(huán)次數(shù)以 及藥物本身性質(zhì)有關(guān)。利用高壓微射流裝備只能制備得到納米混懸液和納米乳兩種劑型,與其他方法連用可以制得納米粒、多孔微球等劑型的納米藥物,制得的藥物可用于口服、注射、外用、肺部吸收等。
3.1 納米乳
納米乳是非平衡體系,形成需要外加能量,通常來自機械設(shè)備或化學(xué)制劑的結(jié)構(gòu)潛能,粒徑通常20~200nm。表面活性劑的種類和用量是納米乳穩(wěn)定性的關(guān)鍵。微射流儀能在最短時間內(nèi)提供所需能量并獲得粒徑最小的均勻乳液,故在國內(nèi)外納米乳劑領(lǐng)域研究中被廣泛應(yīng)用。
Siah等將超聲法和高壓微射流法比較制備阿司匹林納米乳,處理壓力為200bar,處理10次,載有阿司匹林納米乳的黏度為3.98cP,平均粒徑為(146.1 ± 1.528)nm,粒度分布均勻,適用于制劑領(lǐng)域。Zhao 等將高壓微射流法和活塞-狹縫均質(zhì)法 進行比較制備靜脈注射脂肪乳,并研究了影響粒徑 大小和粒徑分布的因素。所研究的影響因素從主到次依次為處理壓力/循環(huán)次數(shù)、溫度、蒸汽滅菌、pH 值,而且制備靜脈注射脂肪乳高壓微射流法比活塞-狹縫均質(zhì)法更有效。高壓微射流法制備的脂肪乳具有粒徑小,粒度分布窄等特點。Kotyl等采用兩 種方法制備組分比例相同的 δ-維生素E乳膏。利用高壓微射流裝備制得的納米乳的平均粒徑為65nm,而用傳統(tǒng)方法制得的微米乳的平均粒徑為2788nm。將制得的微/納米乳膏涂抹在已刮掉背毛倉鼠的背部,以2h后微/納米乳膏的生物利用度為基準(zhǔn),3h后測得納米乳膏的生物利用度翻了1倍,而微米乳膏只是2h后的1.1倍。Kakumanu等以吐溫-80為乳化劑,大豆油為油相,利用高壓微射流裝備制備達卡巴嗪納米乳。納米乳的平均粒徑為112nm,ζ電位為-3.2mV,提高其穩(wěn)定性,有效地減小了異種移植老鼠皮膚癌腫瘤的尺寸。
脂質(zhì)體,即單層或多層雙脂膜結(jié)構(gòu)的球形微粒,也是納米乳的一種形式。脂質(zhì)體的制備方法很多,但是多數(shù)不適合大規(guī)模、連續(xù)化生產(chǎn)。高壓微射流均質(zhì)法不僅克服了以上的缺點,而且達到更高的效果。Barnadas-Rodríguez 等利用高壓微射流裝備制備一系列的磷脂脂質(zhì)體。壓力0.4 MPa下處理9次,得到平均粒徑為(39±7)nm、峰寬為(15±4)nm的脂質(zhì)體; 壓力0.2MPa下處理1次,得到平均粒徑(319±6)nm,峰寬為(83.2±13.4)nm的脂質(zhì)體。Saheki 等用高壓微射流設(shè)備制備蛋卵磷脂和豆油混合的脂質(zhì)納米分散體,在 處理壓力分別為108MPa和135MPa時,平均粒徑均小于100nm,分散穩(wěn)定性好。Chen等利用高壓微射流裝備在120MPa下,處理3次,制得粒徑為(157.7±2.31)nm 的輔酶Q10 納米脂質(zhì)載體,效果是普通乳劑的10倍以上。
3.2 納米混懸液
納米混懸液是指用少量表面活性劑為穩(wěn)定劑將難溶性固體純藥物以微粒狀態(tài)分散于分散介質(zhì)中形成的非均相膠體分散體系的液體制劑。與普通混懸劑相比,通常藥用納米混懸劑的平均粒徑一般低于1000nm。納米混懸劑屬于熱力學(xué) 不穩(wěn)定而動力學(xué)穩(wěn)定的粗分散體系,所以溶劑大多數(shù)為水,其穩(wěn)定性的關(guān)鍵也在于表面活性劑,但制備納米乳的藥物要具有較大的脂溶性,納米混懸劑則適用于大多數(shù)藥物。納米混懸劑制備的主要方法有研磨法、乳化法、蒸發(fā)沉降法、超臨界流體法等,操作簡單,工藝重現(xiàn)性好,易于工業(yè)化生產(chǎn)均采用高壓微射流法。
Pardeike等利用高壓微射流裝備制備以吐溫-80為潤濕劑的不同質(zhì)量濃度的磷脂酶A2抑制劑PX-18。所得的PX-18的平均粒徑均小于1000nm,增加了藥物溶解度,重現(xiàn)性好,提高藥物的生物利用度,可用于靜脈注射。周紅玲等利用微射流均質(zhì)設(shè)備在90MPa壓力下處理3次制備絲裂霉素納米混懸劑,經(jīng)過超速離心機高速離心2h,得到絲裂霉素C-聚氰基丙烯酸丁酯納米粒,測得平均粒徑為113. 5 nm,包封率和載藥量分別為( 85.1 ± 3.8) % 和( 7. 0 ± 0.2) % 。Liu 等利用沉淀-超聲法和沉 淀-微流化法兩種方法制備聯(lián)苯雙酯納米混懸液,并 對其體外表征進行研究。在壓力為23300psi下,處理10次,得到最佳的納米混懸液。Mschwitzer等利用高壓微射流裝備在1500bar下循環(huán)處理40次制備胃酸分泌抑制劑奧美拉唑納米混懸劑,在0 ℃下儲存1個月仍具有良好的穩(wěn)定性。
利用高壓微射流法與其他方結(jié)合可以得到分散 穩(wěn)定性好的納米混懸液。Zhao等采用沉淀-高壓微射流法結(jié)合法制備抗腫瘤藥物羥喜樹堿納米混懸液,在壓力為9000psi下處理5次,然后在壓力為18000psi下處理10次,得到平均粒徑為(286.9±6.1)nm,ζ電位為(-32.21±0.92)mV的納米混懸液,大大增強了其抗腫瘤效果。胡婷婷等將高壓微射流法與噴霧干燥法結(jié)合制得布地奈德多孔微球,在100MPa和循環(huán)60次的最佳條件制得平均粒徑為0.64μm、峰寬為0.44 的布地奈德顆粒,經(jīng)噴霧干燥后制得平均粒徑為2.90μm和比表面積為8.71m2·g-1的多孔微球。
4 結(jié)論與展望
高壓微射流技術(shù)是集物理、化學(xué)、工程學(xué)、微技術(shù)和生物技術(shù)于一體的多學(xué)科交叉的新興技術(shù)。該技術(shù)可以與噴霧干燥法、薄膜分散法、乳化法、蒸發(fā) 沉淀法等技術(shù)聯(lián)合使用,能制備粒徑小且粒度分布窄而均勻的藥物粒子。一般來說,隨著處理壓力增強,處理次數(shù)增多,粒徑減小,分散穩(wěn)定性增強。由于高壓微射流裝備使用簡單、工藝重現(xiàn)性好,許多制藥公司及其研發(fā)機構(gòu)已經(jīng)對其產(chǎn)生濃厚興趣,對未來臨床藥物上市產(chǎn)品具有很大的應(yīng)用前景。利用高 壓微射流法制備化學(xué)小分子藥物居多,在生物大分子及其中藥領(lǐng)域的研究將備受期待。

來源:藥物遞送


