您當前的位置:檢測資訊 > 科研開發(fā)
嘉峪檢測網(wǎng) 2019-06-04 16:26
導讀
本文詳細介紹了仿制藥注射劑穩(wěn)定性試驗方案的設(shè)計依據(jù),試驗樣品、放樣方案、記錄模板,數(shù)據(jù)評價等細節(jié)。
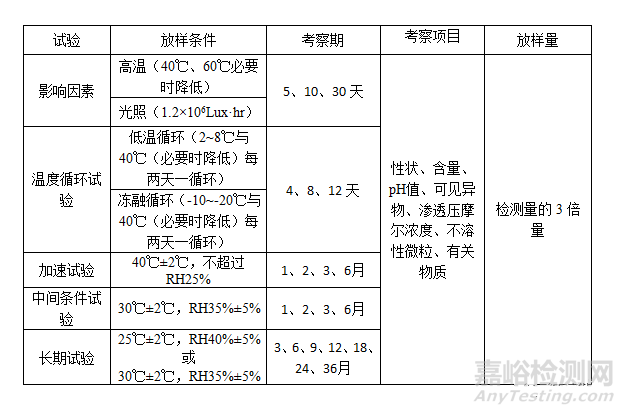
參照“原料藥物與制劑穩(wěn)定性試驗指導原則”(中國藥典2015年版四部通則9001)、“化學藥物(原料藥和制劑)穩(wěn)定性研究技術(shù)指導原則”(國家食品藥品監(jiān)督管理局藥品審評中心頒布)、“新原料藥和制劑的穩(wěn)定性試驗”(ICH Q1),注射劑穩(wěn)定性研究內(nèi)容包括影響因素試驗、加速試驗和長期試驗,必要時應進行中間條件試驗考察;對低溫下可能不穩(wěn)定的注射劑建議進行溫度循環(huán)試驗(低溫試驗和凍融試驗);對于包裝在半透性容器中的注射劑建議進行失水率試驗。
1、試驗樣品
采用1批中試樣品和1批原研制劑進行影響因素考察,采用3批中試樣品和1批原研制劑進行了加速試驗(中間條件試驗)和長期試驗考察,對低溫下可能不穩(wěn)定的采用1批中試樣品進行低溫試驗和凍融試驗,對于包裝在半透性容器中的采用3批中試樣品進行失水率試驗。
試驗用樣品基本信息表如下:
試驗用樣品基本信息
2、穩(wěn)定性考察項目
0天:性狀、裝量、裝量差異、含量、pH值、可見異物、滲透壓摩爾濃度、不溶性微粒、有關(guān)物質(zhì)、無菌、細菌內(nèi)毒素(或熱原)
3、穩(wěn)定性放樣方案
a.包裝在非滲透容器中的制劑
注:長期6月、12月、24月應檢查無菌、細菌內(nèi)毒素(或熱原)
b. 包裝在半滲透容器中的制劑
注:加速試驗和長期試驗應檢查失水率,長期6月、12月、24月應檢查無菌、細菌內(nèi)毒素(或熱原)
c.擬冷藏的制劑
注:長期6月、12月、24月應檢查無菌、細菌內(nèi)毒素(或熱原)
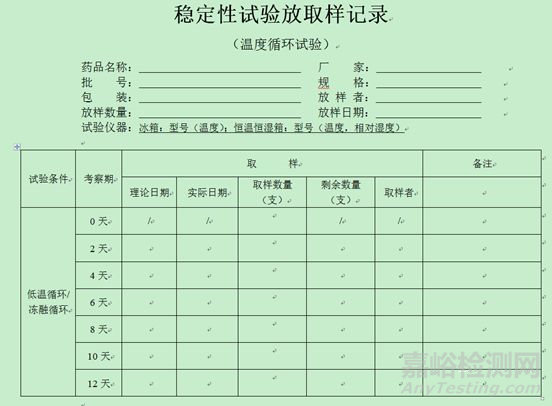
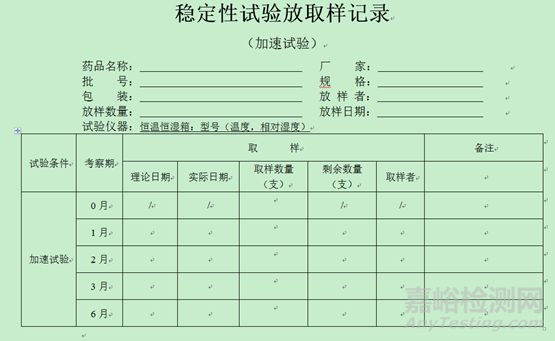
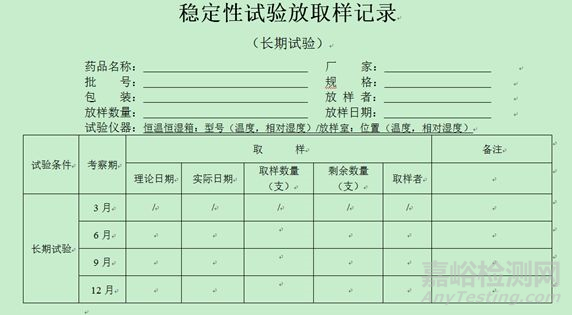
4、穩(wěn)定性放取樣記錄模板(僅供參考,考慮品種情況自定)
5、穩(wěn)定性數(shù)據(jù)評價
原研制劑最好另外檢測一批近效期末的進行檢測,與中試樣品試驗結(jié)果對比,證明中試樣品在加速試驗條件或者影響因素試驗條件下優(yōu)于原研近效期末的樣品。
穩(wěn)定性研究的目的是根據(jù)至少三批制劑及一批原研的測定對比結(jié)果,確定將來所有在相似條件下生產(chǎn)和包裝的制劑的貨架期和標簽上的貯藏條件。批次間變異的程度有可能產(chǎn)生產(chǎn)品質(zhì)量的差異,但產(chǎn)品在貨架期內(nèi)應符合質(zhì)量標準的要求。
任何評價不僅要考慮含量,還要考慮降解產(chǎn)物和其他有關(guān)的性能指標。如有必要,應注意考察質(zhì)量平衡情況和不同的穩(wěn)定性及降解特性。仿制藥的穩(wěn)定性應不低于原研參比制劑。





來源:藥事縱橫


