您當(dāng)前的位置:檢測(cè)資訊 > 科研開(kāi)發(fā)
嘉峪檢測(cè)網(wǎng) 2025-08-09 16:06
本技術(shù)報(bào)告(Technical Report,TR)旨在為制藥工藝驗(yàn)證(PV)生命周期方法的實(shí)施提供實(shí)用指南。它包含的信息能夠使生產(chǎn)廠家實(shí)施全球認(rèn)可的工藝驗(yàn)證程序,該程序與最近的基于生命周期的工藝驗(yàn)證指導(dǎo)文件和現(xiàn)行對(duì)藥品質(zhì)量系統(tǒng)期望相一致。在醫(yī)藥生產(chǎn)中,“工藝驗(yàn)證”是收集和評(píng)價(jià)工藝設(shè)計(jì)階段的數(shù)據(jù),通過(guò)商業(yè)化生產(chǎn)的方式確定科學(xué)的證據(jù),證明一個(gè)工藝能夠持續(xù)地提供高質(zhì)量的產(chǎn)品。美國(guó) FDA 和歐洲藥監(jiān)局認(rèn)定 PV 在現(xiàn)行 GMP 指南的綜述和具體條框中都是必要條件和藥品質(zhì)量保證的必需元素。
工藝驗(yàn)證生命周期概念連接產(chǎn)品和工藝開(kāi)發(fā)、商業(yè)化生產(chǎn)確認(rèn)和協(xié)同努力下商業(yè)化生產(chǎn)過(guò)程的維持。當(dāng)基于良好的工藝?yán)斫夂褪褂觅|(zhì)量風(fēng)險(xiǎn)管理時(shí),生命周期法可考慮生產(chǎn)者在使用傳統(tǒng)的工藝驗(yàn)證外,再使用連續(xù)工藝確證(增強(qiáng)的方式),或者直接由后者代替前者。
在本技術(shù)報(bào)告中應(yīng)用于藥物和藥品生產(chǎn)過(guò)程的信息,包括:
無(wú)菌和非無(wú)菌藥物
生物技術(shù)/生物產(chǎn)品,包含疫苗
原料藥(APIs)
放射性藥物
獸藥
組合產(chǎn)品的藥物成分(如,復(fù)方抗菌藥和醫(yī)療器械)
這份報(bào)告是為全球使用和應(yīng)用到新的和現(xiàn)有的(即遺留的)商業(yè)生產(chǎn)過(guò)程做準(zhǔn)備。它的范圍不包括:
生產(chǎn)的生產(chǎn)過(guò)程如下:醫(yī)療器械,膳食補(bǔ)充劑,藥用物料,人體組織。
盡管這些產(chǎn)品分類(lèi)超出了這份 TR 的范圍,但它的建議是基于現(xiàn)代質(zhì)量思想的/ICH質(zhì)量指南和最近的監(jiān)管機(jī)構(gòu)權(quán)威指導(dǎo)性文件。因此,它可能在其他產(chǎn)品類(lèi)別的工藝驗(yàn)證生命周期法的開(kāi)發(fā)中是有用的參考文獻(xiàn)。藥物生產(chǎn)過(guò)程中的輔助操作的驗(yàn)證在這個(gè)報(bào)告中不做討論。一些 FDA 的技術(shù)報(bào)告已經(jīng)提供了此類(lèi)操作規(guī)程的具體指導(dǎo)性文件;如:清潔、無(wú)菌過(guò)程模擬、濕熱滅菌和干熱滅菌。
5. 持續(xù)工藝確證(第三階段)
5.1建立監(jiān)控程序
5.1.1 目的和策略
持續(xù)工藝確證(CPV)程序提供了確保工藝成功確認(rèn)后保持受控狀態(tài)的一種方法。階段 1 和階段 2收集的信息和數(shù)據(jù)為建立后續(xù)日常生產(chǎn)有效控制策略和有價(jià)值的 CPV 程序做好了準(zhǔn)備。對(duì)前階段建立的工藝輸入和相應(yīng)輸出關(guān)系的理解,是 CPV 程序的成功基礎(chǔ)。
對(duì)工藝變量的持續(xù)控制使對(duì) CPV 計(jì)劃中的輸入進(jìn)行調(diào)整成為可能。這可以補(bǔ)償工藝變化,保證輸出穩(wěn)定。因?yàn)椴皇撬械淖兓瘉?lái)源都能在階段 1 和階段 2 預(yù)計(jì)和確定,持續(xù)工藝監(jiān)控發(fā)現(xiàn)的不可預(yù)期事件或趨勢(shì)可能提示工藝控制問(wèn)題和/或工藝改進(jìn)機(jī)會(huì)。在工藝開(kāi)發(fā)階段,以及產(chǎn)品生命周期的后續(xù)知識(shí)管理階段,采用科學(xué)和基于風(fēng)險(xiǎn)的工具有助于加強(qiáng)對(duì)工藝的理解,促進(jìn)持續(xù)控制的實(shí)施(見(jiàn) 3.0和 4.0 節(jié))。
5.1.2 持續(xù)工藝確證計(jì)劃制訂
設(shè)計(jì)持續(xù)工藝確證開(kāi)始于建立商業(yè)規(guī)模的控制策略(階段 1)。
高級(jí)別的質(zhì)量方針/文件概述了不同部門(mén)如何協(xié)作,如何起草、審核文件,保證處于已驗(yàn)證狀態(tài)。在質(zhì)量方針以及工藝驗(yàn)證主計(jì)劃之下,特定產(chǎn)品的持續(xù)確證計(jì)劃應(yīng)包括以下要素:
l不同職能部門(mén)的作用和職責(zé)
l取樣和測(cè)試策略
l數(shù)據(jù)分析方法(例如過(guò)程控制統(tǒng)計(jì)方法)
l可接受標(biāo)準(zhǔn)(適當(dāng)時(shí))
lOOT 和 OOS 結(jié)果處理策略
l決定何種工藝變更/趨勢(shì)需返回階段 1 和/或階段 2 的機(jī)制
l持續(xù)工藝確證測(cè)試計(jì)劃再評(píng)價(jià)時(shí)限
圖 5.1.2-1 舉例說(shuō)明了產(chǎn)品生命周期中持續(xù)工藝確證控制策略形成。理想情況下,控制策略的大部分在階段 2 (工藝性能確認(rèn))前建立,當(dāng)持續(xù)工藝確證概念應(yīng)用于老產(chǎn)品時(shí),應(yīng)采用同樣的方法形成、執(zhí)行持續(xù)確證計(jì)劃(見(jiàn) 5.1.3,老產(chǎn)品的持續(xù)工藝確證)因?yàn)殡A段 3 是生命周期驗(yàn)證方法(5.1.2-2)的一部分,持續(xù)工藝確證應(yīng)符合驗(yàn)證質(zhì)量體系和工藝驗(yàn)證主計(jì)劃的要求。除了工藝確認(rèn)(階段 2),工藝驗(yàn)證主計(jì)劃至少應(yīng)涵蓋工藝設(shè)計(jì)(階段 1)和持續(xù)工藝確證(階段 3)。
持續(xù)工藝確證取樣/測(cè)試策略的具體內(nèi)容直到完成工藝性能確認(rèn)才最終確定。因此,工藝驗(yàn)證主計(jì)劃可包括持續(xù)工藝確證策略的一般要求,并進(jìn)一步在工藝驗(yàn)證主計(jì)劃中提及的單個(gè)持續(xù)工藝確證計(jì)劃中明確。如果 CPV 活動(dòng)按照確定的 CPV 計(jì)劃啟動(dòng),也可認(rèn)為工藝驗(yàn)證主計(jì)劃在階段 2 后期結(jié)束(就是說(shuō)不得在整個(gè)產(chǎn)品生命周期中始終處于開(kāi)放狀態(tài))
Figure 5.1.2-1 CPV(持續(xù)確證)計(jì)劃的制訂
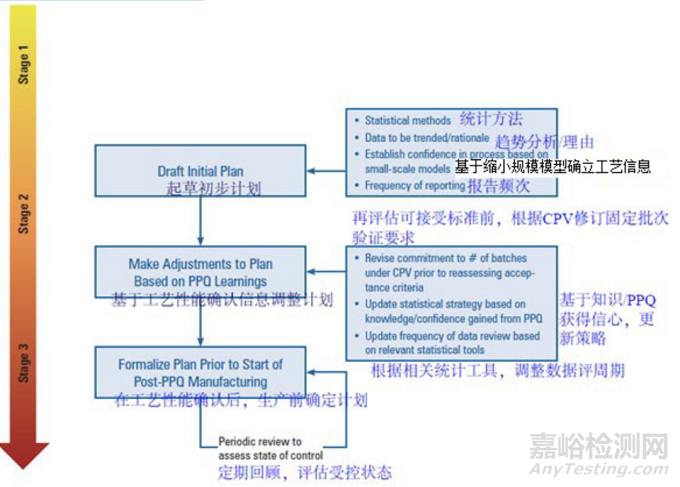
Figure 5.1.2-2 驗(yàn)證文件體系下的 CPV(持續(xù)工藝確證)計(jì)劃
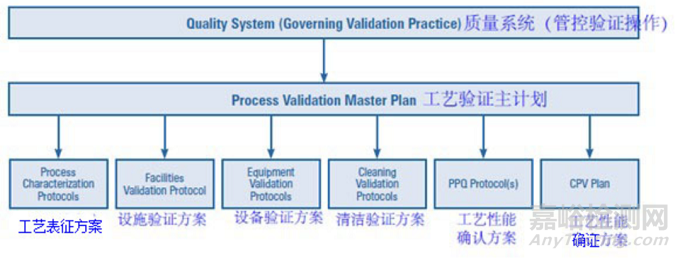
5.1.3 老產(chǎn)品的持續(xù)工藝確證
圖 5.1.3-1 概述了老產(chǎn)品應(yīng)用生命周期概念時(shí),評(píng)估所需完成活動(dòng)的一種方法。老產(chǎn)品通常有完善的監(jiān)控,不需要采取太多行動(dòng)。然而,應(yīng)基于對(duì)歷史工藝和監(jiān)控大量數(shù)據(jù)以及工藝變化的評(píng)估做出決定。采用該方法時(shí),應(yīng)該用歷史數(shù)據(jù)評(píng)價(jià)工藝控制的現(xiàn)狀。評(píng)價(jià)工藝時(shí),應(yīng)考慮采用過(guò)程能力和其他統(tǒng)計(jì)學(xué)方法。除了評(píng)價(jià)過(guò)程能力外,也應(yīng)評(píng)估用于工藝監(jiān)控的參數(shù)充分性。對(duì)現(xiàn)有工藝控制策略適宜性評(píng)估,可以作為決定老產(chǎn)品持續(xù)工藝確證中是否需要其他額外取樣/監(jiān)控的基礎(chǔ)。應(yīng)考慮進(jìn)行一段時(shí)間的加強(qiáng)取樣,以獲得大量變量評(píng)估數(shù)據(jù),作為設(shè)定日常取樣和監(jiān)控水平和頻次的基礎(chǔ)。建議將持續(xù)監(jiān)控寫(xiě)入 5.1.2 節(jié)“持續(xù)工藝確證計(jì)劃制訂”中正式計(jì)劃中。
判斷老產(chǎn)品的取樣計(jì)劃是否充分時(shí),可采用統(tǒng)計(jì)學(xué)的方法。然而,根據(jù)數(shù)據(jù)的數(shù)量和類(lèi)別不同,也許沒(méi)有必要對(duì)取樣計(jì)劃進(jìn)行統(tǒng)計(jì)評(píng)價(jià)。該決定應(yīng)作為對(duì)歷史數(shù)據(jù)和監(jiān)控方法進(jìn)行初步評(píng)估的一部分。盡管也許不需要統(tǒng)計(jì)模型,取樣計(jì)劃應(yīng)科學(xué)合理,并能代表所取的工藝和每批產(chǎn)品。
Figure 5.1.3-1 老產(chǎn)品 CPV 計(jì)劃的制訂
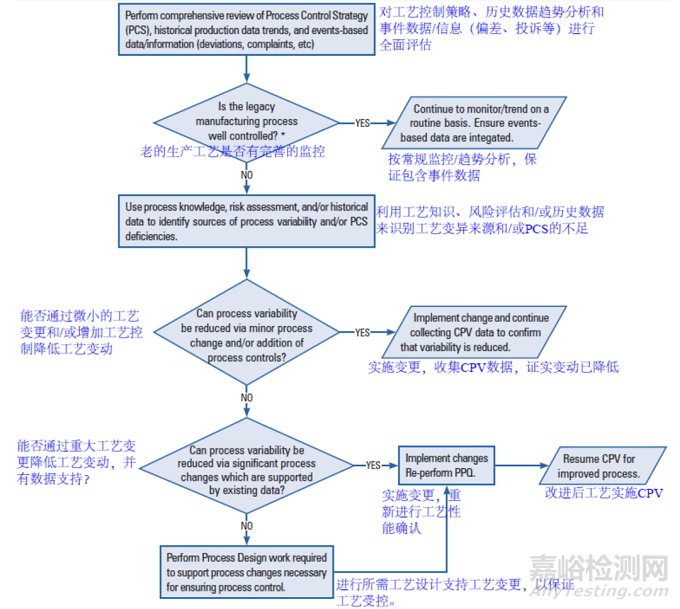
是否確定了適當(dāng)?shù)墓に嚳刂撇呗裕軌蜃C明理解了工藝參數(shù)對(duì)于關(guān)鍵質(zhì)量特性的影響),統(tǒng)計(jì)數(shù)據(jù)是否顯示變化處于受控之中。
5.1.4持續(xù)工藝確證的證實(shí)
CPV 計(jì)劃中數(shù)據(jù)的兩個(gè)基本來(lái)源為:
1. 工藝參數(shù)(即工藝性能和產(chǎn)品質(zhì)量指標(biāo))
2. 可變性潛在來(lái)源為沒(méi)有確定的工藝參數(shù)。例如:
a.原輔料質(zhì)量
b. 冗余的設(shè)備儀表可比性
c.人員對(duì)工藝的影響(如班次之間一致性)
與工藝性能和產(chǎn)品質(zhì)量特性相關(guān)的關(guān)鍵輸入?yún)?shù)和相應(yīng)輸出在工藝設(shè)計(jì)中(階段 1)確定(見(jiàn)圖 1.1-2)。
商業(yè)生產(chǎn)時(shí),生產(chǎn)工藝確認(rèn)(階段 2)批,以證實(shí)工藝運(yùn)行符合預(yù)期要求,并證實(shí)工藝控制策略可穩(wěn)定地生產(chǎn)符合預(yù)定質(zhì)量特性的產(chǎn)品。工藝控制策略也應(yīng)作為出發(fā)點(diǎn),識(shí)別 CPV 計(jì)劃中應(yīng)包含的工藝數(shù)據(jù)/信息。
5.1.5 CPV監(jiān)控計(jì)劃
常規(guī)取樣將獲得部分?jǐn)?shù)據(jù)并用于 CPV 計(jì)劃,但也應(yīng)考慮非常規(guī)取樣。取樣/測(cè)試計(jì)劃應(yīng)動(dòng)態(tài)地由階段 2 前進(jìn)到階段 3;并應(yīng)定期更新和審核。一個(gè)增強(qiáng)的取樣計(jì)劃(可同時(shí)包括在線和離線分析)可保證收集到適當(dāng)?shù)臄?shù)據(jù)。因?yàn)楣に囆阅艽_認(rèn)方案已指明那些必須保持在一定范圍的工藝參數(shù)和質(zhì)量特性(輸入和輸出),以使產(chǎn)品符合預(yù)定質(zhì)量特性,工藝性能確認(rèn)取樣計(jì)劃是 CPV 取樣計(jì)劃的邏輯基礎(chǔ)。工藝性能確認(rèn)可提供充分保證,大生產(chǎn)時(shí)部分參數(shù)良好受控,不需要納入 CPV 計(jì)劃中。
例如,生物工藝要求充分清除工藝殘留(例如消泡劑)或工藝相關(guān)雜質(zhì)(例如 DNA)。這可在工藝性能確認(rèn)批中得到證實(shí),不需要在 CPV 時(shí)繼續(xù)取樣和測(cè)試。當(dāng)歷史數(shù)據(jù)有限或數(shù)據(jù)顯示較大變動(dòng)時(shí),階段2 后應(yīng)繼續(xù)進(jìn)行取樣和趨勢(shì)分析,以充分保證某一特定雜質(zhì)受到控制。這應(yīng)根據(jù)具體情況通過(guò)對(duì)歷史數(shù)據(jù)的風(fēng)險(xiǎn)評(píng)估和/或統(tǒng)計(jì)分析做出決定。
預(yù)期的 CPV 計(jì)劃應(yīng)提供具體說(shuō)明,部分分析只進(jìn)行到一定程度,一旦收集到足夠數(shù)據(jù)確定工藝受控,便可終止。取樣批次和一批內(nèi)取樣頻次應(yīng)在階段 3 的增強(qiáng)取樣計(jì)劃中說(shuō)明。根據(jù)產(chǎn)生的數(shù)據(jù),用于參考目的的取樣和分析應(yīng)有指定的終點(diǎn)。一個(gè)更開(kāi)放的方法,不指明具體批次,可用于數(shù)據(jù)趨勢(shì)分析和結(jié)果討論。另一種選擇是根據(jù)趨勢(shì)分析和結(jié)果降低或增加取樣以及測(cè)試。
5.1.6 數(shù)據(jù)分析和趨勢(shì)分析
CPV 計(jì)劃應(yīng)清楚說(shuō)明收集的數(shù)據(jù)如何進(jìn)行分析。在部分情況下,可與預(yù)定的可接受標(biāo)準(zhǔn)比較,特別對(duì)于嚴(yán)格受控的數(shù)據(jù)(例如柱色譜的一個(gè)梯度洗脫曲線斜率)。另一種情況(如工序收率)是,可進(jìn)行數(shù)據(jù)的統(tǒng)計(jì)分析,評(píng)估工藝趨勢(shì),此時(shí)應(yīng)在 CPV 計(jì)劃中指定持續(xù)工藝控制的統(tǒng)計(jì)方法和規(guī)則。通常用控制圖評(píng)估一段時(shí)間后工藝控制情況,其適用于評(píng)價(jià)統(tǒng)計(jì)過(guò)程控制,以及發(fā)現(xiàn)工藝趨勢(shì)。根據(jù)CPV 要求,控制圖以批為基礎(chǔ)建立和評(píng)估(見(jiàn) 6.2 節(jié)統(tǒng)計(jì)分析工具和附錄 8.1 確定統(tǒng)計(jì)數(shù)據(jù)分析所需批次的統(tǒng)計(jì)方法)。
應(yīng)建立前瞻性標(biāo)準(zhǔn)保證工藝處于受控狀態(tài)。不管公司如何定義它,一個(gè)超出控制范圍的結(jié)果(如趨勢(shì)超標(biāo)、超出控制限、檢驗(yàn)結(jié)果超標(biāo)、超出行動(dòng)限)將觸發(fā)根據(jù)質(zhì)量體系采取行動(dòng)(如調(diào)查、對(duì)驗(yàn)證狀態(tài)的影響分析)。采取的行動(dòng)隨具體情況不同而不同,但應(yīng)在 CPV 計(jì)劃中說(shuō)明何種行動(dòng)。 6.0 節(jié)“用于工藝驗(yàn)證生命周期的工具“,描述了用于趨勢(shì)統(tǒng)計(jì)分析和統(tǒng)計(jì)過(guò)程控制的工具,應(yīng)結(jié)合風(fēng)險(xiǎn)評(píng)估使用這些工具。
5.1.4 節(jié)涵蓋了非參數(shù)相關(guān)(原料、人員和環(huán)境)的工藝變化來(lái)源。作為整個(gè) CPV 評(píng)估的一部分,應(yīng)降低高風(fēng)險(xiǎn)變化來(lái)源的風(fēng)險(xiǎn),并評(píng)估是否已處于可控范圍。例如對(duì)關(guān)鍵原料的純度進(jìn)行趨勢(shì)分析,可能看出不同供應(yīng)商的微小差別。即使表面看是個(gè)供應(yīng)商的微小的變更,可能導(dǎo)致趨勢(shì)超標(biāo)或檢驗(yàn)結(jié)果超標(biāo)。應(yīng)從整個(gè)工藝一致性和產(chǎn)品質(zhì)量角度對(duì)此進(jìn)行評(píng)價(jià)。
5.2 CPV 監(jiān)控結(jié)果的整合
5.2.1 質(zhì)量體系和持續(xù)工藝確證
對(duì)工藝控制進(jìn)行持續(xù)確認(rèn)和細(xì)化的最好工具是能夠提供反饋并客觀評(píng)價(jià)工藝控制的質(zhì)量體系元素。
這些工具是基于對(duì)產(chǎn)品和工藝的理解,并通過(guò)監(jiān)視、測(cè)量、分析和控制工藝性能的程序?qū)崿F(xiàn)。
一旦處于商業(yè)生產(chǎn)中,除了 5.1 節(jié)所述的工藝趨勢(shì)分析外,對(duì)已驗(yàn)證狀態(tài)的維護(hù)還需要一個(gè)基于事件的審核系統(tǒng),并建立一個(gè)控制計(jì)劃。生產(chǎn)、質(zhì)量以及監(jiān)管部門(mén)就審核結(jié)果進(jìn)行溝通,修訂控制策略(為了提高和/或法規(guī)符合),是 CPV 的一個(gè)重復(fù)和基本部分。反饋機(jī)制可以是立即的(批內(nèi)或及時(shí))、每批后或一系列批次后或一段時(shí)間后。CPV 計(jì)劃應(yīng)說(shuō)明各種反饋機(jī)制應(yīng)在何時(shí)采取。
圖 5.2.1-1 描述了用于持續(xù)改進(jìn)生產(chǎn)工藝的數(shù)據(jù)來(lái)源。盡管不是詳盡的清單,該圖展示了與生產(chǎn)和工藝性能相關(guān)的數(shù)據(jù)的典型分類(lèi)。
Figure 5.2.1-1 知識(shí)構(gòu)成和工藝控制的維護(hù)
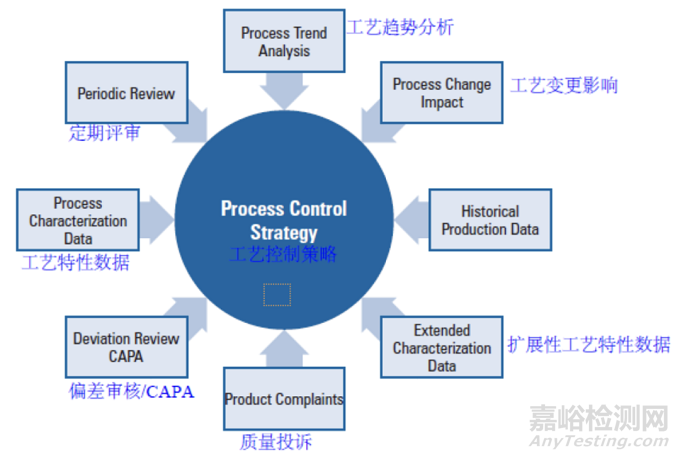
5.3 持續(xù)工藝確證數(shù)據(jù)審核、報(bào)告
CPV 計(jì)劃需要包括數(shù)據(jù)收集機(jī)制和質(zhì)量體系所獲得信息進(jìn)行審核的頻次,也應(yīng)指明哪些情況下需立即對(duì)工藝或產(chǎn)品的一些重大問(wèn)題進(jìn)行評(píng)審,以及評(píng)審程序、參與評(píng)審的人員。按照 ICH Q10,該評(píng)審必須包括高層管理人員。他們是維護(hù)一個(gè)有效藥品質(zhì)量體系,并持續(xù)改進(jìn)的關(guān)鍵人員。
數(shù)據(jù)審核頻次主要取決于風(fēng)險(xiǎn)大小。不同工藝和工序的評(píng)審周期因風(fēng)險(xiǎn)的水平和控制的復(fù)雜程度而不同。應(yīng)采用最新的工藝風(fēng)險(xiǎn)溝通文件,確定評(píng)審周期。隨著生產(chǎn)數(shù)據(jù)的產(chǎn)生,對(duì)于工藝的進(jìn)一步理解,對(duì)工藝有更好的控制,可降低評(píng)審的周期或強(qiáng)度。
將年度商業(yè)生產(chǎn)數(shù)據(jù)匯總起草年度產(chǎn)品質(zhì)量回顧也許是足夠的。但更頻繁的數(shù)據(jù)審核,并與確定的可接受標(biāo)準(zhǔn)比較可幫助生產(chǎn)商更具有前瞻性和減少波動(dòng)。根據(jù)法規(guī)要求,年度產(chǎn)品質(zhì)量回顧是必須的,但年度回顧可能變成對(duì)多重、更頻繁的 CPV 數(shù)據(jù)評(píng)審進(jìn)行的更高一級(jí)別的評(píng)審和匯總。年度產(chǎn)品質(zhì)量回顧可識(shí)別 CPV 數(shù)據(jù)評(píng)審中發(fā)現(xiàn)的問(wèn)題,匯總長(zhǎng)期趨勢(shì),但生產(chǎn)商應(yīng)在規(guī)定時(shí)間間隔內(nèi)進(jìn)行更頻繁的 CPV 數(shù)據(jù)評(píng)審。
注:FDA 21 CFR 211.180(e)要求至少每年進(jìn)行一個(gè)評(píng)估。審核頻次由生產(chǎn)商確定,但應(yīng)至少每年進(jìn)行一次。

來(lái)源:文亮頻道


