方法轉移包括一系列步驟,從計劃開始,到報告結束,其步驟如下:
1、轉移計劃
分析方法轉移可能發(fā)生在研發(fā)過程中的任何階段,比如工藝放大、注冊批生產、批準后生產工藝變更。產品研發(fā)的一個重要里程碑是將注冊批次的生產工藝和檢驗方法轉移到擬定的商業(yè)生產地址,因此應完善生產工藝和檢驗方法,使擬定商業(yè)生產地址能夠獲得生產工藝和檢驗方法的經驗。
在方法轉移前,應成立轉移小組,成員包括雙方經理、QC和QA。小組章程、組成和時間安排應相互溝通并記錄在分析方法轉移計劃中。
2、方法轉移包
轉移實驗室提供信息包作為分析方法轉移的第一步。在分析方法轉移包中協(xié)商并記錄擬轉移的方法、時間點和轉移方式(驗證、對比試驗、共同驗證);提供方法的所有知識文件,主要包括分析操作規(guī)程、質量標準、驗證報告(符合法規(guī)要求)、有代表性的數(shù)據(jù)(如典型色譜圖)、分析方法開發(fā)報告、風險評估以及耐用性試驗結果;另外還應詳細描述影響分析方法轉移的關鍵因素如實驗室環(huán)境、樣品前處理、儀器設備等。
3、儀器設備
應對轉移方和接收方的儀器設備進行評估。供應商和儀器型號的差異可能會對分析方法的性能產生重大影響。轉移方使用的儀器配置應與接收方進行溝通,方法中使用的任何一個附加設備都應詳細說明。
4、檢測用樣品
選擇的樣品應具有代表性,如過期、老化、加標的樣品可能不具有代表性。應評估所選樣品異常結果對臨床供應的潛在影響。通常不建議對多個樣品批次進行檢測,因為在評估中會增加樣品方差作為一個因素,從而混淆了評估結果。
5、接受標準
理想情況下,接受標準應與方法驗證報告一致,然而一般情況下標準設置的比較寬,從而容易達到要求。通常以驗證結果和轉移前可行性研究作為指導,制定合適的、有意義的接受標準。
6、熟悉方法
在分析方法轉移前,應進行實驗室實驗(即可行性研究),這些可行性研究應足夠深入(可發(fā)現(xiàn)導致方法轉移失敗的問題),使接收方能順利地完成方法轉移。可行性研究不作為正式研究的一部分,在預試驗中產生不可接受的實驗結果需在轉移之前采取措施,比如進行培訓、方法評估、修改方案等。
7、轉移方案
轉移方案應詳細地描述分析方法、所用的試劑、儀器設備、樣品批次、對照品信息、待評估的方法參數(shù)以及可接受標準等。轉移方案由轉移方或接收方起草,雙方負責審核批準。
8、轉移報告
方法轉移的最后一步是完成轉移報告。一般來說,轉移方完成轉移報告的編寫,雙方根據(jù)事先商定的格式提供結果(雙方數(shù)據(jù)均應進行同行評審),并與接受標準對比,以完成方法轉移。
分析方法轉移的方式如下:
A、對比試驗 對比試驗是讓轉移方和接收方在合理的、較短時間內完成一批樣品的檢測,然后根據(jù)方案中規(guī)定的接受標準對每個實驗室的結果進行比較和評估。某些情況下,可以將接收方數(shù)據(jù)與轉移方生產的COA進行比對,前提是COA是在與接收實驗室生成的數(shù)據(jù)相關的合理時間內生成的。
B、共驗證 大多數(shù)情況下,轉移方實驗室對于方法的驗證優(yōu)先于接收方實驗室,因此,共同驗證不是一個好選擇。但是,分析方法從公司的研發(fā)部門轉移到QC實驗室,采用這種方式是一個好的選擇。該方式的缺點是接收方結果不符合接受標準,將導致方法轉移失敗,避免這一潛在問題的關鍵是記錄中間精密度試驗,使得轉移實驗室能夠繼續(xù)生成可報告的數(shù)據(jù)。
C、完全驗證 接收方對方法進行全驗證是一種常用方法,這種方法雖然耗費時間和資源,但提供最高水平的保證,即接收實驗室可用該方法產生可接受的結果。這種方式常用于早期階段,或用于糾正或完成之前未按照法規(guī)要求執(zhí)行的驗證元素。
D、轉移豁免 采用這種方式要記錄并說明原因,如接收實驗室檢驗過類似樣品,并對檢驗步驟熟悉;熟悉該方法的分析員調到接收實驗室等。
在分析方法轉移前,還應進行風險評估,確定可能影響的因素,并對風險進行評級,確定消除風險的方法。以HPLC為例:
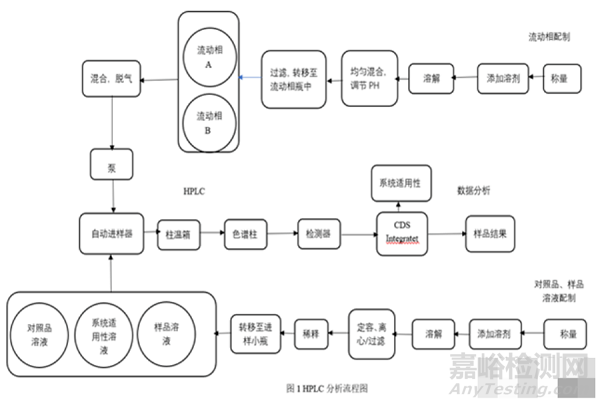
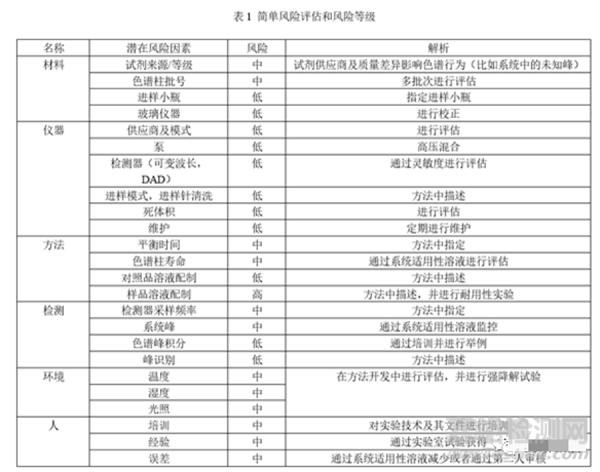
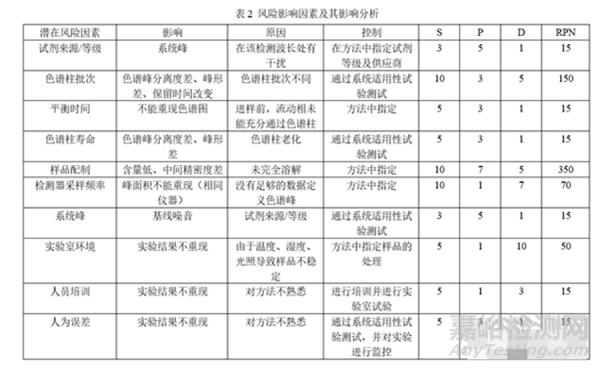
方法轉移中難免遇到許多問題,需要明確檢驗方法、關鍵風險因素、進行可行性研究及現(xiàn)場培訓,雙方及時溝通,解決問題,順利完成方法轉移。







