本文適用于制取醫用壓縮空氣,為醫療機構的集中供氣系統提供壓縮空氣源的醫用空氣壓縮機組。在《醫療器械分類目錄》的分類編碼為08-07-01。
一、醫用空氣壓縮機組結構組成和工作原理
1.結構組成
醫用空氣壓縮機組一般由空氣壓縮機、電控柜、后冷卻器、儲氣罐、空氣過濾器、空氣干燥器、連接管道、閥門、減壓裝置、儀表、露點和一氧化碳檢測裝置組成。
空氣壓縮機是壓縮空氣的氣壓發生裝置。
后冷卻器一般裝于壓縮機與儲氣罐之間,用于冷卻壓縮機出來的高溫空氣,析出水分。
儲氣罐用于壓縮空氣的儲存、緩沖、排污。
空氣過濾器通常包含多級壓縮空氣過濾器,用于分離壓縮空氣中的固體顆粒物、水分、油分以及氣態物質(如CO,CO2、SO2、NO、NO2等)和微生物。
空氣干燥器用于減少壓縮空氣中的水分含量,通常采用吸附式干燥器。
減壓裝置一般裝于末級壓縮空氣過濾器之后、集中供氣系統管道的進氣端前,用于調節輸送到供氣系統管道的壓縮空氣壓力。
露點檢測裝置和一氧化碳檢測裝置用于檢測機組供氣口的露點(含水量)和一氧化碳含量。
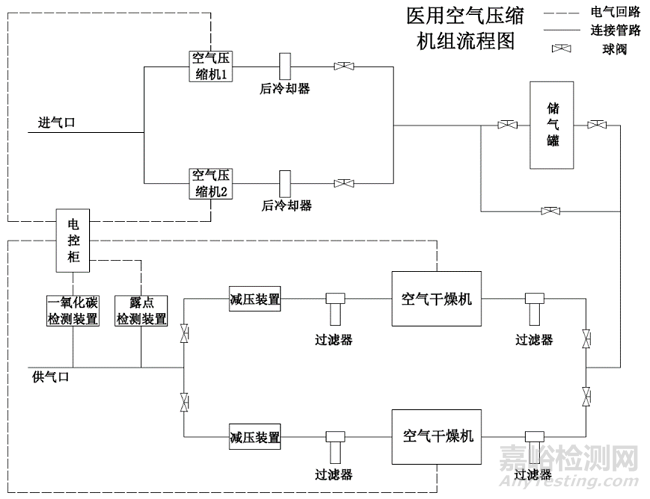
(2)壓縮壓縮空氣制備流程圖
圖1醫用壓縮空氣制備流程圖
注:上述示意圖僅供參考,具體產品結構組成和各組件配置情況應根據實際產品確定。
2.工作原理
外界空氣通過進氣裝置、進氣過濾器后經壓縮機壓縮變成高溫壓縮空氣,高溫壓縮空氣經冷卻后,再通過過濾裝置、干燥裝置等處理后,獲得空氣質量符合要求的壓縮空氣,壓縮空氣經減壓裝置調壓到規定值后輸送到集中供氣系統管道中。醫用空氣壓縮機組內部包括控制系統在內的所有元件、部件均有冗余,按照單一故障連續供氣的要求配置管道和閥門,每臺壓縮機采用獨立控制電路,保證醫用空氣壓縮機組在單一故障狀態下滿足連續供氣要求。
二、醫用空氣壓縮機組性能研究實驗要求
1.醫用空氣壓縮機組主要性能參數:
1.1外觀
1.2機組容積流量
1.3機組供氣壓力
1.4機組壓力試驗
1.5機組泄露性試驗
1.6在單一故障狀態時,應能連續供氣。
1.7機組控制功能
如獨立的電源開關及控制回路、斷電恢復后自動啟動、顯示運行狀態、壓縮機和控制系統故障后的自動切換等。
1.8 空氣質量
至少包括含油量、含水量(露點)、CO、CO2、NO和NO2、SO2含量、固體顆粒物等級、氣味。
1.9結構方面
進氣管、排氣管的連接;防倒流裝置;過濾器的級數和濾芯性能監測措施;儲氣罐的自動和手動排水;露點和一氧化碳檢測裝置。
1.10空氣干燥器的控制功能
1.11報警功能
1.11.1確定發生報警的種類,包括備用壓縮機啟動、傳感器回路斷路、供氣壓力超標、機組故障、露點溫度超標、一氧化碳濃度超標等。
1.11.2聲響報警和視覺報警,聲響報警有暫時靜音功能。
1.12機組噪聲
1.13電氣安全要求
應符合GB 9706.1《醫用電氣設備第1部分:基本安全和基本性能的通用要求》的要求。
1.14電磁兼容性要求
應符合YY 0505《醫用電氣設備第1-2部分:基本安全和基本性能的通用要求并列標準:電磁兼容要求和試驗》的要求。
2.產品性能研究
2.1應制定產品性能指標及試驗方法,明確所采用的標準或方法、采用的原因及理論基礎。
2.2應結合產品工作原理及適用范圍,確定產品結構組成或各主要元器件功能性指標并進行研究,例如機組工作流程的研究;過濾器級數、類型、精度和處理流量、濾芯性能監測措施等的研究;干燥器控制功能的研究。
2.3結合產品包含的元件、部件,進行機組單一故障狀態下可實現連續供氣的研究。
結合產品具備的控制和報警功能,開展機組的監控和報警功能驗證。
開展機組在高溫高濕環境下,空氣質量的性能研究;并結合驗證資料在說明書中對工作環境予以說明。
開展機組在不同使用流量下(至少包括高使用流量和低使用流量情況),空氣質量、壓力穩定性和泄漏量的性能研究。
結合壓縮機的排氣壓力范圍和機組供氣壓力,開展在不同壓力下空氣質量、壓力穩定性和泄漏量的性能研究。
結合正常運行時機組內各壓縮機輪流切換運行的控制措施,開展相關研究。
結合產品設計控制措施,以及機組在不同運行狀態下需要同時運行的機組數量,開展相關研究。
2.4若產品采用冷凍式干燥機,需開展壓縮空氣質量滿足GB 50751中表3.0.1要求的研究。
2.5若生產企業自己開展管道脫脂,開展清洗脫脂方法的驗證;若生產企業自己不脫脂,應確定清洗脫脂方法,且該方法應經過驗證。
2.6若產品可與器械驅動共用同一空氣壓縮機組,機組需同時滿足GB50751對醫用空氣和器械驅動空氣在空氣質量、供氣壓力及偏差的要求。應結合各部件參數、不同臨床使用流量(重點關注滿負荷、高使用流量)、機組供氣壓力等方面要求,開展空氣質量、壓力穩定性、機組供氣壓力等方面的研究。
3.滅菌/消毒工藝研究 (若適用)
終端用戶滅菌/消毒:應當明確消毒工藝(方法和參數)以及消毒方法確定的依據。
4.產品有效期和包裝研究
4.1有效期的確定:應依據《有源醫療器械使用期限注冊技術審查指導原則》要求,分析評價產品使用期限。
應根據自身產品臨床應用和產品設計情況,確定出產品的關鍵部件和可更換部件。應明確在預期使用條件下關鍵部件的使用期限,及可更換部件的定期保養維護時間和更換頻次,且應確定使用壽命和更換頻次的依據。
4.2包裝及包裝完整性:在有效期內以及運輸儲存條件下,保證包裝完整性。
5.環境試驗
應按照GB/T 14710的要求開展相關研究。
6.軟件研究
通常醫用空氣壓縮機組的軟件安全級別為B級,應按照《醫療器械軟件注冊技術審查指導原則》的要求確定軟件描述文檔。如產品具有網絡連接功能或采用存儲媒介的方式用以進行電子數據交換或遠程控制的,需要按照《醫療器械網絡安全注冊技術審查指導原則》的要求確定網絡安全描述文檔。
三、醫用空氣壓縮機組主要風險
依據YY/T 0316的附錄E(表1)從各方面提示性列舉了醫用空氣壓縮機組的可能存在的初始危害因素,可從以下方面考慮。
表1 產品主要初始危害因素
|
危險(源) |
可預見的事件序列 |
危險情況 |
傷害 |
|
電磁能 |
保護接地阻抗超過允許限值 |
電源故障時設備上會有電壓差,人員接觸會形成電流回路;機組可能帶電,通過管道傳導到氣體終端 |
觸電,嚴重時死亡 |
|
電磁輻射超過規定的要求,或抗電磁干擾不符合要求 |
不能在電磁環境中正常工作或對環境產生超過規定的干擾 |
自身受干擾或其它設備受干擾不能正常工作,控制程序紊亂 |
|
熱能 |
壓縮機本體、排氣管路及后冷卻器表面高溫 |
人員接觸高溫表面 |
燙傷 |
|
無潤滑壓縮機嚴重過熱 |
壓縮機壓縮腔內部涂層、填料、密封件由于嚴重過熱釋放出有毒氣體。 |
危害患者 |
|
機械能 |
運動零部件裸露無防護 |
人員接觸或靠近,肢體或衣物卷入 |
碰傷、肢體傷害 |
|
壓力 |
空壓機運行不正常(氣量不足)、系統漏氣、減壓裝置故障、管道系統堵塞,造成輸出壓力低于規定的值 |
輸出壓力不足,終端流量和壓力減小,可能造成空氧配比不符合要求 |
造成氧中毒或呼吸機工作不正常,危及患者的生命 |
|
減壓裝置故障、安全閥失效或堵塞,造成輸出壓力高于規定的值 |
超壓,超過管道耐壓范圍,或造成終端壓力過高 |
氣體壓力過高,可能導致管道破裂,器械(包括呼吸機)超壓保護停機,造成手術中斷,危及患者的生命 |
|
監測壓力的器具(壓力表、壓力報警器等)未按規定檢定或校準 |
壓力顯示偏離,造成醫用氣體機組欠壓或超壓 |
造成的危害如同上述的“氣體壓力低于規定值”或“氣體壓力高于規定值” |
|
生物學危害 |
管道脫脂清洗不完全 |
管道中的油脂混到壓縮空氣中,輸送到患者端 |
造成患者感染 |
|
過濾器濾芯、干燥器干燥劑性能失效,未及時更換 |
污染物超標 |
造成患者感染 |
|
壓縮機進氣口空氣質量低于規定要求或者受到污染 |
有害物質超標 |
造成患者感染 |
|
聲能 |
空氣壓縮機外殼固定件松動或防護罩破損,設備運行時振動 |
環境噪音大,聽覺報警錯失 |
不能及時發現故障,影響聽覺 |
|
使用操作 |
誤將醫療空氣用于驅動器械 |
氣體壓力太低,無法驅動器械正常工作 |
器械無法使用;驅動力不足,造成患者傷害 |
|
操作不當或錯誤 |
閥門操作錯誤、減壓裝置調整不當 |
造成的危害如同上述的“氣體壓力低于規定值”或“氣體壓力高于規定值” |
|
閥門操作錯誤造成供氣中斷 |
危及患者的生命 |
|
未按期巡查、維護、檢修 |
不能及時發現設備故障,可能造成供氣中斷、輸出壓力偏離,品質不符合要求 |
危及患者的生命或對終端的呼吸機造成損壞 |
|
壓縮空氣品質 |
水分含量超標 |
可能在管道系統積液態水,滋生細菌 |
造成患者呼吸系統感染,液態水可能造成設備故障,危及患者生命 |
|
油含量超標 |
污染管道系統,可能造成末端裝置損壞;油與氧氣混合時,有毒,易燃 |
造成患者呼吸系統感染,可能造成設備故障,危及患者生命。 |
|
雜質含量超標 |
化學雜質超標 |
化學雜質超標可能造成患者咳嗽、不適等,嚴重的可能造成中毒 |
|
顆粒物含量超標 |
患者吸入顆粒物; |
可能造成患者咳嗽、不適等,可能影響設備的正常運行,危及患者生命 |
|
顆粒物聚集在過濾器,或堵塞氣道,氣體壓力下降 |
|
使用說明書 |
使用說明操作、維保、注意事項不全或不明確 |
錯誤的操作或維保及維保不及時 |
人身傷害、設備損壞或供氣中斷 |