您當前的位置:檢測資訊 > 科研開發
嘉峪檢測網 2022-06-10 22:18
車前子是中醫常用的利尿通淋藥,《中國藥典》2020年版車前子項下含量測定要求檢測毛蕊花糖苷,且含量不低于0.4%[1]。研究表明車前子中毛蕊花糖苷會受溫度、加熱時間、pH等影響而發生變化[2-6]。谷彩梅等[2]分析了車前子鹽炙品與生品,發現炮制后的車前子中毛蕊花糖苷含量升高,同時鹽炙品中異毛蕊花糖苷含量變化顯著。田偉等[3]發現車前子中的毛蕊花糖苷和異毛蕊花糖苷含量隨煎煮時間、溫度、pH值的變化發生一定程度的變化,推測毛蕊花糖苷可能發生酯鍵斷裂生成咖啡酸,并部分轉化為異毛蕊花糖苷。本實驗以毛蕊花糖苷為研究對象,深入研究pH對毛蕊花糖苷穩定性的影響,明確其變化規律及可能的轉化機制。
毛蕊花糖苷是車前子中主要的苯乙醇苷類化合物,其化學結構見圖1,為連接咖啡酰基的苯乙醇二糖苷。現代藥理研究表明,毛蕊花糖苷具有神經保護作用,能修復阿爾茨海默病的受損神經元,改善學習和記憶功能[7-9];能通過抑制間質表皮轉化因子(c-mesenchymal epithelial transition factor,c-Met)的表達進而抑制膠質母細胞瘤細胞的增殖、遷移和侵襲起到殺死腫瘤的作用[10];此外毛蕊花糖苷還具有抗炎[11]、抗氧化[12]、抗病原微生物[13]等作用。毛蕊花糖苷在植物中廣泛存在,其毒性小、生物活性多樣,因而具有良好的開發和應用前景。但毛蕊花糖苷結構中存在多個酚羥基,易被氧化,化學穩定性較差,限制了它的臨床應用。為了進一步探索毛蕊花糖苷的降解特征和降解途徑,本研究采用高效液相色譜-紫外(HPLC-UV)和高分辨質譜(HPLC-IT-TOF-MS)技術分析了毛蕊花糖苷在不同pH溶液中加熱降解速率,并鑒定了降解產物,初步闡明了其降解規律。

1、材料與儀器
1.1儀器
Prominence型超快速高效液相色譜離子阱飛行時間質譜聯用儀(包括LC-20AD型二元泵,SLI-20AC型自動進樣器,CTO-20A型柱溫箱,SPD-M20A型二極管陣列檢測器,日本島津公司),安捷倫1100型高效液相色譜儀(美國安捷倫公司),XS205DU型電子分析天平(瑞士梅特勒-托利多公司),ST16R型冷凍離心機(美國賽默飛世爾公司),Milli-Q型超純水系統(美國密理博公司),KQ-500DV超聲波清洗器(昆山市超聲儀器有限公司),SevenEasy S20 pH計(瑞士梅特勒-托利多公司)。
1.2藥品與試劑
毛蕊花糖苷(成都普菲德生物技術有限公司,批號19082201,質量分數99.2%)、異毛蕊花糖苷(四川省維克奇生物科技有限公司,批號wkq20050603,質量分數92.3%)、磷酸二氫鉀(天津市風船化學試劑科技有限公司,批號20190904,分析純)、無水磷酸氫二鈉(天津市威晨化學試劑科貿有限公司,批號20140411,分析純)、冰乙酸(天津市致遠化學試劑有限公司,批號20200301,色譜純)、甲醇(默克公司)、實驗用水為Milli-Q型超純水系統制備超純水。
2、方法與結果
2.1色譜條件[1]
Agilent ZORBAX Eclipse XDB C18色譜柱(150mm×4.6mm,5 μm);流動相為0.5%醋酸水溶液(A)-甲醇(B),梯度洗脫(0~1 min,5%B;1~40min,5%~60%B;40~50min,5%B);檢測波長為254nm,進樣量為10μL,柱溫為30℃,體積流量為1mL/min。
2.2質譜條件
采用電噴霧電離離子源(ESI),正離子模式掃描,正離子模式下噴霧電壓設定為4.5kV,一級、二級離子掃描范圍均為m/z100~800,采用三氟乙酸鈉作為校正液,霧化氣為氮氣,體積流量為1.5mL/min,碰撞誘導解離能量50%;曲型脫溶劑管溫度200℃,離子累積時間為30ms,檢測器電壓1.75 kV。
2.3溶液配制
2.3.1毛蕊花糖苷對照品溶液。稱取毛蕊花糖苷對照品適量,精密稱定,置于棕色量瓶中,加20%甲醇水溶解,并定容至刻度,搖勻,制成0.2mg/mL的對照品溶液。
2.3.2異毛蕊化糖苷對照品溶液。稱取異毛蕊花糖苷對照品適量,精密稱定,置于棕色量瓶中,加20%甲醇水溶解,并定容至刻度,搖勻,制成0.2mg/mL的對照品溶液。
2.3.3磷酸緩沖液。分別稱取磷酸二氫鉀和磷酸氫二鈉適量,以水為溶劑,配制pH5、6、7的磷酸緩沖溶液。
2.4毛蕊花糖苷降解實驗
精密量取“2.3.1”項毛蕊花糖苷對照品溶液,分別與pH5、6、7磷酸緩沖液混勻(2∶1),振蕩搖勻后于沸水浴中反應,按0、30、60、90、120、150、180、210、240、300min時間點取樣,每個時間點取反應液500μL于1.5mL離心管中,離心(12000r/min,10min),取上清液于2 mL棕色液相小瓶中。
2.5毛蕊花糖苷降解規律分析
對“2.3.1”項對照品溶液和“2.3.2”項樣品,采用HPLC技術進行分析,色譜圖見圖2。以取樣時間為橫坐標,每個取樣點的峰面積為縱坐標,繪制其在加熱過程中變化規律,見圖3。從圖3可見,pH值越高,毛蕊花糖苷降解速度越快。其中pH5時毛蕊花糖苷降解緩慢,pH7在90min時毛蕊花糖苷幾乎全部降解;異毛蕊花糖苷在pH5時,其含量呈升高趨勢,隨pH升高后,其含量先升高后降低,說明毛蕊花糖苷和異毛蕊花糖苷在接近中性的水溶液中容易降解,毛蕊花糖苷和異毛蕊花糖苷適合在低pH條件下保存。在不同pH條件下,毛蕊花糖苷和異毛蕊花糖苷二者總含量均在降低,推測毛蕊花糖苷在降解過程中,生成異毛蕊花糖苷和其他降解產物,異毛蕊花糖苷在較高pH值還會繼續降解成其他產物。

圖片pH5、6、7條件下毛蕊花糖苷的降解動力學擬合見圖4。毛蕊花糖苷在pH 5時降解方程為y=0.002x+0.0054,R2=0.9991;在pH6時降解方程為y=0.013x+0.28,R2=0.9883;在pH7時降解方程為y=0.1826x+0.327,R2=0.8651;毛蕊花糖苷−ln(Ct/C0)與t的關系函數斜率即pH 5、6、7中毛蕊花糖苷的反應速率常數k呈增長趨勢,且pH5、6中毛蕊花糖苷−ln(Ct/C0)與t的線性相關系數(R2)均接近1,可見相關性很好,降解反應屬于一級反應;pH7降解速率較快,數據較少,R2為0.8651。pH5、6、7條件下毛蕊花糖苷的降解半衰期分別為346.5、51.9、3.73min。隨pH值增加,毛蕊花糖苷的降解反應速率增大,半衰期減小。通過分析毛蕊花糖苷在不同pH條件下降解反應常數及其半衰期,提示在低pH條件下毛蕊花糖苷穩定下較好,適合在低pH條件下保存。

2.6降解產物的HPLC-IT-TOF-MS鑒定
對“2.3.1”項對照品溶液和“2.3.2”項樣品,采用HPLC-IT-TOF-MS技術進行分析。典型樣品的總體離子流圖見圖5,根據色譜峰保留時間、質荷比及裂解規律信息推斷化合物結構。毛蕊花糖苷降解產物的HPLC-IT-TOF-MS信息見表1。


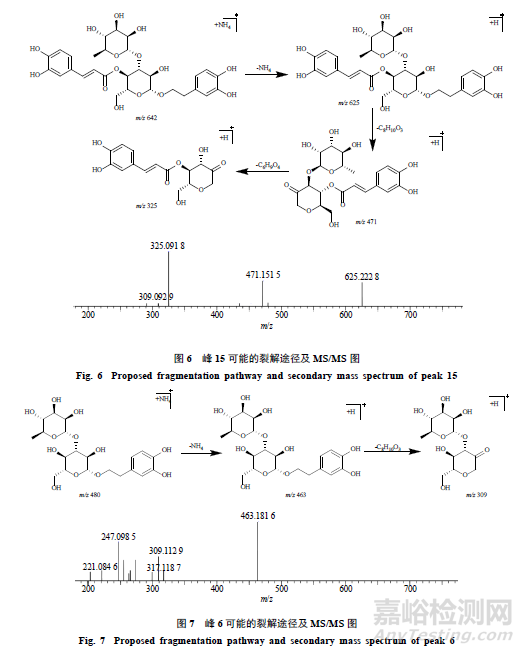
2.6.1毛蕊花糖苷原形。峰15,保留時間為26.245min,其準分子離子峰為m/z642.2381[M+NH4]+,推測的分子式為C29H36O15,誤差為−2.6×10−6,峰15與毛蕊花糖苷和異毛蕊花糖苷相對分子質量相同;在MSE質譜圖中,主要碎片有脫去1羥基酪醇(C8H10O3,154)的碎片m/z471.1515 [M+H-NH4-C8H10O3]+以及脫去1鼠李糖基的(C6H10O4,146)碎片m/z325.0918[M+H-C8H10O3-C6H10O4]+,可能的裂解規律見圖6。通過與毛蕊花糖苷對照品比對,鑒定峰15為毛蕊花糖苷。

2.6.2異構化產物。峰19,保留時間為28.412min,其準分子離子峰為m/z642.2379[M+NH4]+,推測的分子式為C29H36O15,誤差為−3.0×10−6,峰19與毛蕊花糖苷和異毛蕊花糖苷相對分子質量相同;在MSE質譜圖中,主要碎片離子m/z625.2115[M+H]+,m/z471.1500[M+H-C8H10O3]+,m/z325.0933[M+H-C8H10O3-C6H10O4]+,同峰15的裂解規律相同,通過與異毛蕊花糖苷對照品比對,鑒定峰19為異毛蕊花糖苷。
2.6.3水解產物。毛蕊花糖苷在加熱過程中發生水解反應,可能水解掉咖啡酰基、鼠李糖基、羥基酪醇等結構,水解產物包括峰6、7、8。
峰6,保留時間為11.645min,準分子離子峰為m/z480.2090[M+NH4]+,推測的分子式為C20H30O12,誤差為1.9×10−6,峰6相對于毛蕊花糖苷和異毛蕊花糖苷少了1咖啡酰基(C9H6O3,162)碎片;在MSE質譜圖中,可見脫去一羥基酪醇(C8H10O3,154)產生的碎片m/z309.1129 [M+H-C8H10O3-NH4]+,通過質譜數據推斷峰6為毛蕊花糖苷或異毛蕊花糖苷水解掉一咖啡酰基(C9H6O3,162)的產物,其可能的裂解規律見圖7。
峰8,保留時間為12.812min,準分子離子峰為m/z506.1846[M+NH4]+,推測的分子式為C21H28O13,誤差為−2.3×10−6,峰8相對于毛蕊花糖苷和異毛蕊花糖苷少了1羥基酪醇(C8H10O3,154)碎片;在MSE質譜圖中,可見脫去1咖啡酰基(C9H6O3,162)產生的碎片m/z325.0907[M+H-C9H6O3]+,通過質譜數據推斷峰8為毛蕊花糖苷或異毛蕊花糖苷水解掉1羥基酪醇(C8H10O3,154)的產物,其可能的裂解規律見圖8。毛蕊花糖苷在加熱過程中生成的水解產物還包括峰7、10、18,其可能的結構見圖9。
2.6.4氧化產物。研究[14-15]表明,鄰苯酚類化合物在過量氧存在時會發生自氧化,生成相應的半醌或醌類化合物。毛蕊花糖苷和異毛蕊花糖苷結構中均有2個鄰苯酚存在,在過量氧存在時,發生自氧化。由于結構中鄰苯酚位置不同,因此氧化產物不同,分別為峰9、10、12、14、16和18。
峰9,保留時間為16.912min,準分子離子峰為m/z654.2008[M+NH4]+,推測的分子式為C29H32O16,誤差為−5.2×10−6,峰9相對于毛蕊花糖苷和異毛蕊花糖苷少了4個H(4H)、加了1羥基(OH)碎片;在MSE質譜圖中,可見脫去1鼠李糖基(C6H10O4,146)產生的碎片m/z491.1183[M+H-NH4-C6H10O4]+,再脫去1咖啡酰基(C9H6O3,162)產生的碎片m/z329.0622[M+H-NH4-C6H10O4-C9H6O3]+,通過質譜數據推斷峰9為毛蕊花糖苷或異毛蕊花糖苷2個鄰苯酚羥基均被氧化的產物,其可能的裂解規律見圖10。
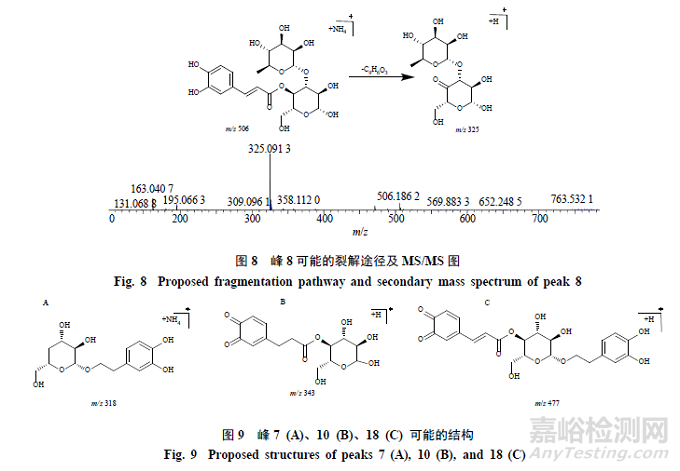
峰12,保留時間為22.612min,準分子離子峰為m/z640.2231[M+NH4]+,推測的分子式為C29H34O15,誤差為−1.6×10−6,峰12相對于毛蕊花糖苷和異毛蕊花糖苷少了2個H(2H)碎片;在MSE質譜圖中,可見脫去1鼠李糖基(C6H10O4,146)產生的碎片m/z477.1374[M+H-NH4-C6H10O4]+,再脫去1咖啡酰基(C9H6O3,162)產生的碎片離子為m/z315.0853[M+H-NH4-C6H10O4-H2O-C9H6O3]+,通過質譜數據推斷峰初步推測峰12為毛蕊花糖苷或異毛蕊花糖苷鄰苯酚羥基被氧化的產物;峰12、14和16有相同碎片和裂解規律,推測三者可能是同分異構體,其可能的裂解途徑見圖11。

2.6.5其他類。毛蕊花糖苷在加熱過程中發生水解、氧化反應,還可能發生聚合、還原等其他反應。峰4準分子離子峰為m/z171.0294[M+H]+,推測的分子式為C7H6O5,通過質譜數據推斷及參考文獻報道[16],鑒定峰4為沒食子酸。圖12為推測峰4、11、13可能的結構。
峰11,保留時間為21.245min,準分子離子峰為m/z513.1605[M+H]+,誤差為0.4×10−6,推測峰11可能是由毛蕊花糖苷結構中鄰苯酚羥基發生氧化,再失去1苯二酚(C6H6O2,110)產生的化合物C23H28O13。峰13,保留時間為23.212min,準分子離子峰為313.0704[M+H]+,誤差為−0.9×10−6,推測峰13可能是由碎片咖啡酸(C9H8O4,180)和羥基酪醇(C8H10O3,154)結合生成的化合物C17H12O6。圖13為峰11、13可能的生成途徑。


3、討論
多酚中特殊的多酚羥基結構,尤其是鄰位酚羥基,在堿性條件下容易氧化,使多酚的應用受到了很大的限制[17-18]。毛蕊花糖苷結構中存在4個酚羥基,在不同pH條件下,毛蕊花糖苷存在不同程度的降解。在弱酸性條件下,毛蕊花糖苷溶液降解緩慢;在pH7條件下其降解加快,且在90min時幾乎全部降解。Zhou等[19]研究表明在常溫條件下,毛蕊花糖苷水溶液在pH5條件下比在pH9條件下穩定,降解速率慢,高pH降解速率加快。此研究結論與本研究結果一致,但本研究還鑒定了其降解產物,并對降解途徑做了系統的推測,見圖14。毛蕊化糖苷降解可能的途徑包括異構、水解、氧化等。研究結果顯示,毛蕊花糖苷可部分降解為異毛蕊花糖苷,毛蕊花糖苷與生成的異毛蕊花糖苷繼續發生水解及氧化等降解反應,異毛蕊花糖苷含量在pH較高時呈先升高再降低趨勢,水解與氧化降解的比例隨pH升高增加。

田偉等[3]的研究顯示,車前子煎煮過程中毛蕊花糖苷含量呈現先增加后降低的變化趨勢,且隨時間的增加,其含量繼續降低,異毛蕊花糖苷含量在煎煮過程中呈增加的趨勢。本研究前期對車前子水煎液的pH進行了測定,其pH值為6.2,介于本試驗考察的pH6與7條件之間,推測車前子水煎液中毛蕊花糖苷的變化規律可能與本研究結果相似。毛蕊花糖苷的降解產物可能在車前子水煎液存在并發揮藥效,提示應關注車前子、地黃、肉蓯蓉等含毛蕊花糖苷藥材的煎液中毛蕊花糖苷的降解產物。
本研究結果顯示毛蕊花糖苷在弱酸性條件向異毛蕊花糖苷轉化,且轉化率較高。現代藥理研究表明,毛蕊花糖苷與異毛蕊花糖苷可以增強樹突狀細胞的增殖,具有免疫調節作用[20];毛蕊花糖苷具有神經保護作用[9],異毛蕊花糖苷可能通過上調神經型尼古丁受體亞單位蛋白來發揮神經保護作用[21],毛蕊花糖苷與異毛蕊花糖苷均具有抗氧化作用[22];毛蕊花糖苷與異毛蕊花糖苷具有相似的藥理活性,因此建議開展毛蕊花糖苷與異毛蕊花糖苷相關藥效等效性試驗,明確二者藥效關系。
本研究探討了影響毛蕊花糖苷穩定性的因素并對其降解產物進行分析,為毛蕊花糖苷提取、純化及車前子、地黃、肉蓯蓉等富含毛蕊花糖苷的中藥的質量控制提供了參考。

來源:Internet


