您當(dāng)前的位置:檢測資訊 > 生產(chǎn)品管
嘉峪檢測網(wǎng) 2025-06-06 12:26
藥品生產(chǎn)企業(yè)應(yīng)根據(jù)生產(chǎn)范圍、生產(chǎn)產(chǎn)品特點、業(yè)務(wù)類型、監(jiān)管要求等,結(jié)合企業(yè)實際,針對不同崗位,分類分層制定培訓(xùn)計劃,明確培訓(xùn)內(nèi)容,強化對質(zhì)量關(guān)鍵(主要)崗位人員的質(zhì)量安全培訓(xùn)和崗位技能培訓(xùn),開展履職能力、日常工作、綜合成效動態(tài)評估,強化結(jié)果應(yīng)用,確保履職盡責(zé)。
1、企業(yè)內(nèi)部培訓(xùn)與考核
企業(yè)應(yīng)建立內(nèi)部質(zhì)量培訓(xùn)制度, 對質(zhì)量安全人員進行崗前培訓(xùn)和繼續(xù)教育,并對培訓(xùn)、考核情況予以記錄。鼓勵企業(yè)使用信息化技術(shù)開展內(nèi)部培訓(xùn)與考核工作。對培訓(xùn)考核不通過且補考仍未通過的,應(yīng)不予上崗、轉(zhuǎn)崗或離崗。
企業(yè)應(yīng)根據(jù)實際需要,分類分級制定培訓(xùn)計劃。培訓(xùn)計劃應(yīng)明確培訓(xùn)時間、內(nèi)容以及培訓(xùn)對象。培訓(xùn)內(nèi)容應(yīng)至少包括:藥品生產(chǎn)相關(guān)法律法規(guī)、藥品專業(yè)知識及技能、質(zhì)量管理制度、職責(zé)及崗位操作規(guī)程。從事特殊管理藥品生產(chǎn)的企業(yè),還應(yīng)當(dāng)符合國家相關(guān)法律法規(guī)的培訓(xùn)規(guī)定。
2、企業(yè)內(nèi)部培訓(xùn)的內(nèi)容
企業(yè)應(yīng)根據(jù)藥品法律法規(guī)和質(zhì)量管理體系文件的變化,及時更新培訓(xùn)內(nèi)容。培訓(xùn)計劃可參考如下:
藥品相關(guān)法律法規(guī)培訓(xùn):如《藥品管理法》《藥品生產(chǎn)監(jiān)督管理辦法》《藥品生產(chǎn)質(zhì)量管理規(guī)范及其附錄》等。這些法規(guī)是藥品生產(chǎn)操作的基本準(zhǔn)則,應(yīng)定期或在法規(guī)有新增/ 更新時進行開展這些培訓(xùn)。考核的方式可以是試卷、測試等,企業(yè)可根據(jù)崗位的重要性、試卷難易程度等因素設(shè)置合格分?jǐn)?shù)線。
藥品專業(yè)知識及技能:包括藥品生產(chǎn)相關(guān)知識、驗證與校準(zhǔn)相關(guān)知識等。培訓(xùn)方式可以多樣化,可現(xiàn)場授課、線上授課或自主學(xué)習(xí),考核方式除了試卷、測試外,還可以是調(diào)查問卷或?qū)嵺`操作。培訓(xùn)周期同樣是定期或指南、指導(dǎo)原則有新增/ 更新時進行。
質(zhì)量管理體系文件:涉及產(chǎn)品研發(fā)和技術(shù)轉(zhuǎn)移的規(guī)定,偏差管理、變更管理、文件管理、記錄管理、培訓(xùn)管理等內(nèi)容。培訓(xùn)對象根據(jù)文件規(guī)定有所區(qū)分,關(guān)鍵人員需定期培訓(xùn),主要人員則要定期或有變更時培訓(xùn)。考核方式以試卷、測試、調(diào)查問卷為主。
職責(zé)及崗位操作規(guī)程:包括崗位職責(zé)說明書、作業(yè)指導(dǎo)書或操作管理規(guī)程等內(nèi)容。培訓(xùn)方式包括現(xiàn)場授課、實操、線上授課或自主學(xué)習(xí),考核方式為試卷、測試、實踐操作或模擬演練,培訓(xùn)周期為定期或有變更時。

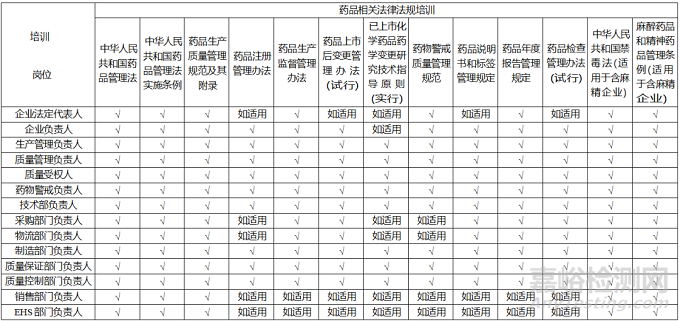
3、企業(yè)內(nèi)部培訓(xùn)矩陣
可參考下表制定公司內(nèi)部的培訓(xùn)矩陣:



來源:Internet


