您當(dāng)前的位置:檢測資訊 > 科研開發(fā)
嘉峪檢測網(wǎng) 2024-06-03 12:21
腹膜透析設(shè)備是指將透析液灌入患者的腹腔,利用腹膜完成透析,隨后再把液體引出腹腔的過程所使用的醫(yī)用電氣設(shè)備。
根據(jù)《醫(yī)療器械分類目錄》,分類編碼為10-03-06,管理類別為Ⅱ類。
一、腹膜透析設(shè)備的工作原理與結(jié)構(gòu)組成
1、工作原理
腹膜透析設(shè)備完成透析治療過程主要分為兩種方式:壓力控制方式和重力控制方式。
1.1壓力控制方式
利用壓力方法,將腹膜透析液輸送到腹膜透析設(shè)備,經(jīng)過腹膜透析設(shè)備加熱輸送到患者腹腔,經(jīng)留腹透析交換后引流到廢液裝置內(nèi)的方式。(透析液袋可平放)

1.1.2重力控制方式
利用重力方法,液體由高向低流動的特性,實現(xiàn)腹膜透析液從高點流向腹膜透析設(shè)備,經(jīng)過腹膜透析設(shè)備加熱灌入患者腹腔,經(jīng)留腹透析后引流到廢液收集裝置內(nèi)的方式。(透析液袋高于腹膜透析設(shè)備的加熱裝置)

2、結(jié)構(gòu)組成
腹膜透析設(shè)備通常由主機(jī)、控制單元、加熱器等組成。
產(chǎn)品結(jié)構(gòu)主要有以下兩類:壓力控制型腹膜透析設(shè)備(產(chǎn)品示例如圖一)、重力控制型腹膜透析設(shè)備(產(chǎn)品示例如圖二)。

圖一 壓力控制型腹膜透析設(shè)備

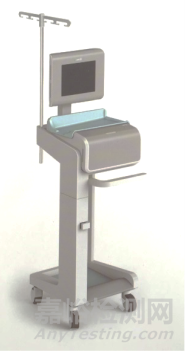
圖二 重力控制型腹膜透析設(shè)備
注:上述結(jié)構(gòu)組成及示意圖僅供參考,具體產(chǎn)品結(jié)構(gòu)組成應(yīng)根據(jù)實際產(chǎn)品確定。
二、腹膜透析設(shè)備的主要風(fēng)險
下表所列為常見可預(yù)見事件序列/可能的傷害示例,需關(guān)注:
表 常見可預(yù)見事件序列/可能的傷害示例
|
危險 |
可預(yù)見的事件序例 |
可能產(chǎn)生的傷害 |
|
|---|---|---|---|
|
能量危險 |
電磁能 |
設(shè)備受電磁干擾; 設(shè)備產(chǎn)生電磁能 |
運行異常或不能工作,影響透析治療。 患者不能進(jìn)行透析治療。 影響操作者健康或其他設(shè)備的使用。 |
|
網(wǎng)電源 |
網(wǎng)電源不穩(wěn)定 |
設(shè)備不能正常工作,影響透析治療。 |
|
|
漏電流 |
電擊 |
操作者或患者受電擊傷害 |
|
|
熱能 |
設(shè)備加熱功能失常 |
操作者或患者皮膚被燙傷; 透析液溫度超溫或過低灌入患者腹腔,傷害患者,影響透析治療。 |
|
|
重力 |
液袋墜落傷害(如適用) |
砸傷操作者,損壞藥液,影響治療。 |
|
|
機(jī)械能 |
產(chǎn)生動力的壓力源或氣泵失控透析液管路壓力過高或過低 |
傷害患者,影響透析治療。 |
|
|
貯存的能量(若有備用電源) |
蓄電池超期使用 |
設(shè)備某些功能失效,影響透析治療。 |
|
|
性能有關(guān)的危險 |
不正確或不適當(dāng)?shù)妮敵龌蚬δ?/span> |
控制軟件或程序不完善;操作錯誤 |
影響透析治療;患者受到過熱或低溫傷害;患者受過量注入或引流不足傷害。 |
|
不正確的測量 |
軟件缺陷;元器件損壞 |
溫度和液體量等數(shù)據(jù)的測量不準(zhǔn)確,患者受到過熱或低溫傷害,液體量不足或過多影響透析治療。 |
|
|
錯誤的數(shù)據(jù)轉(zhuǎn)換 |
電子器件損壞或受到干擾;軟件缺陷 |
||
|
功能喪失或變壞 |
加熱和測量等功能喪失或變壞 |
||
|
使用錯誤 |
不正確的參數(shù)設(shè)置,錯誤的安裝 |
影響透析治療 |
|
|
不遵守規(guī)則 |
不遵守醫(yī)囑設(shè)置參數(shù) |
影響透析治療 |
|
|
信息危險 |
不完整的使用說明書或操作說明書 |
使用或操作說明存在缺陷過于復(fù)雜或缺少步驟描述 |
不能正常使用設(shè)備,影響透析治療。 |
|
產(chǎn)品所使用的附件不適當(dāng) |
型號不統(tǒng)一 |
設(shè)備不能被正確的使用,影響透析治療。 |
|
|
不適當(dāng)?shù)臉?biāo)記 |
標(biāo)記缺失,不明顯,不規(guī)范 |
錯誤使用設(shè)備,影響透析治療。 |
|
三、腹膜透析設(shè)備性能研究實驗要求
1、電氣系統(tǒng)安全性研究
應(yīng)當(dāng)開展電氣安全性、機(jī)械和環(huán)境保護(hù)以及電磁兼容性的研究。
2、軟件研究
腹膜透析設(shè)備軟件通常作為軟件組件體現(xiàn),應(yīng)按《醫(yī)療器械軟件注冊審查指導(dǎo)原則(2022年修訂版)》開展軟件研究(含現(xiàn)成軟件研究、互操作性研究、GB/T 25000.51-2016自測),軟件安全性級別通常為中等。
具備電子數(shù)據(jù)交換、遠(yuǎn)程控制或用戶訪問功能的產(chǎn)品,應(yīng)當(dāng)開展網(wǎng)絡(luò)安全研究,還應(yīng)當(dāng)按照《醫(yī)療器械網(wǎng)絡(luò)安全注冊技術(shù)審查指導(dǎo)原則(2022年修訂版)》的要求單獨提開展絡(luò)安全研究。
3、清潔和消毒研究
3.1使用者清潔和消毒(如適用):應(yīng)當(dāng)明確推薦的清洗和消毒工藝(方法和參數(shù))、工藝的確定依據(jù)并開展相關(guān)驗證。
3.2若清潔、消毒方法可能出現(xiàn)殘留,開發(fā)人需要開展殘留物毒性的相關(guān)研究。
4、穩(wěn)定性研究
4.1使用穩(wěn)定性
應(yīng)當(dāng)開展設(shè)備使用穩(wěn)定性/可靠性研究,證明在規(guī)定的使用期限內(nèi),產(chǎn)品的性能功能可以滿足臨床使用要求。可參考《有源醫(yī)療器械使用期限技術(shù)審查指導(dǎo)原則》的要求進(jìn)行驗證。
4.2運輸穩(wěn)定性
應(yīng)當(dāng)開展運輸穩(wěn)定性和包裝研究,證明在生產(chǎn)企業(yè)規(guī)定的運輸條件下,運輸過程中的環(huán)境條件(例如:震動、振動、溫度和濕度的波動)不會對醫(yī)療器械的特性和性能,包括完整性和清潔度,造成不利影響。
開發(fā)人可以參考GB/T 14710等相關(guān)標(biāo)準(zhǔn)進(jìn)行研究。

來源:嘉峪檢測網(wǎng)


