摘要
近年來,隨著人口老齡化時代的到來以及人民健康意識的普追提高,疾病預防及早期干預越來越受到重視,具有“治未病”獨特優勢的中醫藥產業迎來巨大的發展機遇�。尤其在全球新型冠狀病毒肺炎(COVID-19)大流行的特殊背最下。中醫藥發揮了重要作用,更為其產業化發展提供了良好契機���。隨著我國一系列政策的出臺,中藥傳承創新發展已進入快車道。本文對國內外中藥市場、中藥企業研發投入、中藥創新藥審批趨勢��、中藥國際化以及近 20 年中藥專利布局進行調研,分析我國中藥創新發展現狀,并對未來趨勢做出展望���,以期對我國中藥傳承創新發展提供啟示�����。
[關鍵詞] 中藥;創新藥��;研發�;專利;趨勢分析
隨著《中華人民共和國中醫藥法》���、《中醫藥發展戰略規劃綱要(2016-2030 年)》《促進健康產業高質量發展行動綱要(2019-2022 年)》、《中共中央國務院關于促進中醫藥傳承創新發展的意見》[1-4]等法律法規政策的出臺,鼓勵中藥新藥研發與創新���、促進中藥產業化高質量發展成為中藥領域未來的核心發展路徑。2021 年��,我國更是迎來中醫藥政策落地暴發期����。經過多年的發展與探索���,國家對中醫藥的支持政策已由頂層設計逐步過渡到落地執行階段,具有更強的連貫性���。在抗擊新型冠狀病毒肺炎(COVID-19)疫情期間通過臨床篩選出的“三藥三方”也發揮了重要作用��。未來,中藥無論是在我國還是在全球范圍內都將迎來更大的發展潛力。
2020 年版《藥品注冊管理辦法》的中藥注冊分為4類�,分別是中藥創新藥����、中藥改良型新藥�����、古代經典名方中藥復方制劑及同名同方藥]�。其中1類創新型中藥和3類古代經典名方的開發將是中藥創新傳承發展重點鼓勵的研究方向[6-8]�����。
中藥專利保護是促進創新中藥及經典名方研發的重要措施,是中藥國際化的必然要求,并可指引未來中藥創新藥布局的技術及方向�����,值得深度挖掘�����。其中發明專利審查嚴格.對新穎性�、創造性的要求高,法律地位相對穩定,是衡量一個國家/地區科技創新能力的重要指標叨��。本文從國內外中藥市場中藥企業研發投入創新藥審批趨勢 中藥國際化以及專利布局角度,分析我國中藥創新發展現狀及現存問題.并對未來趨勢做出展望.以期對未來我國中藥傳承創新發展提供啟示���。
一��、數據來源與方法
本文所列中藥市場數據主要來源于米內數據庫和網絡公開數據,創新藥審批信息 、中藥國外上市和臨床注冊信息主要來源于藥渡和 CPM 數據庫��。本文所收集的中藥創新藥注冊審批數據為按《藥品注冊管理辦法》2007 年版中藥1- 6類注冊申請及2020 年版的1類新藥注冊申請的藥物信息���。
中藥專利數據來源于 Incopat 數據庫,利用關鍵詞“中藥”“草藥”“天然藥物”��、“植物藥”��、“提取物“ Traditional Chinese Medicine” ," Chinese Mate.rial Medicine” ,“Herbal Medicine * " ,“Natural Medicine” " Botanical Or “ Natural Product * ” “ MarineMedicine”,“Marine Drug” ,“ Marine Produet” , “ Extract"和 IPC 分類號進行檢索,并將申請日限定在2002 年1 月1 日-2021 年 12 月 31 日申請類型為發明專利。清洗不相關的專利并以簡單專利族計����,最終獲得在全球申請的 25.5 萬件專利,在中國大陸申請的 21.9 萬件專利,其中,國內申請剔除個人申請后的職務發明專利共計 10.7 萬件�����。文中涉 及專利授權率為專利授權量/專利申請量,轉化率為專利轉化量/專利申請量.其中專利轉化量為發生過權利轉讓和許可行為的專利數。
本文采用 Excel 和帆軟報表軟件開展數據清洗和數據分析�����。由于信息公開不充分及檢索方式的原因�����,個別信息可能存在遺漏。
二、中藥市場分析
2.1 全球中藥市場
隨著全球對天然植物藥的接受度提高,全球中藥類產品市場發展迅猛。Fortune Business Insights數據顯示.2021 年全球中草藥( herbal medicine)市場約為1 519 億美元,預計 2029 年將增至 3 475 億美元����。其中.藥品/營養品細分市場占據主導地位約占據總體中草藥市場的 60% 以上]�����。在當前全球 COVID-19 大流行的特殊背景下.與大流行前相比.全球所有區域的草藥需求都高于預期。以中國日本、韓國為代表的傳統中藥市場�、北美市場��、歐洲市場和非洲/阿拉伯市場是全球四大主要中草藥市場.這 4 個植物藥市場約占全球植物藥市場年銷量的90%[11]。
2.2 我國中藥市場
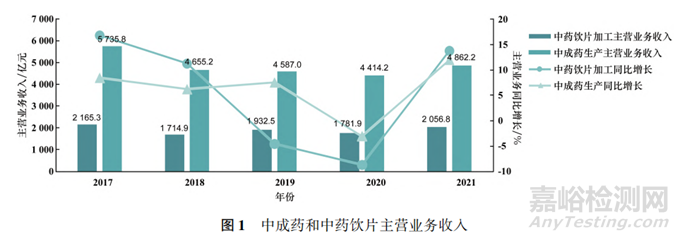
2017一2020 年間.我國中藥主營業務收人呈下滑態勢,而在 2021 年實現了恢復性增長。2021 年中藥工業主營業務收人達到6919億元,占醫藥工業總主營業務收人的 21.3%利潤總額為 1004 億元�����。其中,中成藥生產主營業務收入為 4862.2 億元.同比增長 11.9%:中藥飲片加工為 2056.8 億元,同比增長 13.7%(見圖 1)。中藥行業競爭力增強�����,實現高質量增長�。
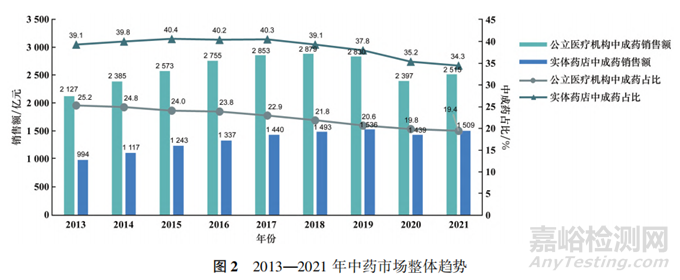
2021 年,我國公立醫療結構( 包括城市公立醫院、城市社區醫院�、縣級公立醫院����、鄉鎮衛生醫院)和零售實體藥店中成藥銷售額均有所上漲,整體市場達4024億元[12]�。其中公立醫療機構的中成藥銷售額為2515億元,占總體公立醫療藥品銷售的19.4% ;零售實體藥店中成藥銷售額達1509億元占藥店總體零售銷售額的34.3%(見圖 2)。公立醫療機構中成藥銷售額在2018年見頂��,且占比持續下滑�,可能原因是 2017 年版醫保目錄對多款重磅中藥注射劑附加了醫保限制�。
心血管疾病和呼吸系統疾病是中成藥應用的兩大主要疾病領域。心血管疾病急性期患者一般需要住院,用藥結構以日均費用較高的注射劑為主,是中成藥院內用藥的第一大疾病領域:呼吸系統疾病的多數患者無須住院,用藥結構以日均費用較低的口服制劑為主,是中成藥院外用藥的第一大領域���。
三、中藥企業研發投入
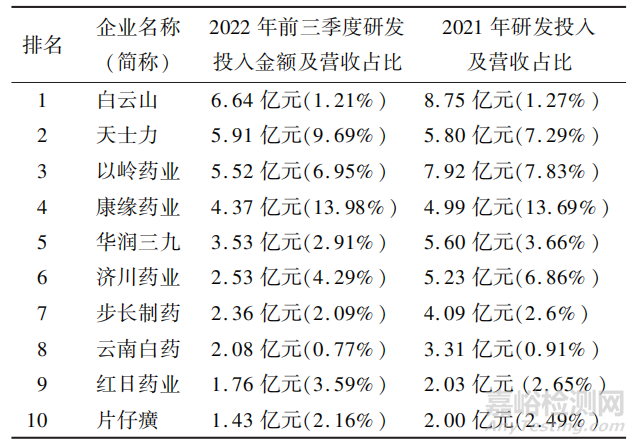
相對于化學藥和生物藥,中藥領域研發投入相對偏低,增加研發投入已經成為業內本階段的主要發展趨勢。在2022 年 A 股 75 家中藥企業公布三季報的公司中��,研發投入金額排前 5 名的企業(簡稱)分別為:白云山(6.64 億元)��、天士力( 5.91 億元)以嶺藥業(5.52 億元) 康緣藥業(4.37 億元)華潤三九(3.53 億元)��,見表 1。多數中藥企業的研發投入占營業收入比重低于 5%,處于較低水平����?��?稻壦帢I 2021 年營收占比為 13.69%,位居首位�����,但仍低于以創新化藥和生物藥研發為主的恒瑞醫藥的研發投入(2018-2021 年營收占比為 15.33% ~22.94% )中藥的研發成本相對較低,一般而言,單個中藥創新藥品種需要的研發費用在千萬元左右。分析中藥頭部企業 2019-2022 年獲批的9 款產品的研發投入顯示,單個產品的研發總投入在1000~5000萬元平均為2635萬元[2-13],見表2�����。
▲表1-2022年 A 股75 家中藥企業公布的三季報研發投入金額前 10 名
▲表2-2019-2022 年獲批的9款創新產品的研發投入
四��、中藥創新藥審批趨勢
截至 2022 年 10 月2022 年國家藥品監督管理局(NMPA)共批準了2款中藥創新藥上市,分別為廣金錢草總黃酮提取物和阿可拉定(淫羊董素)��。而在2021年,NMPA 共批準了 9 個創新藥,此外還有3個通過特別審批程序應急批準的來源于古代經典名 方的清肺排毒顆粒��、化濕敗毒顆粒�、宣肺敗毒顆粒[ 14]中藥臨床申請(IND)和上市申請(NDA)的申請品種適應證相對集中,集中在呼吸系統疾病、消化系統疾病、神經系統疾病、婦科病和心血管系統疾病 5個治療領域,其他治療領域的申報量相對較少,這與近年來中成藥市場的占比也較為一致�。自 2011 年至2022 年 10 月NMPA 已批準了 88 個中藥創新藥,NDA 批準量自2013 年達頂峰之后���,一直呈下降趨勢,但 2019 年之后在不斷復蘇.且審評速度在不斷加快。這 88 個創新藥中�����,10 個為 1類中藥��、3 個為3 類中藥�����、15 個為5 類中藥、60 個為6類中藥���,見圖3。
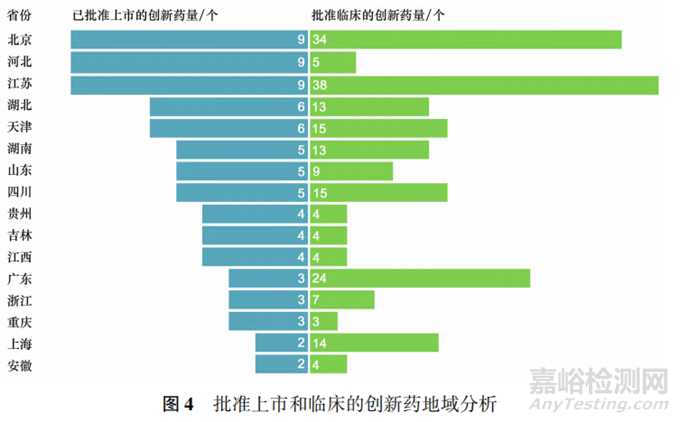
從地域看���,2011-2022 年 10 月批準的88個創新藥中,北京市�����、河北省與與江蘇省的公司上市藥物量最多�����,均為 9個�,并列全國第一位��;在此期間批準臨床的創新藥共計 281 個�,以江蘇省和北京市居多,超過 30 個�����。河北省的公司雖然在此階段新藥上市量居首���,但新藥臨床量卻并未在第一梯隊( 見圖 4)�。
五��、中藥國際化
近年來�����,我國中藥的海外注冊取得了較大突破多款中藥在海外獲得上市許可。2012 年�,荷蘭藥物評價委員會( CBG-MEB)按照《歐盟傳統植物藥注冊程序指令》( Directive 2004/24/EC)的簡化注冊程序批準了穿龍薯黃(穿山龍)根蕓的干燥提取物地奧心血康膠囊的上市注冊申請�;2015 年香雪制藥的抗病毒口服液在加拿大上市�,2017 年其板藍根顆粒在英國獲批上市,成為首個以治療感冒為主要適應證在英國上市的中成藥����;2016 年����,和黃藥業的膽寧片在加拿大獲批上市�����,成為首個“功能主治”全部被歐美國家監管當局認可的復方中藥�;2017 年華西藥業的樂脈顆粒在加拿大獲批上市����,治療冠心病心絞痛多發性腦梗等相關癥狀。截至 2022 年 1 月���,以嶺藥業的連花清瘟膠囊已經在27個國家和地區獲得注冊批文或進口許可[15],見表3�。這些產品在國外市場的成功標志著我國中藥國際化進展取得了關鍵性突破��,中醫藥企業已邁進國際市場。
▲表 3-我國中藥企業研發的中成藥在國外上市詳情
雖然中成藥在海外的注冊取得了進步����,但美國市場的藥品注冊一直未能突破,在美國 FDA申請臨床注冊的企業有許多,但進程緩慢步履維艱。以天士力為例���,早在 1997 年,復方丹參滴丸就以治療藥身份通過了美國 FDA 的IND 申請。目前該藥針對恨性穩定性心絞痛的適應證的亞期臨床研究尚在進行中針看�����,對急性高原綜合征(AMS)I 期臨床試驗已完成,亞期臨床試驗在招募中����。康緣藥業的桂枝獲參膠囊于 2009 年完成I 期臨床試驗。目前尚在推講但美國依然是中藥企業研發重點關注的市場,據不完全統計���。目前有 23 個藥物已在美國注冊臨床試驗,其中大多為近 2 年新增品種,如用于癌癥治療的養正合劑、養陰扶正解毒療法,用于 COVID-19 的金振口服液、扶正化瘀片,用于腦產中的麝香保心丸、安宮牛黃丸���、血栓通、醒腦靜、補氣通終顆粒等�����。
六�����、專利布局分析
6.1 全球中藥專利布局概況
近 20 年,全球中藥研究總體呈上升趨勢,但自 2015 年以來熱度在降低���,專利質量尚待提升��,2002-2021 年 全球中藥領域共由請了 25.5 萬件專利,其中有效專利 8.3 萬件、失效專利 21.8 萬件尚在審評中的專利共計 3.1 萬件�����。
全球中藥專利申請的年度申請量由 2002 年的2 582 件增長到 2015 年的約 3 萬件 隨后一直處于下降趨勢.2020 年的年度申請量為 1.1 萬件���,見圖5���。
近 20 年申請的中藥專利中,我國申請人申請的專利占全球申請的 85.5%,其次是韓國(4.6% )��、日本(3.8%)�����、美國(1.7% )和俄羅斯(0.5%)。其他國家申請人申請的專利量不足 4%。
6.2 我國中藥專利布局概況
6.2.1 申請趨勢
2002-2021 年,我國專利申請近 22 萬件,其中個人申請占 51%���,企業、大專院校機關團體及科研單位的申請分別占 35%,7%,4%和3%。由于個人專利存在非正常專利申請嚴重的情況,本文以下的國內數據依據剔除個人申請后的10.7 萬件職務發明專利進行分析����。
2002-2021 年�,我國中藥專利申請形成了明顯的:階段發展態勢��。中藥專利申請量在 2002-2011年期間緩慢增長���,在 2012-2016 年期間呈現出快速增長的趨勢����,2017 年后年申請量開始逐漸下降( 見圖 6)��。專利申請量先升后降�����,反映了我國在中藥領城由專利弱國向數量大國進而向高質量大國的轉變過程。
6.2.2 專利質量分析
在此期間申請的專利已被授權專利為 2.9 萬件�,總體授權率為 26.8%(專利授權量/專利申請量)���。在2013 年之前,專利的授權率基本在 40% 以上���,但在隨后的幾年里,中藥領域專利授權率出現了斷崖式下降,2016 年僅有 11%��。近幾年授權率有所上升����,但仍然低于我國發明專利平均專利授權率。此外����,在此期間申請的專利存活期在5年以下的(包括5 年)占 81%存活期在 10年以上的(不包括 10 年)專利僅有 6%�����。
6.2.3 專利申請區域分布
國內中藥領域專利申請區域排名以山東省居于首位,廣東省����、江蘇省����、北京市���、四川省���、安徽省��、天津市���、河南省、廣西壯族自治區��、浙江省也是申請量靠前的省市,見圖 7�����。
6.2.4專利申請人分析
2002-2021 年��,我國中藥行業專利申請人中�,天士力的專利申請量和授權率均較高,康緣藥業���、北京亞東生物制藥���、以嶺藥業和步長制藥的專利申請量雖不屬于第一梯隊����,但授權率較高,創新能力居于前列:國內多所高校如上海中醫藥大學����、黑龍江中醫藥大學的專利授權率也居于前列�。北京藝信堂醫藥研究所以 763 件的專利申請量居于申請人排名首位,但其專利授權率僅有5%����,見圖8。創新力居于前列的申請人的疾病布局方向各有不同�,如北京亞東生物制藥重點布局的適應證是呼吸系統疾病和生殖系統疾?����。徊介L制藥重點布局領域為心血管系統疾病與消化系統疾?����?�;康緣藥業在消化道疾病和呼吸系統疾病有較多的專利布局;以嶺藥業的重點布局方向為心血管系統疾病神經系統疾病與代謝疾病�;天士力重點布局領域為心血管系統疾病��、腫瘤和神經系統疾病。但總體而,這些企業/機構的專利布局方向與其產品線較為致���,尚不豐富。
6.2.5 專利申請的疾病領域分析
在腫瘤/免疫制劑、感染���、抗炎鎮痛及皮膚疾病等領域,創新的投入與產出比例尚小,新藥研發的難度比較大。消化系統疾病�����、感染���、腫瘤/免疫���、抗炎鎮痛�、生殖/泌尿系統疾病是專利申請涉及較多的疾病領域。從 2002-2021年批準的中藥創新藥 IND 及 NDA 看,這些藥物涉及前五大治療領域是消化系統疾病�、呼吸系統疾病���、牛殖/泌尿系統疾病����、血液或細胞外液疾病以及肌肉或神經肌肉系統疾病����,見圖 9。
6.2.6 專利轉化趨勢
我國中藥領域專利的轉化量在 2017 年之前都呈上升趨勢,之后在不斷下降與我國專利申請量呈正相關����。2002-2021 年期間國內申請的專利成功實施轉化的共有8520件,總體轉化率為 7.9%,與 2021 年我國發明專利許可率���、轉讓率基本持平(許可率、轉讓率分別為 10.4%和7.4% )[16] ���,但低于美國(72.3% )、歐盟(21.6% )和日本(11.1%)的中藥專利轉化率����,見圖10���。
七�����、結語
通過對中藥市場����、中藥企業研發投入��、中藥創新藥審批趨勢�����、中藥國際化以及中藥專利布局分析,得出以下結論:(1) 我國中藥市場的規模和新藥研發活躍度在全球都占有舉足輕重的地位,我國中藥行業正邁向高質量發展新階段���。(2) 在國家政策和市場的刺激下,中藥創新藥研發已取得階段性成果,研發積極性有了明顯提升,但還需進一步激發[17]�。(3)中藥國際化已走上創新發展之路����,在歐洲���、東南亞部分地區已取得上市的突破��,但仍然任重而道遠,在美國的注冊上市及開展臨床的產品尚未取得重大突破。(4) 中藥創新藥研發地域發展不均衡���,北京市與江蘇省無論在新藥產出還是在專利布局上,都居于全國領先地位�,但西部地區如新疆維吾爾自治區�、西藏自治區�、甘肅省、云南省等尚處于落后階段�����。(5)我國企業/機構對產品的專利布局越來越重視���,但中藥領域總體專利質量和轉化水平偏低,有大量的非職務申請,專利轉化率低于美國����、歐盟和日本。(6 )在疾病領域方面,中藥創新藥的研發����、產出及專利布局均以消化系統疾病�、呼吸系統疾病�、心血管系統疾病為主,部分疾病領域如腫瘤/免疫制劑、感染�����、抗炎鎮痛及皮膚疾病雖有大量的創新研究,但創新藥產出的成功率較低����。
我國中藥行業已走過野蠻生長階段,未來將更加強調以臨床價值為導向的創新藥物研發[8-23]�����;面對中藥行業變革�����,增加研發投入已經成為業內本階段的發展趨勢;北京市與江蘇省的中藥領域領軍效應與頂層設計、產業集聚效應密切相關,打造領先的創新中藥產業化基地是促進中藥行業高質量發展的可行路徑,未來國內產業集聚效應將更加明顯。此外,在成果轉化方面����,近年來國家和地方也出臺了一系列政策促進科技成果轉化[24-25]�,強化企業在專利技術轉化中的主體地位��,構建以企業為主體���、產學研協同的創新體系��,這也是引領帶動行業技術進步的有效途徑����。綜上所述,中藥行業未來將更趨向于堅持創新驅動發展戰略,不斷提高行業核心競爭力���,尋求新的增長點�,從而實現國際國內長遠發展。
參考文獻
[1]國家中醫藥管理局.《中華人民共和國中醫藥法》[ EB/OL].(2016 - 12 - 26 ). hllp://fjs. satcm. gov. cn/zhengcewenjian/2018-03-24/2249.html.
[2]中華人民共和國中央人民政府.國務院關于印發中醫藥發展戰略規劃綱要(2016-2030 年)的通知( 國發[2016]15 號)[EB/OL].(2016 - 02 - 26 ). http://www. gov. cn/zhengce/content/2016-02/26/content 5046678.htm.
[3]中華人民共和國中央人民政府����。促進健康產業高質量發展行動綱要(2019-2022 年)[ EB/0L].(2019 -09 - 30).hlp://www. gov. cn/xinwen/2019-09/30/content 5435160. htm.
[4]中華人民共和國中央人民政府.中共中央 國務院關于促進中醫藥傳承創新發展的意見[ EB/OL].(2019 - 10 -26).hl-tp://www. gov. cn/zhengce/2019-10/26/content 5445336. htm.
[5]國家市場監督管理總局.藥品注冊管理辦法(國家市場監督管理總局令第 27 號)[EB/OL].( 2020 - 01 - 22 ). htp://www. gov. cn/gongbao/content/2020/content 5512563. htm.
[6]劉建勛,李艷英,付志明. 中藥新藥傳承發展與創新之路J7.中國現代中藥���,2021��,23(1): 14.
[7]瞿禮萍,唐健元.張磊,等。我國中藥注冊分類的歷史演變����、現狀與問題[]J].中國中藥雜志,2022,47(2): 562 -568.
[8]梁愛華.韓佳寅,陳士林,等.中藥經典名方的質量與安全性考量[]].中國食品藥品監管�、2018(6):4 -10.
[9]張婷.盧巖,陳娟,等.我國生物醫藥領域技術創新態勢研究[J].中國新藥雜志���,2020��,29(22): 2521 -2527.
[10]Fortune Business Insights. Herbal Medicine Market Size , Share% COVID-19 Impact Analysis , By Application( Pharmaceutical &Nutraceutical , Food & Beverages, And Personal Care & BeautyProducts) , By Form ( Powder , Liquid & Gel, And Tablets &Capsules ) ,And Reginal Forecast,2022 - 2029[ EB/0L].( 2022 -07 -03 ). https ://www. fortunebusinessinsights. com/herbal-medi-cine market-106370
[11]王春麗,高月紅,黃瑤慶,等.中國中藥行業格局及未來展望[J].中國新藥雜志,2020�����,29(16): 1845 -1850.
[12]周小剛����。中藥創新藥行業深度報告:政策邊際改善明顯,中藥創新藥迎來增長新階段[ R].北京:國海證券。2022.
[13]健民集團.健民藥業集團股份有限公司關于七蕊胃舒膠囊獲批上市的公告[ R].湖北:健民集團,2022.
[14]國家藥品監督管理局.國家藥監局批準清肺排毒顆粒�、化濕敗毒顆粒����、宜肺敗毒顆粒上市[EB/OL].(2021 -03 - 02).hps://www. nmpa. gov. cn/yaowen/ypigyw/20210302190503177. html.
[15]新華網��。以嶺藥業中成藥連花清瘟已獲 27 個國家上市注冊EB/OL]. ( 2022 - 01 - 27 ). http ://www. news. cn/fortune2022-01/27/c 1128304635.htm.
[16]國家知識產權局.國家知識產權局2021 年度報告[R].北京國家知識產權局���,2022.
[17]洪峰,褚丹丹,徐慧芳,等.近年我國中藥新藥審批及注冊申請現狀分析[J].中國新藥雜志,2021,30(14):1260 -1265.
[18]雷翔���,商洪才�����,高春升,等��。中藥新藥研發臨床定位的相關思考[].中國新藥雜志����,2023�����,32(17): 1703 -1706.
[19]郭慶�����,鄧勇。藥物臨床試驗合作中的法律風險識別與防控J7.中國新藥雜志�����,2023��,32(17 ): 1761 - 1767.
[20]佟梁慧�����,張帆,孫潭霖����,等.中國臨床試驗數據監管改革的分標與思考廠7.世界臨床藥物��,2023����,44( 8): 882 -890
[21]蘭婭菲�����,陳穎�����,韓朦����,等.中國藥品監管政策網絡演化和發展研究[]].中國現代應用藥學,2023����,40(17): 2346 -2353.
[22]蔣杰����,唐洪梅��,伍俊妍�,等.中成藥創新內涵專家共識[J].今日藥學����,2022、32(10): 721 - 724.123
[23]湯涵��,苗采烈�����,林凡鈺��,等.中國醫藥工業發展現狀淺析與未來挑戰廠]].中國醫藥工業雜志,2021����,52(11): 1534 - 1544.
[24]上海市人民政府.上海市人民政府辦公廳關于印發《上海市促進科技成果轉移轉化行動方案( 2021-2023 年)》的通知(滬府辦規[ 2021]7 號)[ EB/OL].(2021 -06 - 11 ).hltps ://www. shanghai. gov. cn/nw12344/20210610/a5cafle9734945919(4aab02bdafdd10. html.
[25]中華人民共和國中央人民政府.國務院辦公廳關于印發促進科技成果轉移轉化行動方案的通知( 國辦發[ 2016]28 號)[EB/OL].(2016 - 05 - 09 ). htp://www. gov. cn/zhengce/content/2016-05/09 /content 5071536. htm.