近年來,連續制造技術在制藥行業中備受關注,該技術以其降本增效、提高生產率等顯著優勢備受追捧,并成為未來制藥行業的發展趨勢���。相比傳統的批量生產方式,連續制造技術具有實時可控、綠色智能等特點�,能夠幫助制藥企業更加高效地生產藥品�����。然而,在中藥制藥領域中��,連續制造技術的推廣應用緩慢����。一方面,符合中藥制劑特點的連續制造設備和技術研究還不夠充分���;另一方面,復合型人才匱乏等問題也影響了其發展。因此�,為了促進中藥制藥行業的現代化和升級���,該文結合中藥產業發展現狀��,概述連續制造技術的發展狀況和監管要求。同時,還將對現有中藥制造模式的問題進行分析,探討連續制造技術在中藥制藥領域中的應用前景和存在的挑戰。在分析中�,將重點剖析連續制造控制策略��、技術工具和制藥裝備等方面,以期提出具有針對性的建議,推動中藥制藥行業的發展。
《中醫藥發展戰略規劃綱要(2016—2030 年)》提出“到2030 年��,中醫藥工業智能化水平邁上新臺階”的發展目標��,并將“促進中藥工業轉型升級����,推進中藥工業數字化���、網絡化����、智能化建設����,加強技術集成和工藝創新,提升中藥裝備制造水平”列為重要任務�。然而�,目前我國中藥行業生產工藝水平與國際領先技術仍然有較大差距�,中藥制藥裝備自動化程度較低,制造過程以落后的單元操作為主[1]����,數據顯示��,2014 年到2020 年,我國大健康產業整體營收規模超過7 萬億元[2]��,但現有整體技術水平仍停留在工業2.0 階段�,中藥高質量制造需要產業技術和裝備升級,中藥制藥行業面臨新的機遇和挑戰����。
連續制造(continuous manufacturing�����,CM)是指物料連續地投入并在工藝中完成轉換,同時加工后的物料被連續地從系統中移除�����,其作為一種先進的生產模式���,具有提高生產效率并降低成本的顯著優勢��,在汽車����、食品�、石油化工等行業已成功應用多年,但在制藥領域中的發展仍相對緩慢[3]���。2022年11 月16 日,國際人用藥品注冊技術協調會 (The International Council for Harmonisation of Technical Requirements for Pharmaceuticals for Human Use����,ICH)發布《Q13:原料藥與制劑的連續制造》指南的最終采納版本���,在該指南中���,連續制造范圍涉及生產過程中輸入物料的持續投料����,物料的持續轉化�����,以及輸出物料的同步去除����。目前��,我國中藥制劑生產仍以傳統批量制造模式為主��,與傳統模式相比,連續制造通過將各個單元生產環節組合為連續生產線���,借助過程分析技術(processanalytical technology,PAT)實現了許多優勢:僅需較小的生產場地����、生產靈活迅速、過程質量實時可控��、綠色智能化程度高�����,在經濟效益建模中成本相比傳統制造降低了55%[4]����。將連續制造技術與我國中藥制藥相結合����,不僅有助于中藥制藥行業發展轉型,更有利于我國從中藥大國邁向中藥強國。
雖然連續制造相比傳統制造存在諸多優點,見圖1,但全球范圍內應用連續制造技術生產商品化藥品的制藥企業仍較少����,國內外現已上市品種均為口服固體制劑�,多采取連續制造工藝與批次生產組合的“單元連續”或“半連續”方式進行生產����,與其他類型的制劑(例如液體、注射劑等)相比,固體口服制劑的生產過程更容易實現自動化和數字化控制����,物理和化學特性相對穩定并具有良好的耐儲存性能�,實現難度也更小�。
圖1 連續制造與傳統制造模式對比
1、連續制造發展概況
制造業實行連續制造可以追溯到工業革命時期,隨著現代科技發展,石油化工�����、制漿造紙��、食品烹飪等行業應用連續制造技術已較為常見���,制藥行業由于法規監管的特殊性及對藥品質量的嚴格要求,新技術�、新裝備的使用仍然較為緩慢�,但研究人員對于連續制造的探索從未停止�。
美國一直以來積極探索CM 在制藥中的應用���,將藥品連續生產認定為國家重點技術���,美國食品藥品監督管理局(FDA)將原料藥與藥品的連續制造列為公認的新興技術名單[5]�����,2016 年美國國會通過法案授權衛生與公眾服務部部長可向高等教育機構和非營利組織撥款,以研究和建議改進藥品和生物制品的連續生產過程以及類似的創新監測和控制技術[6]。CM 被認為接近于FDA 在2004 年發表的《藥品制造的創新和持續改進》[7]中描述的藥品制造“理想狀態”,貫徹了FDA 一直倡導的質量源于設計(quality by design�����,QbD)理念����。為幫助實施創新制藥技術,FDA 創建了新興技術團隊(emerging technology team,ETT)和生物制品評價與研究中心先進技術小組(CBER advanced technology team�,CATT)����,2018 年美國藥典委員會(US Pharmacopeia���,USP)發布《藥品連續生產的USP 視角》���,內容涉及CM 中的術語和定義�、批量定義、控制策略、風險管理����、PAT、監管預期等方面�����。同時其他發達國家和地區也成立了專注藥品制造現代化����、關注連續制造的產學研聯盟,例如藥品連續制造技術知識中心(美國)�����、結構化有機顆粒系統工程研究中心(美國)��、諾華-麻省理工學院連續制造研究中心(美國)��、連續制造和先進結晶中心(英國)、合成和固態制藥中心(愛爾蘭)�、制藥工程研究中心(奧地利)���。
我國積極投入CM 的研究與實踐中����,2021 年10 月�����,國家藥品監督管理局藥品審評中心公開向社會征求ICH 指導原則《Q13:原料藥和制劑的連續制造》意見[8]�����,并于2023 年3 月20 日發布《化藥口服固體制劑連續制造技術指導原則(試行)》[9]使得該進程向前更進一步,國內暫無中藥連續制造相關指導原則與品種審批�����,相關政策亟待建設完善�����。目前批準的連續化生產品種多為單一制劑產品。
目前,全球已有12 款使用CM 生產的藥物獲批,見表1��,FDA2022 年審計表明�,與傳統批處理方式相比���,CM 藥品評審時間平均快9 個月�,批準和上市時間較短�����,這意味著收益的增多和快速占領市場[10]��。其劑型與生產工藝集中在口服固體制劑產品,這體現了連續制造在口服固體制劑中的應用潛力�。
表1近年來使用連續工藝生產的企業與獲批藥物
2��、中藥制造模式
中藥是中醫藥事業傳承和發展的重要載體,升級中藥制造模式����、提升中藥生產效能對于推動中藥產業高質量發展至關重要��。隨著我國新版《藥品管理法》于2019 年頒布實施,國家大力推動完善中藥全過程質量控制體系����,構建中藥全過程質量追溯體系�����,一方面遵循以臨床價值為導向的原則��,另一方面強調重視“QbD”“全過程質量控制”等理念�,指導中藥生產企業更加有效地控制藥品質量��。
2.1 中藥制劑生產過程管理
隨著國內疫情政策的調整�����,藥品的可及性問題突出,依賴傳統設備的生產模式正暴露出越來越多的問題,例如設備性能發揮較為依賴員工���;關鍵設備容量大小桎梏生產批量;提升產量依賴人員加班加點。目前我國中藥制劑的主要生產模式為批次間斷生產,即通過單元式設備���,在完成每一單元生產步驟后由操作人員對中間品進行離線檢驗,期間物料暫存于設備內或暫存間,結果合格后放行至下一環節����,重復過程直至形成最終產品��,通常耗時1 周以上,不僅時間漫長���,繁瑣重復的過程也帶來了質量管理風險隱患,在CM 中,可通過4 種主要方式定義生產批量:①輸出物料量��;②輸入物料量����;③規定的質量流量下的運行時間;④基于CM 工藝特征的科學合理方法[8],企業可通過運行時間定義批次和批量使中試至商業化過程變得簡單�,使用連續化設備自動轉移物料縮短供應鏈����,通過改變設備運行時間��、增加質量流量或增加設備等方式來增加產量,通過停留時間分布(residence time distribution����,RTD)確定分流和收集時間����,并可用于追溯物料��,助力中藥生產的全過程質量管理�����。
2.2 中藥制劑產品質量管理
中藥全過程質量控制強調從藥材源頭入手,傳統生產過程常年對于不同批次飲片使用相同的工藝參數進行生產,中間品檢驗依賴水分�、密度等單一指標��,對于多組分��、多靶點的中藥制劑來說,難以有效地在過程中發現質量風險隱患,從而過于依賴成品檢驗確定制劑質量好壞,在使用隨機化控制試驗設計的中藥研發方案中����,多重視考察工藝參數的變化�����,較少考慮關鍵物料屬性與關鍵工藝參數(critical process parameters, CPPs),關鍵質量屬性(critical quality attributes, CQAs)之間的交互[11]。使用CM 可以大幅改善這種局面�,通過在關鍵工藝點使用PAT 監測生產過程中的CQAs����,利用反饋和前饋回路系統自主控制CPPs�����,以保證過程和最終的產品CQAs 在規定范圍內,管理者在生產過程中能夠實時掌握過程數據����,系統的自主決策減少了人工干預�,并可利用積累的生產數據持續優化工藝�,改善中藥制劑質量。
2.3 建立符合中藥特點的連續制造技術體系
與化學藥品多采用規定固定工藝參數的模式不同��,中藥原料的質量波動性較大��,生產中的關鍵工藝參數和質量屬性應保持在經優化驗證的設計空間內��,并非穩定不變。中藥復方工藝對物料等輸入性因素過度嚴格控制可能會造成適得其反的結果[12]�,中藥連續制造技術體系需要考慮中藥制劑的特點��,包括中藥的復雜組成、藥效成分的多樣性和易揮發性等��。同時對投入物料的控制�、過程檢測、物料的分離和收集能力�����、數據處理和分析能力�����、穩定性能力具有一定要求�����,因此,建立符合中藥特點的連續制造技術體系可從以下部分考慮:
①連續化改造����,特別是中藥制藥裝備自動化與單元智能化設備程度低的環節(如藥材前處理)重點突破��、積累關鍵工序的共性技術方法(如算法���、建模���、PAT 等)����。
②良好的控制策略,解決在線檢測技術沒有和工藝�、設備有效結合的現實問題��,實現制造過程中的產品可追溯性、開發中藥連續制造其中的一個關鍵就在于對過程動力學的理解[13]�,常見的方法是通過各個工序或整體生產系統的RTD 來描述物料從進入到離開所需的時間分布情況�,該函數可以用數學模型進行建模和預測��,并作為取樣和追溯物料的依據��,這對于設計連續生產工藝的控制策略至關重要。
③質量預測技術�,通過建立實時數據庫并結合歷史數據庫和知識庫(如中藥物料屬性數據庫)進行實時過程監控����、診斷和優化�����,并對不斷更新和積累的質量大數據進行重復利用和深度挖掘�,實現質量追溯、工藝優化���、設備運行優化等任務,最終實現提前預測質量變化趨勢����,變被動防御為主動預防����。
3���、連續制造技術
QbD 理念的貫徹實施離不開良好的控制策略[14]��,越來越多的企業借助連續制造關鍵技術實現良好的控制策略,進行高效����、精確和可持續的生產�����。
3.1 過程分析技術
過程分析技術被定義[15]為“一個在加工過程中通過及時測量原材料、加工材料和工藝的關鍵質量和性能屬性來設計,分析和控制制造的系統�,目的是確保最終產品質量”���。主要包括過程認知��、過程檢測、過程建模、過程控制����、持續改進5 個關鍵技術步驟[16]���,通過使用光譜傳感器和化學計量模型等工具可以實時監控產品質量�����,使產品符合法規要求。將PAT 納入工藝監控的控制策略中,通過整合集成各環節數據信息實現對生產過程自動化控制,從而有效保證藥品質量穩定。強大的PAT 在線數據和預測性工藝模型�,結合基于QbD 的工藝設計��,可以實現過程控制的自動化,并實現實時放行檢測,而不是靠生產結束后的離線檢測����。產品的上市時間將會更短,批次問題率將更低�,生產率可提高約20%[17]�����。
現場可編程門陣列作為PAT 的硬件基礎,在數據多通道采集和并行處理領域正發揮快速數據處理�����、高性能����、低功耗等技術優勢,在諸多領域已被廣泛使用�����,利用其創建實時放行檢測是解決中藥制藥過程中參數混雜問題的重要手段[18]�����,在軟件系統層面�,有CAMO����、Umetrics、Siemens 等知名公司先后推出PAT 軟件系統����。由于在端到端連續制造過程中需要監控多個過程�,PAT 及其實時過程監控功能在確保最終產品質量方面發揮著重要作用。MIYAI Y 等 [19]討論了在CM 上實施PAT 的策略與試驗方法,在合成裝置上使用在線傅里葉變換紅外和拉曼光譜實時監測環丙沙星中間體和藥物活性成分濃度�,通過在線模型處理軟件和PAT 數據收集和管理軟件實現了中間體和產物濃度的實時預測����。在水分含量在線監測方面�����,王晴等[20]利用在線近紅外光譜技術,采集樣本數據進行建模�����,實現了用于生產規模的桂枝茯苓膠囊流化床干燥過程水分含量在線監測���。
3.2 信息化智能化技術
制造業的轉型需要“智能化”賦能�,需要信息技術的加持,將生產過程中數據作為基礎�����,發揮大數據優勢��, 將連續制造與人工智能結合��, 目前制藥行業應用較為廣泛的有生產執行管理系統 (manufacturing execution system,MES)�����、PDM 研發過程數據集成系統����、LIMS 實驗信息管理系統等。
數據采集與監視控制系統(supervisory control and data acquisition����,SCADA)是結合了軟件和硬件的自動化控制系統�,可將工藝參數�����、進料和再加工物料屬性以及最終產品質量屬性的測量與工藝動態模型相結合,使用這些數據來控制和優化工藝�����,從而支持實時放行檢測�,該系統廣泛用于石化、自來水輸送系統等一系列工業過程中,可實現持續監控過程、實時控制���、自動化和保護、遠程控制和操作功能。多元統計工藝控制 (multivariate statistical process control, MSPC) 可分析具有潛在相關變量的復雜工藝數據�����,用于確定工藝中的可變性是否隨時間穩定�,檢測工藝中的異常事件。近年來,陸續有新適用于CM 信息化智能化系統涌現����,涉及開發���、生產����、維護等方面�,如薛啟隆等[21]完成了以中藥真空帶式干燥工藝為例的工藝自主決策模型的構建與驗證,實現了工藝參數組合自主優化策略發現和最優過程控制路徑規劃�。提高產品質量一致性���,降低生產成本����,提升企業效益����。余雅婷等[22]利用人工智能中的專家系統,輸入人類專家的專業知識和經驗,用計算機模擬人類專家的思維過程解決藥品生產領域問題���,于佳琦等[23]以QbD 為基礎,將智能工具納入生產系統中,提出由連續制造����、信息集成����、智能模擬和智慧應用組成的中藥智能制造關鍵技術體系���。蕭偉[24]基于目前的生產控制設備和工藝基礎���,開發來了可用于中藥連續制造的過程知識系統�,可根據生產數據的持續累計,通過AI 算法計算最佳調控策略以實現產品質量的持續優化。GANESH S 等[25]介紹了一種基于狀態的口服固體藥物產品維護系統,該系統可主動監測可能導致系統故障或性能出現偏差的情況并闡述了實現該系統所需的系統架構����,這對于管理藥品生命周期中的過程風險至關重要���。國內的浙江海正藥業股份有限公司也正積極推進智能制造信息化系統建設���,包括MES 系統�、SCADA 系統����、BI 建設等。MES 系統能自動生成符合《藥品生產質量管理規范(2010 年修訂)》(good manufacturing practice,GMP)和FDA要求的電子批記錄,將制藥生產各環節的人員��、設備�、物料�、環境、規程進行有機結合�,實現整個生產過程的規范化��、電子化、可視化���,確保生產數據的可靠性和性。SCADA 系統提供數據監控一體化平臺��,實現全廠生產設備/系統運行監控�����。BI 建設使任務操作��、設備工況可視化管理,實時反映生產任務完成情況����,實時監控設備參數��,異常報警。
3.3 虛擬仿真技術
通過VR 虛擬現實���、3D 仿真技術等虛擬仿真技術模擬現實環境,將一些不可視的結構和原理可視化�����,進行信息化與工業化的融合��,并通過建立三維仿真模型進行虛擬現實的模擬[26]�����,通過在預設好的軟件中更改條件可直觀了解工序對產品的影響,該技術具有降低成本���、高效安全��、易于拓展的特點�����,對連續制造中可能涉及的工藝�����、設備改造、人員培訓等方面可起到重要作用����,其包括仿真目標定義�、基礎數據收集�����、仿真建模��、仿真分析、仿真優化5 個主要步驟�,德國GEA 公司使用VR 展示連續固體制劑生產的運作方式���,使每個員工可在設備安裝之前接受培訓����,從典型的9 個月入職時間縮短到僅3 個月�,節省了66%的時間[27]。于洋通過采用Aspen Plus 軟件對甘草多糖水溶液的濃縮工段進行仿真模擬����,使用機械蒸汽壓縮技術對傳統濃縮工藝進行改造[28]。通過對現階段工藝仿真模擬、改造工藝和成本節約率的模擬仿真�����,得到改造后的最佳操作工藝��。DAMMACCO L 等[29]將物理世界與虛擬世界高水平連接��,提出使用基于虛擬現實技術作為解決復雜制造系統設計問題的設計方法。JELSCHM 等[30]將模型預測控制(model predictive control,MPC)從石油化工行業推廣至藥物連續制造,MPC 是一類控制算法并依賴于過程模型,能在每個單位的已知時間點預測未來輸出物料的質量,在仿真研究中����,可在考慮干擾和不確定因素的情況下自動采取糾正措施�,使產品質量向期望值方向移動���。
4��、連續制造裝備
未來連續制造技術應用于中藥生產����,從裝備開發的角度主要有2 個路徑:一是串聯現有最先進的單元制造設備����,重點解決和突破單元設備之間的物料定量輸送問題;二是開發全新的整體連續制造設備,這需要有全新的設備開發思路,有些要突破傳統的工藝單元制造設備的理念,從單元設備開始就實現物料的連續化生產�。
4.1 單元裝備的集成創新
將現有生產設備進行串聯改造�����,可實現部分連續的生產模式,在該模式下,部分單元操作為批生產模式���,其他2 個或2 個以上單元操作直接相連為連續模式。考慮到連續制造的投入較大��,目前應用該模式較為廣泛�。
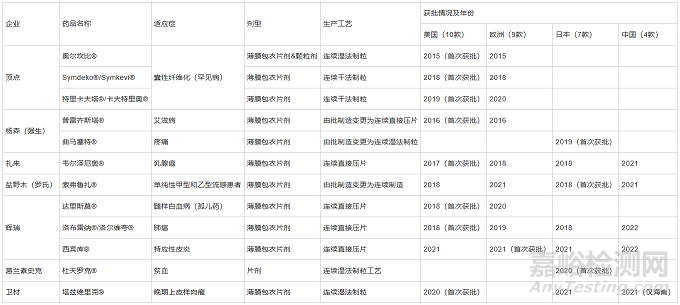
在中藥的前處理環節��,中藥傳統提取下開蓋的出料方式與雙效濃縮方式存在藥材利用率低�、出料密封圈易老化��、現場環境差���、生產環境溫度高���、濕度大等問題�。華潤江中制藥集團使用自動喂料機�,采取“吊籃式循環提取”技術,見圖2A����,實現整條提取線無人化���,所有輸送設備可沖洗或擦洗�����,所有輸送線均帶有接水�、接渣的料槽����,使得工作環境得到極大改善,藥液經管道輸送至MVR 濃縮設備,降低能耗、減少污染物的排放�,實現低溫濃縮����。在制粒工序���,將制粒�����、干燥、整粒��、混合等功能整合密閉���,采用密閉輸送及齊墻的方式��,使用PAT 等手段掌握生產過程進而主動控制產品關鍵質量特征�����,更加符合EHS 管理體系,設備之間可獨立操作也可實現批次的連續生產��,現有設備如宜春萬申制藥機械有限公司的高密閉連續制粒線���,見圖2B����,OEB4&OEB5 抗腫瘤制粒線。在中藥丸劑的連續化干燥工序�����,江西赫柏康華制藥設備有限公司的中藥丸劑連續干燥系統將濕物料自智能離心振動干燥機頂部進料口自動進入����,在重力與振動激振力作用下物料做規律性離心運動,同時與自下而上的熱空氣進行逆流的充分接觸��,濕熱空氣經除塵后從排風口排出����,而干燥完成的物料自干燥塔底部出料口自動排出�,多層逆流干燥降低能耗,連續化的自動進、出料在增高產量的同時避免人員接觸物料造成污染。
圖2 吊籃式循環提取示意圖(A)�、高密閉連續制粒線(B)�����、中藥丸劑連續干燥系統(C)外觀示意圖
4.2 新型連續制造裝備
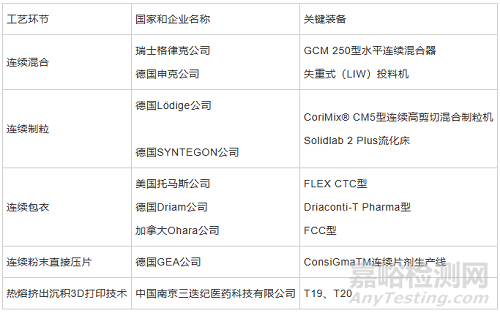
設計開發新型連續制藥裝備,可實現部分連續甚至是全過程連續的生產模式���。繼GEA Pharma Systems 公司在全球率先推出制藥連續制造設備后,設備制造商紛紛跟進����,L.B. Bohle 公司推出全連續流化床干燥并建立技術中心����,將研發重點從批量生產轉移到了連續制造����,Glatt����、Fette 等其他設備供應商也在連續制造領域推出了相應的產品[31]��,在平臺與系統方面��,GLATT 推出了Modcos 連續直接壓片系統、L.B. Bohle 推出了QbCon®連續生產系統�、SYNTEGON 推出了連續化生產平臺Xelum����,GEA 推出了ConsiGma® 4.0 連續制造平臺�����,一些固體制劑環節的新型連續制造裝備見表2。
表2固體制劑環節的新型連續制造裝備
在中藥領域���,除了連續逆流提取、連續濃縮��、連續醇沉等單元的物料連續化生產����,也可考慮單一設備多功能化。以固體制劑中常見的片劑為例,其連續化生產流程見圖3��。
圖3 連續化生產片劑制造流程
4.3 關鍵核心部件
傳感器為連續制造中關鍵核心部件���,其適用于組合式連續制造和獨立開發連續制造2 種模式����,高精度傳感器目前多依賴于國外進口,應用較多的PAT 供應商有Bruker、Vaivi、Thermo、Kaiser���、Cobalt 等公司,連續制造常用傳感器見表3。傳感器的數據被用作過程控制策略的一部分�,可用于改變參數確保CQAS 保持在可接受的范圍內�����,傳感器的放置位置、探針深度和清潔采樣面積、取樣量和采樣頻率等都需要經過充分的驗證��,同時在傳感器發生故障時的預防與糾正措施�、傳感器的校準和維護等策略也需充分考慮,傳感器的采樣頻率是實現實時放行檢測的關鍵,它需要足夠快以檢測瞬時變化��,并能通過收集足夠的測量數據進行趨勢分析來檢測過程漂移��,從而根據可靠的統計數據對批次的質量進行分析�。
表3連續制造常用傳感器
飼料器作為生產過程中的整個物料起始�����,是產品性能變異的第一來源,其性能在CM 中非常關鍵�,需滿足向每個單元輸送物料���,維持產品的處方量并穩態運行�,達到隨著時間的推移能夠持續提供準確數量的物料����,確保過程的穩定性,目前常用設備有失重模式飼料器(loss-in-weight feeders�����,LIW)�����,其進料速率由螺桿的轉速控制����,LIW 控制器根據對失重速率的監控來調整進料器速度以獲得所需的設定值����。
在中藥制劑過程中����,前處理工序是生產過程的第一道工序����,中藥材的揀選、清洗、炮制等相關操作均在前處理工序完成���。前處理過程的處理結果的好壞����,直接影響后工序的提取效果。吳志生團隊對于紅花染色和摻假問題���,結合計算機視覺和近紅外,實現了紅花的快速無損分析����,分析方法快速可靠�,為市場紅花質量分類標準的制定提供重要參考[32]��。通過基于機器視覺的中藥藥材自動篩選裝置��,在智能識別系統的基礎上,可搭建紅參自動化分選平臺�����,改變了傳統生產方式�,等級分選能力極大提高,增加特等品和一等品的檢出量[33]�����。
5�、中藥連續制造的挑戰
5.1 政策與監管方面
在監管方面,我國在注冊審評����、核查檢驗方面實施連續制造存在經驗不足�����、專業領域人員缺乏等問題,與國際其他監管機構仍有一定的差距���,相關監管配套文件如涉及連續制造現場檢查�����、上市后變更等指導文件仍待發布����,如何將現行GMP 與連續制造銜接值得思考���。在效益方面����,中藥企業存在連續制造初期投入大、老設備改造難度大、涉及工藝變更周期長、數據服務商可靠性不足等問題,結合近年來我國中藥集采的推進����,企業對投入后的利潤產出存在一定擔憂��,應提倡業界合作,鼓勵藥廠在研發或建設階段申請監管提前介入,廣泛聽取意見組織開展實地調研交流�,深化對先進技術的理解與掌握�����。
5.2 關鍵技術與裝備
中藥產品種類豐富,不同產地�����、不同季節的中藥表現出的特征圖譜可能不一致,各類劑型工藝差異較大�����,加大了中藥作為連續化控制的難度�,在硬件層面����,我國目前的中藥制劑設備整體缺乏創新,普遍相互模仿重復。符合中藥固體制劑生產特點的設備仍然不足,一些企業將化藥設備稍加改進便簡單照搬�,導致了工藝與設備的適宜性問題�����;設備迭代緩慢;能實現在線數據采集、導入、處理的自動控制設備較少。在軟件層面�����,國家政策的支持與市場規范管理為中藥智能化��、自動化升級提供了保障����,但在中藥固體制劑領域應用人工智能技術���、自動化技術��、產業數字化的范例仍不多�����,共性技術開發不足,技術關注點主要集中在下游生產階段,對于上游的藥材種植管理關注不夠。國內大部分企業對中藥工藝質量規律理解還不充分�����,對于智能化信息化的理解和數據的利用有待深入�����,各個生產模塊總設備接口不同,未建立設備通信的標準接口協議���,企業手握大量生產數據但各個環節之間的數據缺乏流動與分析,當前連續制造的啟動階段物料損耗仍較大�,中藥浸膏類在線檢測器放置位置的選擇和探頭易污染的問題仍需研究解決����。
5.3 新工科制藥工程類人才匱乏
中藥口服制劑連續制造技術的技術人員培養是一個重要課題����,CM 是一種新型的生產工藝,本土制藥企業對連續制造工藝具有一定的關注度���,但認識不夠深入,動力不足�,在專業人才����、技術儲備和儀器設備開發等方面存在實際困難�����,較為可行的方案是在原有裝備的基礎上進行一定的技術改造�。企業人員面對傳統與智能并行的制造雙通道模式工作量將增加���,從管理層到一線員工都需要加強培訓�,CM 需要藥學、工程���、數學、計算機等多領域學科知識專家支持配合��,但現有技術人員多為純藥學研究或純軟件開發���,缺少復合交叉型人才���,高校也未設置相關藥品智能制造專業和課程�。下一步可考慮高校開設相關課程或與企業進行聯合培養,加強技術人員的在職培訓���,使單一的藥學人才轉化為復合型人才,加速中藥智能制造產業化。
6�����、結語
《醫藥工業發展規劃指南》提出引導企業推動“制造執行系統”“過程分析技術(PAT)”在生產過程中的應用�����,整合集成各環節數據信息實現對生產過程自動化控制�,有效保證藥品質量穩定����。2019 年新版《藥品管理法》規定,國家鼓勵運用現代科學技術和傳統中藥研究方法開展中藥科學技術和藥物研究����,面對突發疫情�,連續制造技術可以有效縮短供應鏈�,保證藥物的可及性和有效性。
對于現有批次制造的企業��,目前仍然存在設備利用���、專業人才缺口以及前期投資較大等挑戰��。未來制造現場所需人員將大幅減少, 但對技術人員要求更高���。先進裝備不能解決目前制藥行業的所有問題,操作人員需要在項目前期跟進,加強對制藥工藝過程和產品質量設計的理解�,以便靈活應對生產中可能的出現的狀況�����。我國連續制造發展尚在起步階段,需要更多不同行業的專家參與進來,無論是企業還是監管機構����,在CM 這一新技術的實踐上�,都需要化學工程��、處方開發����、建模仿真���、流程控制����,以及傳統藥學等領域的多學科復合型人才共同參與,以加快我國中藥連續制造技術和裝備的發展,推進我國中藥產業高質量高效益發展�。
參考文獻
[1] 楊明����,伍振峰�����,王芳�����,等.中藥制藥實現綠色�����,智能制造的策略與建議[J].中國醫藥工業雜志�����,2016�,47(9):1205.
[2] 艾媒咨詢. 2021 全球與中國大健康產業運行大數據及決策分析報告[EB/OL] . ( 2021-04-30 ) [2022-12-21] . https ://baijiahao.baidu.com/s?id=1698447533452464968&wfr=spider&for=pc.
[3] PEDERSEN T, KARTTUNEN A P, KORHONEN O, et al. Determination of residence time distribution in a continuous powder mixing process with supervised and unsupervised modeling of in -line near infrared (NIR) spectroscopic data[J]. J Pharm Sci, 2021, 110(3): 1259.
[4] WALTHER J, GODAWAT R, HWANG C, et al. The business impact of an integrated continuous biomanufacturing platform for recombinant protein production[J]. J Biotechnol, 2015, 213: 3.
[5] FOOD AND DRUG ADMINISTRATION. Examples of Accepted Emerging Technologies[EB/OL]. (2022 -02-22)[2023-03-28].https://www.fda.gov/about-fda/center-drug-evaluation-and-research-cder/examples-accepted-emerging-technologies.
[6] CONGRESS OF THE UNITED STATES. Senate and house of representatives of the united states of America in congress[EB/OL]. (2016-11-13)[2023-03-28]. https://www.gpo.gov/fdsys/pkg/PLAW-114publ255/pdf/PLAW-114publ255.pdf.
[7] Food And Drug Administration. Innovation and continuous improvement in pharma ceutical manufacturing[EB/OL]. (2004-01-01)[2023-03-28].https://www.pharmaceuticalonline.com/doc/innovation-and-continuous-improvement-in-phar-0004.
[8] 國家藥品監督管理局藥品審評中心.關于公開征求ICH 指導原則《013:原料藥和制劑的連續制造》意見的通知[EB/OL].(2021-10-18) [2023-03-28]. https://www.cde.org.cn/main/news/viewInfoCommon/d30747763265e07fae058d565519070.
[9] 國家藥品監督管理局藥品審評中心. 國家藥監局藥審中心關于發布《化藥口服固體制劑連續制造技術指導原則(試行)》的通告( 2023 年第19 號) [EB/OL] . ( 2022-03-20 ) [2023-03-28].https ://www.cde.org.cn/main/news/viewInfoCommon/fcd2eeca1882b5782411bf00fe21e123
[10] FISHER A C, LIU W, SCHICK A, et al. An audit of pharmaceutical continuous manufacturing regulatory submissions and outcomes in the US[J]. Int J Pharm, 2022, 622: 121778.
[11] 徐冰�����, 史新元��, 羅贛,等. 中藥工業大數據關鍵技術與應用[J]. 中國中藥雜志, 2020��,45(2):22.
[12] 伍振峰����,林瑞華,王學成,等.基于中藥制藥工程質量觀的質量控制模式研究[J].中國中藥雜志,2022���,47(1):271.
[13] Food And Drug Administration. Quality considerations for continuous manufacturing[S]. New York: Food and Drug Administration, 2019.
[14] LEE S L, O’CONNOR T F, YANG X, et al. Modernizing pharmaceutical manufacturing: from batch to continu ous production[J]. J Pharm Innov, 2015, 10(3): 191.
[15] AFNAN A. PAT-A framework for innovative pharmaceutical development, manufacturing and quality assurance[R]. FDA/RPSGB Guidance Workshop, 2004.
[16] 熊皓舒,張嬙,章順楠����,等.中藥制藥過程分析技術方法學研究與應用進展[J].中國中藥雜志����,2023�,48(1):22.
[17] SCHMIDT A, HELGERS H, LOHMANN L J, et al. Process analytical technology as key‐enabler for digital twins in continuous biomanufacturing[J]. J Chem Technol Biotechnol, 2022, 97(9): 2336.
[18] 李小莉,薛啟隆���,苗坤宏�����,等.FPGA 技術在中藥智能制藥中的應用探討[J].中草藥�����,2023,54(1):283.
[19] MIYAI Y, FORMOSA A, ARMSTRONG C, et al. PAT implementation on a mobile continuous pharmaceutical manufacturing system: real -time process monitoring with in-line FTIR and raman spectroscopy[J]. Org Process Res Dev, 2021, 25(12): 2707.
[20] 王晴�����, 徐芳芳����, 張欣, 等. 在線近紅外光譜監測桂枝茯苓膠囊流化床干燥過程水分的方法研究[J].中草藥�����,2019�����, 50( 22):5429.
[21] 薛啟隆���,苗坤宏����,于洋����,等.基于深度強化學習的中藥制藥過程自主優化決策方法研究[J].中國中藥雜志��,2023���,48(2):562.
[22] 余雅婷����,趙立杰���,杜若飛�����,等.淺析專家系統在實現中藥智能制造中的作用與地位[J].世界科學技術(中醫藥現代化)���,2020���,22(3):843.
[23] 于佳琦��,徐冰����,姚璐�����,等.中藥質量源于設計方法和應用:智能制造[J].世界中醫藥����,2018�,13(3):574.
[24] 蕭偉�����,劉雪松�,凌婭��,等. 一種中藥生產過程知識系統[P]. CN107578104A��, 2018-01-12.
[25] GANESH S, SU Q, PEPKA N, et al. Design of condition -based maintenance framework for process operations management in pharmaceutical continuous manufacturing[J]. Int J Pharm, 2020, 587: 119621.
[26] 曹婷婷,王耘.中藥智能制造理論模型的構建[J].中國中藥雜志, 2019�,44(14):3123.
[27] GEA. Improving the ConsiGma 4.0 customer experience with virtual reality[EB/OL]. (2020 -08-25) [2023-03-28].https://www.gea.com/en/stories/improving -consigma-4-customer-experience-virtual-reality.jsp.
[28] 于洋��,司夢蘭,高雪地,等.MVR 技術在中藥濃縮過程中節能優化的仿真研究[J].中國醫藥工業雜志,2017���,48(11):1610.
[29] DAMMACCO L, CARLI R, LAZAZZERA V, et al. Designing complex manufacturing systems by virtual reality: a novel approach and its application to the virtual commissioning of a production line[J]. Comput Ind, 2022, 143: 103761.
[30] JELSCH M, ROGGO Y, KLEINEBUDDE P, et al. Model predictive control in pharmaceutical continuous manufacturing: a review from a user’s perspective[J]. Eur J Pharm Biopharm, 2021, 159: 137.
[31] PORTIER C, VERVAET C, VANHOORNE V. Continuous twin screw granulation: a review of recent progress and opportunities in formulation and equipment design[J]. Pharmaceutics, 2021, 13(5): 668.
[32] LIN L, XU M, MA L, et al. A rapid analysis method of safflower ( Carthamus tinctorius L.) using combination of computer vision and near -infrared[J]. Spectrochim Acta A Mol Biomol Spectrosc, 2020, 236: 118360.
[33] 李正,于洋,趙靜��,等.一種基于機器視覺中藥藥材自動篩選裝置[P].CN109499919A��,2019-03-22.