骨感染是由于骨組織感染化膿性細菌而導致的炎癥性疾病,目前治療手段常為手術清創聯合抗生素使用,但不具有靶向功能的給藥系統會帶來全身副作用,最終導致局部治療不理想或引起全身毒性。
近期,西南交通大學醫學院翁杰教授和陳星羽副研究員在藥學領域期刊Journal of Controlled Release上發表了題為“Hexapeptide decorated β-cyclodextrin delivery system for targeted therapy of bone infection” 的研究性論文,報道了一種新型骨靶向給藥系統Asp6-β-CD@NFX,負載疏水性藥物諾氟沙星后,能有效提高其溶解度和生物利用度,并有效解決骨感染的局部治療問題(圖 1)。
圖1 Asp6-β-CD@NFX靶向羥基磷灰石(HA)治療骨感染示意圖。
來源于骨橋蛋白的天冬氨酸六肽(Asp6)具有結合羥基磷灰石特性,將Asp6和聚乙二醇(PEG)對β-環糊精載體改性(Asp6-β-CD)以獲得具有骨靶向特性的給藥系統。將疏水的抗菌藥物諾氟沙星(NFX)載入Asp6-β-CD(Asp6-β-CD@NFX)用于靶向骨組織治療骨感染。基于Asp6-β-CD的水溶性增強,NFX的抗菌能力得到了提升。體外研究了Asp6-β-CD@NFX給藥系統對大腸桿菌(E. coli)和金黃色葡萄球菌(S. aureus)的抗菌活性(圖2)。
圖2. A-B)Asp6-β-CD@NFX對大腸桿菌的殺菌率和MIC值; C-D)Asp6-β-CD@NFX對金黃色葡萄球菌的殺菌率和MIC值;E-F)不同樣品對大腸桿菌和金黃色葡萄球菌的抑菌圈及死活染情況;G-H)不同樣品結合HA片后對大腸桿菌和金黃色葡萄球菌的抑菌圈及SEM圖像。
通過體外(羥基磷灰石片)和體內(裸鼠)實驗分別驗證了Asp6-β-CD的骨靶向特性(圖3,圖4 A&B),研究表明與未改性的β-CD相比,Asp6-β-CD的骨靶向能力提升了10倍。此外,建立了大鼠骨感染模型,研究了Asp6-β-CD@NFX治療骨髓炎促進骨組織修復的作用(圖4C-E,圖5)。
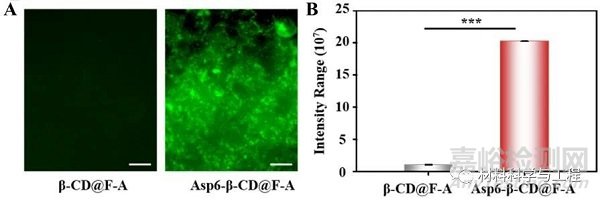
圖3. β-CD@F-A與 Asp6-β-CD@F-A結合HA片后的熒光圖像及熒光定量圖。
圖4. A-B)對裸鼠注射 β-CD@F-A和Asp6-β-CD@F-A 30分鐘后的IVIS圖像,及其對心臟、肝臟、脾臟、肺、腎臟和股骨的富集情況;C-E)大鼠骨髓炎模型及治療示意圖,治療不同時間后IL-6、IL-1β、TNF-α的濃度及HE染色(箭頭顯示炎癥細胞)。
圖5. A) 不同時間治療后骨組織的Masson染色圖;B–D) 注射28天后重建股骨遠端缺損的Micro-CT三維圖像重建及定量分析。
綜上所述,該骨靶向給藥系統Asp6-β-CD能夠特異性的靶向骨組織、提高疏水藥物的水溶性和有效性,可廣泛應用于骨感染等臨床骨相關疾病的精準靶向治療。