現階段,難溶性藥物(BCSⅡ和BCSⅣ類)的開發越來越多,提高藥物的溶解度是制劑研發中的一個關鍵問題,增加難溶性藥物溶解度的方法有很多種,例如成鹽、合成水溶性前藥、微粉化、共研末、固體分散體技術、納米晶技術、自乳化等等。其中成鹽是最常見的解決方案,能夠有效的提高藥物的溶出度和溶解速率。但是由于所成的鹽常為強酸弱堿鹽或強堿弱酸鹽,因此很容易發生鹽歧化,且不容易發現,可能會引起產品的質量問題。例如被研究用于神經退行性疾病的馬某來酸鹽片劑,在早期臨床研究中,沒有跡象表明存在不穩定的情況,但是在后期臨床試驗中,雖然相關物質水平未增加,但是片劑的效價隨時間顯著降低,嚴重影響了質量問題。因此,本文將從鹽歧化現象介紹、鹽歧化發生的原因及減少鹽歧化發生的策略3個方面展開討論。
一、鹽歧化現象
鹽歧化通俗的講,就是高溶解度的鹽解離并回復為低溶解度非離子形式的過程。由于常規的含量檢測和有關物質檢測常常難以發現鹽歧化的發生,導致鹽歧化成為影響鹽型化合物藥物質量的一個重要因素。
鹽歧化發生后,對制劑的主要影響有:
①影響效價:一般而言,鹽型的溶出度大于游離堿,發生鹽歧化后游離堿比重增大,導致溶出度降低,也有可能導致生物利用度降低。
②批次間差異大:制劑中的鹽會不同程度的轉變為游離態,生產、處理、以及包裝的方法不足以保證其純度、質量、穩定性和生物利用度等。可能會導致生物利用低、批次之間差異大等問題。例如,FDA2009年批準上市的普拉格雷鹽酸鹽,片劑中的游離態含量可達42-87%,且批次間差異大、生物利用度的差異。
③改變輔料功能:鹽的歧化可能會改變輔料功能,從而影響藥物溶出。例如地拉夫定甲磺酸鹽,鹽歧化產生的游離甲磺酸會與交聯羧甲基纖維素鈉反應,不僅降低了溶出度,還因為消耗了崩解劑交聯羧甲基纖維素鈉而影響了崩解功能,導致該片劑在40°C/75% RH條件下存儲一周后,溶出度有明顯的降低。
④影響物理性質:鹽的歧化可能影響固體制劑的物理完整性。如一些藥物的游離堿在室溫下為油或蠟狀。發生鹽歧化轉變為游離堿后,部分變為蠟狀,可能會影響片劑的硬度和崩解時間。
二、鹽歧化發生的原因
純的API由于自身的穩定性和外界環境的影響,可能發生解離。在制劑的過程中,往往會涉及到一些條件相對劇烈的單元操作,如濕法制粒,干法制粒,干燥等,同時又有輔料的作用,鹽更可能發生歧化反應。鹽歧化發生的原因分為自身因素和環境因素(圖 1),自身因素是因化合物自身性質導致該化合物更易發生鹽歧化,是鹽歧化發生的根本因素。主要與①pKa、②pHmax、③鹽、游離堿溶解度的差異有關。環境因素主要包括輔料形成的pH微環境、水分、溫度、粒度和比表面積等,下面將以強堿弱酸鹽為例介紹這些因素是怎樣導致鹽歧化的。
圖1 鹽歧化發生的原因
1、自身因素
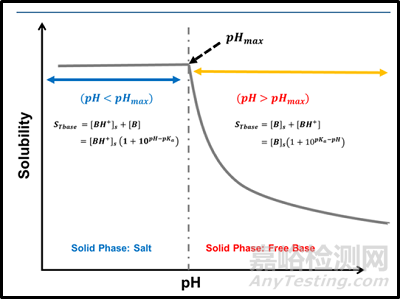
從弱堿鹽化合物溶解度隨pH的變化圖(圖 2)可以看出,隨著pH減小,游離堿向鹽轉化,溶解度逐漸升高,當達到某個pH值后,所有化合物分子都成鹽,此時溶解度達到最高,此時的pH即為pHmax。環境pH大于pHmax時,鹽將不成比例形成溶解度較低的游離堿,即發生鹽歧化。因此pHmax越大,越不容易發生鹽歧化,pHmax越小,越容易發生鹽歧化。
圖2 弱堿鹽化合物溶解度隨pH的變化圖
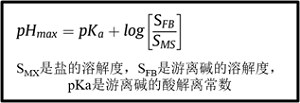
此外,(圖 3)為pHmax的計算公式,從公式可以看出,pHmax影響因素有兩個,一個是pKa一個是游離堿和鹽溶解度的比值。從公式我們還可以看出兩點,一是pHmax≤pKa,因此pKa越小,越容易發生鹽歧化。二是鹽、游離堿溶解度差異越大,pHmax越小,越容易發生鹽歧化,可以通過吉布斯自由能解釋。
圖3 pHmax的計算公式
(圖 4)是吉布斯自由能的公式,從公式我們可以看出,鹽和游離堿之間的溶解度差異較大的化合物的吉布斯自由能差異較大,由鹽轉為游離堿也更容易發生,也就是鹽歧化更容易發生。
圖4 吉布斯自由能公式
對于高鹽和低游離堿溶解度的化合物,吉布斯自由能差異更大。因此,在熱力學上,這些鹽更容易發生歧化。因此在選擇成鹽時,溶解度過高可能并不一定是一件好事。
對自身因素進行小結可以看出,影響化合物是否會發生鹽歧化最直接的自身因素就是pHmax,pKa和溶解度的差異,這些差異都可以通過pHmax來表現。
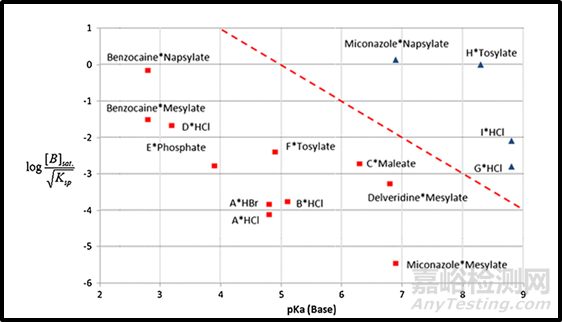
有學者(Merritt et al.,2013)繪制了一些研究化合物和已上市模型化合物的溶解度和pKa曲線(圖 5),并繪制了虛線以顯示比例失衡風險。邊界線以上的化合物未顯示任何歧化證據。預測pHmax較低的分子具有較高的歧化風險,也就是左下象限中這些pKa較低且游離堿和鹽溶解度差異較高的分子。即當pHmax較小時,更容易發生鹽歧化。
圖5 一些化合物的溶解度和pKa曲線
此外,由于pHmax與pKa密切相關,有學者綜述了203種市售化合物,將其活性成分的pKa與成鹽形式作圖(圖 6)。從圖中觀察到pKa小于4.6的弱堿性化合物沒有一款成鹽。作者得出結論,pKa小于5的堿性化合物更難形成鹽,或者說鹽不穩定的風險很大。此外作者還根據pKa值將弱堿性藥物分為三個區域。第一區(pKa 1-4)是弱堿歧化的高風險區,首選游離形式,第二區(pKa 4-8)需要評估弱堿鹽的歧化趨勢和生物利用度,第三區(pKa 8-10)成鹽對生物利用度的益處最小。
圖6 203種市售化合物的pKa與成鹽形式
2、環境因素
除了自身因素外,環境因素對鹽歧化的發生也產生了巨大的影響
(1)輔料
輔料影響的本質還是與pHmax有關。對于弱堿性藥物的鹽,輔料可使吸附水層的微環境pH值高于pHmax值,從而發生鹽歧化。
常見的三種導致鹽歧化的輔料分別是硬脂酸鎂、硬脂富馬酸鈉和交聯羧甲基纖維素鈉,他們共同的特點是具有質子受體羧酸基團,能夠爭奪鹽中的質子導致鹽歧化,一個例子是含有甲磺酸地拉韋啶和交聯羧甲基纖維素鈉以及其他輔料的片劑在40 ℃/75 %RH下儲存時,輔料的羧酸鈉與釋放的甲磺酸反應,形成羧酸,加快了鹽歧化的進程,從而加劇了鹽歧化。
(2)水分
影響鹽歧化的第二個環境因素就是水分,主要原因有兩個,①水可以作為溶劑,為化學反應提供平臺。②晶體固體上存在的薄水層也會促進表面遷移率,促進質子轉移從而加快歧化反應。
(3)溫度
溫度的影響有兩方面,①溫度可以影響理化性質并加快反應速率,②溫度升高時,pKa和pHmax均會降低,因此,會促進鹽歧化的發生。
(4)其他因素
還有一些其他因素也會加快鹽歧化的發生,比如API粒度減小、增加表面積將加快反應速度、鹽酸鹽的鹽酸揮發等。
小結:
現在我們對鹽歧化發生的因素進行小結(圖 7),鹽歧化發生的因素主要分為自身因素和環境因素,自身因素為根本因素,主要有① pKa②pHmax③鹽、游離堿溶解度的差異,這些參數可以通過pHmax來體現。環境因素有輔料①輔料②水分③溫度④粒度和比表面積⑤其他,這些因素大部分仍與pHmax有關。因此鹽歧化中最需要關注的點為pHmax。
圖7 鹽歧化發生的因素
三、減少鹽歧化發生的策略
了解了鹽歧化發生的原因,就可以做一些針對工作,以減少鹽歧化的發生,可以在以下四個角度減少鹽歧化發生(圖 8)。
首先在成鹽的選擇上:在分子的pKa較低的情況下,溶解度較低的鹽可能優于溶解度較高的鹽。鹽選擇的主要目的應該是找到足夠溶解的鹽,而不是最易溶的鹽,因為過度溶解通常會導致物理和化學不穩定性。
在制備工藝的選擇上,由于水分會促進弱堿鹽歧化,所以應該避開水性制粒,降低含水量。
輔料選擇上:避開導致鹽歧化的堿性輔料:硬脂酸鎂、交聯羧甲基纖維素鈉、硬脂富馬酸鈉,尤其是硬脂酸鎂,最容易導致鹽歧化的發生。
降低微環境pH:若降低pH至pHmax以下,則可減弱鹽歧化,可以通過加入pH調節劑來實現:如草酸、酒石酸等有機酸。
如果能兼顧這些因素,就可能制備鹽歧化風險較小的制劑。
圖8 減少鹽歧化發生的策略
總結:
最后我們對鹽歧化現象進行總結(圖 9):
鹽歧化常發生在弱酸鹽和弱堿鹽中,最常見的是弱堿鹽,若API的鹽型或制劑處方沒有選好,就可能造成產品批間差異大、效價喪失、溶出緩慢、生物利用度降低等,延緩研發進度或者造成上市后的損失。而鹽歧化發生的因素分為自身因素和環境因素,這些因素中pKa和pHmax最為關鍵,需要格外關注。若一個藥物確定作為強酸弱堿鹽時,常見的減少鹽歧化發生的策略有①選擇合適溶解度的鹽型,②避開水性制粒,③避開導致鹽歧化的堿性輔料,④降低微環境pH。
圖9 鹽歧化現象總結
參考文獻:
[1]Gregory A. Stephenson, Aktham Aburub, Timothy A. Woods,Physical Stability of Salts of Weak Bases in the Solid-State,Journal of Pharmaceutical Sciences,Volume 100, Issue 5,2011,Pages 1607-1617。
[2]Thakral, Naveen, K, et al. Salt disproportionation: A material science perspective[J]. International Journal of Pharmaceutics, 2017.
[3]Sampada Koranne, Rahul Lalge, and Raj Suryanarayanan
Molecular Pharmaceutics 2020 17 (4), 1324-1334
[4]Mol.Pharmaceutics 2021,18,3247−3259。