現(xiàn)有的醫(yī)療器械中應用的納米材料包括添加到醫(yī)療器械中的游離態(tài)納米材料,利用納米材料特性增加生物學活性(如醫(yī)用納米羥基磷灰石/聚酰胺66復合骨充填材料)或者預防感染(如納米銀創(chuàng)傷貼)的固化納米材料以及利用納米技術設計制備成納米結構的醫(yī)療器械(如口腔種植體材料表面納米化處理)等。此外,即使醫(yī)療器械本身不含有納米材料,其使用/植入過程也有可能導致納米顆粒的產(chǎn)生。
根據(jù)國家標準(GB/T 30544.1),納米材料是指任一外部維度、內(nèi)部或表面結構處于納米尺度的材料,而納米尺度是指1~100 nm之間的尺寸范圍,該尺寸范圍通常,但非專有地表現(xiàn)出不能由較大尺寸外推得到的特性,對于這些特性來說,1-100 nm的上、下限值是近似的。納米材料獨特的物理、化學和生物學性質(zhì)為醫(yī)療器械獲得突破性發(fā)展提供了新的機遇,同時也蘊含潛在的臨床應用風險。
本指導原則為申請人/監(jiān)管人員提供關于應用納米材料的醫(yī)療器械安全性和有效性評價相關方面的信息。
本指導原則是對應用納米材料醫(yī)療器械的一般要求,申請人應依據(jù)具體產(chǎn)品的特性對注冊申報資料的內(nèi)容進行充分說明和細化。申請人還應依據(jù)具體產(chǎn)品的特性確定其中的具體內(nèi)容是否適用,若不適用,需詳細闡述理由及相應的科學依據(jù)。
本指導原則是在現(xiàn)行法規(guī)和標準體系以及當前認知水平下制定的,隨著法規(guī)和標準的不斷完善,以及科學技術的不斷發(fā)展,本指導原則相關內(nèi)容也將進行適時的調(diào)整。
醫(yī)療器械應用納米材料評價
一、適用范圍及一般原則
1、適用范圍
本指導原則適用于與人體直接或間接接觸,由納米材料組成或包含納米材料的醫(yī)療器械的安全性和有效性評價。
不適用于:
應用納米材料的體外診斷(In Vitro Diagnosis,IVD)產(chǎn)品,但在考慮IVD產(chǎn)品有效性時,可參考相關內(nèi)容;
應用納米材料的賦能技術;
應用納米材料的藥品;
應用納米材料的醫(yī)療器械在制造和廢棄過程中造成的職業(yè)和環(huán)境風險。
2、一般原則
(一)應用納米材料醫(yī)療器械的分類
目前現(xiàn)有或者正在處于研發(fā)階段的應用納米材料的醫(yī)療器械,按照GB/T 16886.1進行分類。對于所有類型的醫(yī)療器械,納米材料的潛在暴露均應納入考慮。
(二)風險評估
納米材料的特性為醫(yī)療器械獲得突破性發(fā)展提供了新機遇,同時也存在潛在的不確定風險,在設計、臨床前測試、臨床評價和設計變更等階段,注冊申請人可以根據(jù)GB/T 16886.1、YY/T 0316和《醫(yī)療器械產(chǎn)品受益-風險評估注冊技術審查指導原則》等中規(guī)定的風險因素,對應用納米材料的醫(yī)療器械進行風險評估。應用納米材料醫(yī)療器械的風險因素主要包括納米材料從器械釋放的可能性、暴露劑量、暴露途徑、接觸部位和暴露時間。
(三)安全性評價
生物學評價是應用納米材料醫(yī)療器械安全性評價的重要內(nèi)容。GB/T 16886.1規(guī)定了應當根據(jù)器械類型、接觸途徑和接觸時間來進行生物學風險評估的程序框架,該程序框架通常也適用于應用納米材料的醫(yī)療器械。GB/T 16886系列標準的后續(xù)部分描述了詳細的試驗方案和評價策略。
當前ISO TC 194“醫(yī)療器械生物相容性評價技術委員會”已頒布了醫(yī)療器械生物學評價第22部分:納米材料指南,納米材料生物學評價可參考ISO/TR 10993-22。目前,已發(fā)布并實施的三項推薦性標準:YY/T 0993、YY/T 1295和YY/T 1532,這些標準為應用納米材料的醫(yī)療器械生物學評價提供了專屬方法。
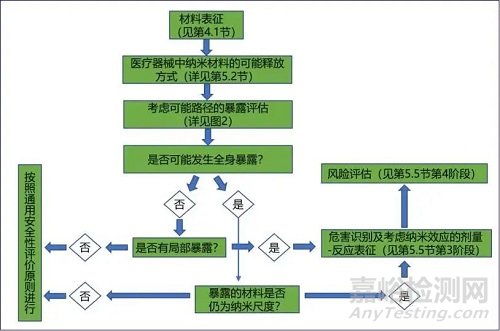
由于納米材料的比表面積等因素不同,納米材料表現(xiàn)出不同的理化性質(zhì),因此,生物體暴露于納米材料之后,可能表現(xiàn)出與常規(guī)材料不同的生物學反應。申請人應針對醫(yī)療器械的結構特征、預期用途、與人體的接觸途徑、所含納米材料的種類和形態(tài)等因素,通過設計一系列試驗來確認測試系統(tǒng)的適用性,從而建立起適合所申報產(chǎn)品特點的生物學評價試驗方案。應用納米材料醫(yī)療器械的安全性評價流程和路徑見下圖。
圖片來源:NMPA的法規(guī)匯總
(四)有效性評價
應用納米材料的醫(yī)療器械有效性評價方法可包括臺架試驗、體外測試、計算機模擬、動物實驗和臨床試驗。申請人應闡明在產(chǎn)品中使用納米材料/納米技術的必要性,以及與不采用納米材料的已上市同品種醫(yī)療器械明顯優(yōu)勢。如有可能,臨床試驗建議采用優(yōu)效性試驗。
應用納米材料的醫(yī)療器械開展動物實驗評價,可以根據(jù)醫(yī)療器械動物實驗研究技術審查指導原則第一部分和第二部分的要求進行。臨床評價應按照《醫(yī)療器械監(jiān)督管理條例》《醫(yī)療器械注冊管理辦法》《醫(yī)療器械臨床試驗質(zhì)量管理規(guī)范》和《醫(yī)療器械臨床評價技術指導原則》等要求進行。
由于納米技術是正在快速發(fā)展的新興領域,應用納米材料的醫(yī)療器械在進行風險評估時,可能無法與已上市的同品種醫(yī)療器械進行等同性比較,需要通過適宜的動物模型和臨床試驗來評價其有效性。申請人宜提出明確的試驗目的(即擬解決的問題),并根據(jù)試驗目的由具有相應專業(yè)知識和實踐經(jīng)驗的人員來制定科學、合理的研究方案。
(五)安全性和有效性評價體系框架
根據(jù)《醫(yī)療器械安全和性能的基本原則》,醫(yī)療器械應是安全的并且能夠實現(xiàn)其預期性能,其設計和生產(chǎn)應確保器械在預期使用條件下達到預期目的,與患者受益相比,其風險應是可接受的,且不會損害醫(yī)療環(huán)境、患者安全、使用者及他人的安全和健康。
本系列指導原則將在充分吸收最新科研成果的基礎上,分別對應用納米材料的醫(yī)療器械理化表征、生物學評價、動物實驗評價、體外替代測試/計算機模擬研究及臨床評價進行分析,并給出建議。由于醫(yī)療器械種類眾多,其人體接觸/暴露途徑也存在很大差異,具體到某一醫(yī)療器械,并非上述所有評價方法都是必要的。
二、理化表征
(一)一般原則
醫(yī)療器械的材料表征包括化學、物理、形態(tài)學和表面等性質(zhì)的表征(GB/T 16886.18和GB/T 16886.19),納米材料表現(xiàn)出獨特的性質(zhì)取決于它們的大小、結構和表面性質(zhì)等不同于常規(guī)材料。因此,參與組成器械的納米材料的理化性質(zhì)表征是完成生物學評價的重要一步,可以指導應用納米材料醫(yī)療器械生物學評價試驗方案的制定,也對醫(yī)療器械中新的納米材料進行有效篩選給出建設性意見。
ISO/TR 13014列出了以下毒理學試驗中需要表征的工程化的納米材料的特性:化學成分、純度、尺寸和尺寸分布、聚集和團聚狀態(tài)、形狀、表面積、表面化學、表面電荷、溶解度和分散度等。
附加屬性的表征可以根據(jù)醫(yī)療器械的設計、預期用途和磨損特性來表示。如結晶、孔隙度、氧化還原電位、(光)催化、自由基的形成潛力和辛醇/水系數(shù)(未必適用于固體材料)等。
除了上述理化表征,表面具有納米結構的醫(yī)療器械可能需要從形態(tài)學上進行表征。對于表面結構的有效表征所需測量的參數(shù)取決于特定的應用。如對應用納米多孔材料的醫(yī)療器械的表征包含但不限于以下信息:孔隙或空隙的尺寸和結構、密度和分布等。
(二)表征參數(shù)與方法
ISO/TR 13014提供了與納米材料相關的生物學評價參數(shù)的詳細信息和每個參數(shù)進行定量和/或定性分析的方法。隨著對納米材料的不斷研究和探索,其表征方法也將不斷改進優(yōu)化,故以上內(nèi)容應根據(jù)需要進行動態(tài)調(diào)整。
結合幾種方法可以同時研究顆粒大小、形狀、結構、組成成分和表面性質(zhì)。單一的表征方法可能無法提供準確的評價參數(shù)(例如粒徑分布、表面配體和表面電荷等),建議使用微觀和宏觀多種方法用于一個特定理化參數(shù)的表征。但需要注意,可能對特定屬性使用不同方法所獲得的結果不能直接比較,并且目前幾乎沒有統(tǒng)一方法對納米材料進行理化評價以輔助形成可靠的試驗方案。申請人宜在醫(yī)療器械中納米材料的類型、形式以及醫(yī)療器械預期用途的基礎上選擇表征的方法。
由于納米材料的表征往往是科學和技術上的挑戰(zhàn),因此,申請人宜考慮實驗室的質(zhì)量保證體系和最優(yōu)方案。納米材料理化表征手段的選擇、表征結果和納米材料特性的解釋分析應該由經(jīng)過培訓且有經(jīng)驗的專業(yè)人員進行。在分析過程中,宜謹慎考慮樣品制備以確保所獲得的數(shù)據(jù)來自該器械中有代表性的材料。如有可能,申請人宜在理化表征中采用可獲得的適當?shù)膮⒄詹牧希员銓Ψ治鰞x器設備和試驗方法進行校正和檢驗。表征過程的各個環(huán)節(jié)應仔細記錄,以確保結果的可追溯性和可重復性。若有必要,所用方法應進行方法學驗證被證實能恰當用于納米材料的研究。有關應用納米材料的醫(yī)療器械理化性質(zhì)表征的具體內(nèi)容,將在本系列指導原則第二部分:應用納米材料的醫(yī)療器械理化表征指導原則中給出。
三、生物學評價
本指導原則僅給出應用納米材料醫(yī)療器械生物學評價的概述。有關具體內(nèi)容,將在本系列指導原則第三部分:應用納米材料的醫(yī)療器械生物學評價指導原則中給出。
相比于常規(guī)材料,納米材料在樣品制備時會有溶解性和分散性的區(qū)別,因此可能需要考慮納米材料在樣品制備時的特殊性;由于納米材料被認為可能穿越所有的保護屏障,包括血腦屏障和胎盤屏障等,因此可能需要考慮納米材料的全身毒性,特別是中樞神經(jīng)毒性和生殖毒性;“納米分子冠”的形成,可能會影響其生物響應、動力學、蓄積和毒性等生理效應;有些納米材料具有類佐劑特性,可能會對免疫系統(tǒng)產(chǎn)生影響,需要關注免疫毒性;血液中納米材料暴露的時間間隔不同可能改變其毒代動力學特征。因此,應用納米材料的醫(yī)療器械生物學評價內(nèi)容,在兼顧常規(guī)器械評價內(nèi)容的基礎上,重點考慮與納米材料有關的其他問題,如樣品制備,吸收、分布、代謝和排泄/清除(ADME)、全身毒性、中樞神經(jīng)毒性和免疫毒性等。
(一)樣品制備
樣品制備是對醫(yī)療器械最終產(chǎn)品及其制造過程中使用的材料進行表征和/或生物學試驗時的一個關鍵的多步驟過程,包括對器械有代表性取樣、浸提液制備,制備的試驗材料的貯存和穩(wěn)定性檢測等,應重點關注應用納米材料醫(yī)療器械的最終產(chǎn)品在樣品制備不同階段的理化性質(zhì)。樣品制備具體內(nèi)容詳見GB/T16886.12。
與常規(guī)材料相比較,納米材料樣品制備時應該考慮的因素包括表面特性增加了其反應性,溶解性和分散性的區(qū)別,聚集物或團聚物的形成和微量雜質(zhì)的污染(微量雜質(zhì)可能對納米材料理化特性和毒理學特性具有潛在的影響)等。另外,納米材料有吸附到容器表面的可能性。由重力引起的擴散和重力沉降也會影響納米材料(當發(fā)生團聚或聚集、或納米材料由致密物質(zhì)組成等)到細胞的輸送率。納米毒理學的劑量單位可能不是傳統(tǒng)的質(zhì)量濃度,而是納米顆粒數(shù)量或總表面積。
針對這些問題,有必要針對應用納米材料的醫(yī)療器械制定可靠的樣品制備方案。
在樣品制備時,需要仔細分析來確定一個特殊的納米材料在規(guī)定的實驗條件下是否完全分散、和/或部分溶解(如一些金屬)還是完全溶解,因為微溶或不溶的納米材料可能以顆粒的形式分散存在于實驗體系中。分散可能引起一種不同于從化學成分預測的分子、離子或元素毒性的反應;而可溶性的納米材料可能出現(xiàn)與相同分子或元素組成的常規(guī)材料相似的反應。
納米材料的分散性受納米材料之間和/或與其所處環(huán)境相互作用的影響,分散的納米材料不一定僅以原形存在,也可能以聚集體或團聚體的形式存在;納米材料的粉末和氣溶膠形式通過表面電荷或空間效應則變得不穩(wěn)定。因此,試驗樣品穩(wěn)定性是納米材料生物學評價中獲得準確、可靠的試驗結果的關鍵因素之一。
電解質(zhì)濃度、pH范圍、離子強度或分子成分(如血清蛋白分子等)對浸提液制備有顯著影響。因此,生物學評價試驗中應用的分散條件應盡可能與生理條件一致。
在應用納米材料醫(yī)療器械的成品或原材料的表征、動物實驗或體外試驗時,需要進行樣品制備。制備的具體方法可能因接觸途徑和劑量選擇的不同而有差異。在試驗樣品制備和接觸方式的記錄或報告內(nèi)容中至少應包含以下內(nèi)容:
試驗材料的鑒定、貯存和穩(wěn)定性,包括批與批之間的差異性;
浸提介質(zhì)的化學組成;
合適的劑量單位選擇;
原料分散劑制備的樣品在給予動物(和/或細胞、器官、組織)之前的表征;
作為一般原則,樣品制備的細節(jié)和所選用方法的基本原理應當詳細記錄。
NMPA相關解讀
本指導原則對于納米材料的定義依據(jù)是國家標準(GB/T 30544.1),納米材料是指任一外部維度、內(nèi)部或表面結構處于納米尺度的材料,而納米尺度是指1nm—100 nm之間的尺寸范圍。然而,納米材料的科學定義,國際科學界仍在討論,隨著對于納米技術的發(fā)展,科學界對于何為納米尺度,納米尺度的外延等問題不斷有新的認識。因此,對于一種材料是否為納米材料,應主要考察其是否具有宏觀尺度所不具備,且無法由其他尺度外推得出的獨特性質(zhì)。
指導原則適用范圍及相關術語
本指導原則不適用于:
1.應用納米材料的體外診斷(In Vitro Diagnosis,IVD)產(chǎn)品,但在考慮IVD產(chǎn)品有效性時,可參考相關內(nèi)容;
2.應用納米材料的賦能技術;
3.應用納米材料的藥品;
4.應用納米材料的醫(yī)療器械在制造和廢棄過程中造成的職業(yè)和環(huán)境風險。
因IVD產(chǎn)品不與人體接觸,所以對于納米材料的安全性,僅考慮制造和廢棄過程中的職業(yè)和環(huán)境風險,而不是對于醫(yī)療器械進行評價。作為一類應用廣泛的平臺性技術,納米技術的應用不限于醫(yī)療器械,在微電子等領域應用更為普遍,如目前的芯片,多數(shù)都需要采用納米加工技術。而采用納米技術賦能制造的產(chǎn)品,本身不被視為納米產(chǎn)品。納米技術在醫(yī)藥領域的應用,可能產(chǎn)生一系列新的醫(yī)療產(chǎn)品,其中可能包括藥品或藥械組合產(chǎn)品,本指導原則僅適用于由國家藥監(jiān)局標準管理部門明確界定為醫(yī)療器械的產(chǎn)品。
納米尺度
處于1nm至100nm之間的尺寸范圍。
注1:本尺寸范圍通常、但非專有地表現(xiàn)出不能由較大尺寸外推得到的特性。對于這些特性來說,尺度上、下限值是近似的。
注2:本定義中引入下限(約1nm)的目的是為了避免在不設定下限時,單個或一小簇原子被默認為是納米物體或納米結構單元。
納米材料
任一外部維度、內(nèi)部或表面結構處于納米尺度的材料。
注1:本通用術語包括納米物體和納米結構材料。
注2:見工程化的納米材料、人造納米材料和伴生納米材料。
注3:近些年隨著科學界對納米材料的認知逐漸增多,某一維度的尺寸在100nm至1000nm范圍內(nèi),且表現(xiàn)出因尺寸而產(chǎn)生的特殊效應或現(xiàn)象的材料,該材料在本指導原則評價范圍之內(nèi)被認為是納米材料。納米材料的定義根據(jù)最新研究進展實時更新。
工程化的納米材料
為了特定目的或功能而設計的納米材料。
人造納米材料
為了商業(yè)目的而制造的具有特定功能或特定組成的納米材料。
伴生納米材料
在某一過程中作為副產(chǎn)品非特意產(chǎn)生的納米材料。
注1:過程包括制造、生物技術或其他過程。
注2:見ISO/TS 27628: 2007, 2.21對“超細顆粒”的定義。
納米物體
一維、二維或三維外部維度處于納米尺度的物體。
注:用于所有相互分離的納米尺度物體的通用術語。
風險評估及材料評價等問題
1、關于應用納米材料的醫(yī)療器械風險評估問題
應用納米材料的醫(yī)療器械需符合GB/T 16886.1、YY/T 0316和《醫(yī)療器械產(chǎn)品受益-風險評估注冊技術審查指導原則》等文件中規(guī)定的風險因素,主要包括納米材料從器械釋放的可能性、暴露劑量、暴露途徑、接觸部位和暴露時間。風險評估最重要的因素是納米材料從醫(yī)療器械中釋放的可能性。風險評估應分階段、有步驟進行,考慮暴露評估(納米材料釋放)、納米材料分布及持續(xù)存留和環(huán)境轉化、危害識別,并最終根據(jù)產(chǎn)品的適用范圍是否給患者帶來足夠的受益來綜合考慮產(chǎn)品風險。
2、關于應用納米材料的醫(yī)療器械安全性評價問題
由于納米材料的比表面積等因素不同,納米材料表現(xiàn)出不同的理化性質(zhì),因此,生物體暴露于納米材料之后,可能表現(xiàn)出與常規(guī)材料不同的生物學反應。申請人應針對醫(yī)療器械的結構特征、預期用途、與人體的接觸途徑、所含納米材料的種類和形態(tài)等因素,通過設計一系列試驗來確認測試系統(tǒng)的適用性,從而建立起適合所申報產(chǎn)品特點的生物學評價試驗方案。當前,GB/T 16886(ISO 10993)的生物學評價體系總體適用于納米材料,但具體到某一應用納米材料的醫(yī)療器械,其試驗方法、樣品制備、細胞系/動物品系選擇、觀察終點、結果分析等均可能與常規(guī)材料不同。因此,需要各學科領域專家共同完成。
3、關于應用納米材料的醫(yī)療器械理化表征問題
ISO/TR 13014提供了與納米材料相關的生物學評價參數(shù)的詳細信息和每個參數(shù)進行定量和/或定性分析的方法。但需要注意,如果對于某個納米材料,對某個特定屬性使用不同方法所獲得的結果不能直接比較,并且目前幾乎沒有統(tǒng)一方法對納米材料進行理化評價以輔助形成可靠的試驗方案。申請人宜在醫(yī)療器械中納米材料的類型、形式以及醫(yī)療器械預期用途的基礎上選擇表征的方法。納米材料的理化表征,對于醫(yī)療器械申請人的研發(fā)能力、實驗室質(zhì)量保證體系等要求很高。
4、關于應用納米材料的醫(yī)療器械生物學評價問題
相比于常規(guī)材料,納米材料在樣品制備時會有溶解性和分散性的區(qū)別,因此可能需要考慮納米材料在樣品制備時的特殊性。由于納米材料被認為可能穿越所有的保護屏障,包括血腦屏障和胎盤屏障等,因此可能需要考慮納米材料的全身毒性,特別是中樞神經(jīng)毒性和生殖毒性。“生物分子冠”的形成,可能會影響其生物響應、動力學、蓄積和毒性等生理效應。有些納米材料具有類佐劑特性,可能會對免疫系統(tǒng)產(chǎn)生影響,需要關注免疫毒性。血液中納米材料暴露的時間間隔不同可能改變其毒代動力學特征。綜上所述,應用納米材料的醫(yī)療器械生物學評價內(nèi)容,在兼顧常規(guī)器械評價內(nèi)容的基礎上,建議重點考慮與納米材料有關的其他問題,如樣品制備,吸收、分布、代謝和排泄/清除(ADME)、全身毒性、中樞神經(jīng)毒性和免疫毒性等。