當前,單克隆抗體是目前發展最快的新型治療性生物大分子藥物,隨著國內生物醫藥的快速發展,越來越多的新型抗體藥物(如雙特異性抗體、抗體偶聯藥物(ADC)等)進入產業化階段,本文梳理了新型抗體藥物-ADC的生產現場檢查關注點,新型抗體藥物企業在員工培訓或內部質量審計等工作中可參考使用。
一 新型抗體藥物-ADC的生產工藝
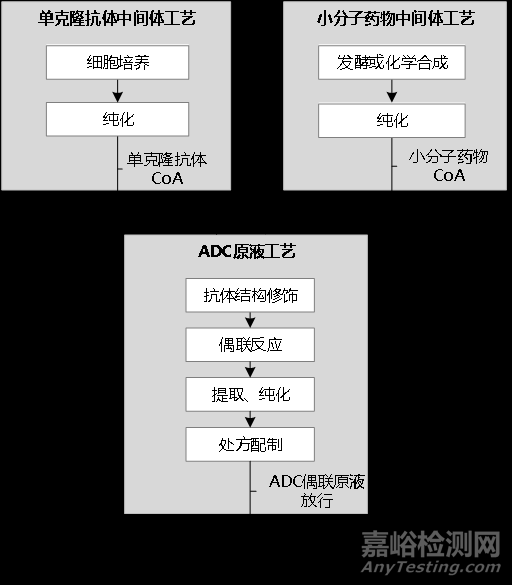
抗體偶聯藥物(Antibody–Drug Conjugates,簡稱ADC)是新藥研發熱點之一,被業界人士稱為靶向殺傷腫瘤細胞的“生物導彈”,ADC是指由靶向特異性抗原的抗體藥物與有效載荷(如小分子細胞毒藥物)通過連接子偶聯而成,兼具傳統小分子細胞毒藥物的強大殺傷效應和抗體藥物的腫瘤靶向性,通俗地講,ADC主要由三部分組成,分別是抗體(制導系統-靶向定位)+連接子(linker)+細胞毒素(也有效載荷(payload)、殺傷性彈藥),ADC的優勢是在抗體藥物高特異性的基礎上,增加了對腫瘤具有更強殺傷力的細胞毒性小分子藥物,ADC藥物生產流程參考示意圖如下:
二 新型抗體藥物檢查策略
新型抗體藥物屬于生物大分子的特殊屬性,在檢查中除了應當關注新型抗體藥物的工藝特性、過程控制、生產能力和質量屬性,還需要重點關注抗體生物活性和原液生產過程中污染控制的工藝控制要求,現在監管機構現場檢查一般采用兩種策略,分別是基于體系的橫向檢查策略和基于品種的縱向檢查策略。

三 新型抗體藥物-ADC檢查關注點
ADC藥物的生產是一個技術密集型流程,大體可分為小分子藥物生產工藝、原液的生產工藝及制劑的生產工藝3個環節,每個環節都擁有其關注點,基于對ADC藥物當前的認識,梳理了ADC藥物小分子藥物生產工藝和制劑生產工藝檢查關注的重點,原液生產工藝可參見單抗的通用檢查要點,如有遺漏,歡迎大家補充。
1.小分子藥物生產
生產工藝主要包括:連接子制備、小分子藥物制備、連接子-小分子藥物制備。
【檢查要點示例】
應當盡可能使用專用設施(如獨立的HVAC系統)和設備進行小分子藥物分裝;如共線生產,需采取特別防護措施并經過風險評估和必要的清潔驗證,應充分評估小分子藥物在環境及設備表面殘留可能造成的風險。
應設立獨立的洗衣間,用于小分子藥物生產人員穿戴的防護服的清洗,如有必要,應進行預浸泡處理。
小分子藥物中間品及產品等進行轉運時應采用不易破碎的器具進行二次包裝。
小分子藥物和連接子-小分子藥物生產區域及存儲設備設施應受控。
對產品質量有影響的起始物料、試劑應建立質量控制標準,如果手性對ADC藥物的活性有影響,對具有手性的起始物料應制定對映異構體或非對映異構體的限度。
當起始物料或中間體的某個雜質與產品的關鍵質量屬性關聯時,應驗證生產工藝去除該雜質或其衍生物的能力并確定質量標準。
應制定中間體的質量控制標準,如性狀、有關物質等;
應對制備過程中影響產品質量的工藝參數(例如:投料量、工藝溫度、工藝時間、精制方法、干燥方式、干燥溫度等)進行控制。
根據產品質量控制的需要,應檢測外觀性狀、理化常數(如比旋度、溶解度等)、無機雜質、有機殘留溶劑(如有必要)、有關物質、含量等(如必要)。
工藝中涉及柱層析和制備純化等使用填料的步驟時,若填料循環使用,應關注填料壽命及清潔方法,并有相關驗證研究。
如涉及中間體或產品混合(包括但不限于將小的批次混合以增加批量、將相同中間體或產品的尾料(例如分離出的相對較少的量)混合成一個批次),每一個將被用于混合的批次均須是按照注冊批準的規程生產、檢測并符合質量要求;應對混合過程進行監控和記錄;混合批號的有效期或復驗期應根據混合物中最早的尾料或批次的生產日期決定。
如果涉及物料和溶劑回收,應具備經過批準的溶劑回收規程,且回收的物料和溶劑應有質量標準;若回收溶劑與新溶劑混合使用,應有相關研究證明回收溶劑可適用于其可能被使用的所有生產步驟;對母液、回收溶劑和其他回收物料的使用應有記錄。
2.ADC制劑生產
ADC制劑的生產工藝包括:半成品配制、過濾灌裝、凍干(如有)、軋蓋、燈檢、貼簽、包裝等。
2.1【半成品配制工藝檢查要點示例】
關注原液儲存容器、原液化凍方式和化凍時間的控制方式(如凍融條件(溫度、時長、震搖)、凍融次數等)。
關注原液/成品藥液工藝時長、原液稀釋時的攪拌溫度/時間/速度、緩沖液配制參數(容器開口后吐溫多次使用或者長時間存放,需要考慮氧化雜質影響、如產品對金屬粒子、氧氣和光照敏感,配液罐(金屬離子)、罐體頂空氧/稀釋劑/溶劑的溶氧、光照等。
關注除菌過濾前的微生物負荷控制水平、除菌過濾工藝的過濾設計,如濾器種類、過濾動力學參數(如最大過濾體積、壓力或濾速、時長、溫度)等工藝參數;
2.2【過濾灌裝工藝檢查要點示例】
關注灌裝泵種類和速度(剪切力)、灌裝溫度/時長、噴嘴(直徑、位置、數量)、充氮(起泡)、光/氧等工藝參數;
采用蠕動泵進行灌裝的,應當重點關注灌裝精度要求。
2.3【凍干工藝檢查要點示例】
凍干步驟關注凍干曲線的批間一致性,如出現異常,相關的調查、評估對產品質量的影響及風險控制措施。
2.4【加塞/壓蓋工藝檢查要點示例】
ADC制品軋蓋結束后應對容器外壁進行清洗,以減少取樣、燈檢過程中人員操作暴露,清洗時應控制清洗水的溫度。清洗后應確保容器在進入后段包裝或暫存冷庫前,已處于干燥的狀態。
加塞/壓蓋除關注無菌保證相關參數(如軋蓋力等)外,還應根據產品自身特性關注膠塞/活塞的硅油、玻璃的金屬離子等對產品質量的影響;
生產過程應注意消毒劑殘留(如雙氧水等)對產品質量的影響(氧化物)。
2.5【軋蓋、燈檢、貼簽、包裝等工藝檢查要點示例】
由于ADC品種多為低溫儲存,應當重點關注燈檢、包裝、貼簽等步驟的脫冷鏈暴露及光照暴露和時間的控制要求。
當抗體偶聯的小分子藥物具有較強的疏水性時,應關注ADC藥物在生產和貯藏期間多聚體的變化情況,檢測方法應具有專屬性和靈敏度。
如共線生產,經有數據的風險評估和采取有效的措施后方可實施。應充分評估ADC制品在環境及設備表面中殘留可能造成的風險,并采取有效的措施進行殘留去除,設備的清潔應經過清潔驗證,確保制品暴露風險可接受。
采用人工燈檢的,人員應經過實操培訓且經考核合格后方可上崗,應定期進行再培訓;
采用燈檢機燈檢的,燈檢機應當經過驗證。驗證應包含人機對比且不得低于人工燈檢效果。
應當建立不合格品樣品庫, 以便于后續追溯,并定期進行盤點,當生產過程中出現新種類的不合格品時應進行調查并評估是否更新至不合格品樣品庫。應定期對不合格品趨勢進行分析,并對出現的異常趨勢或偏差進行調查。
參考文獻
《人用重組單克隆抗體制品生產通用技術要求》、《抗體類藥品現場檢查指南(征求意見稿)》、《探討單抗注冊生產現場檢查中的質量控制要點》等。