您當前的位置:檢測資訊 > 科研開發
嘉峪檢測網 2022-06-12 22:26
一、前言
美國藥典USP<60>收載了洋蔥伯克霍爾德菌(以下簡稱Bcc菌)的相關要求及檢測方法,FDA于 2021年9月發布了微生物控制的指南草案《Microbiological Quality Considerations in Non-sterile Drug Manufacturing》(非無菌藥品生產中的微生物質量考量),里面也包括Bcc菌在內的相關要求,但現行版中國藥典尚未收錄Bcc菌的相關要求。為與國際接軌,同時更好控制產品的微生物質量,中國藥典正在進行與Bcc菌相關內容的制修訂工作。
二、我國微生物質量控制的發展趨勢
考慮到要與國際接軌,國家藥典委員會正在制修訂微生物質量控制方面的通則內容,截圖如下:

中檢院也于今年5月份開展了微生物質量控制方面的相關培訓,具體培訓內容截圖如下:

從以上內容可以看出:我國的微生物質量控制趨勢正在與國際接軌,在非無菌藥品微生物質量控制中引入水分活度的概念(關于水分活度的相關內容詳見USP<1112>),使微生物質量控制更加科學;同時引入新型控制菌--Bcc菌的檢查方法,逐步與FDA和USP趨同。關于Bcc菌的相關介紹詳見下文。
三、洋蔥伯克霍爾德菌(Bcc菌)的研究趨勢
Bcc菌與現有的微生物限度檢查并不沖突,Bcc菌是微生物限度檢查的補充,它是一種有害微生物,屬于控制菌的一種。在美國,Bcc菌是非無菌藥品召回的首要原因。由于其危害性較大,美國藥典及FDA近期出臺的相關指南均重點關注了Bcc菌,在現有微生物限度檢查(一般包括需氧菌總數、霉菌酵母菌總數及控制菌檢查)的基礎上對Bcc菌提出了新的要求,其具體檢測方法詳見USP<60>。現有的關于微生物限度檢測所遵循的技術要求匯總如下表所示:
各國藥典及ICH指南中關于微生物限度控制的對比
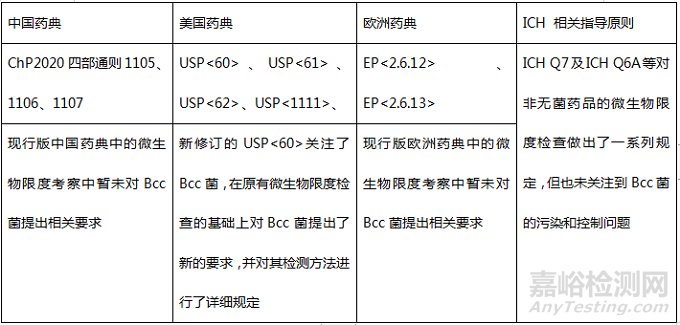
由于Bcc菌的危害性較大,我國于近期也開始關注水性非無菌藥品中的Bcc菌污染問題。國家藥典委已將Bcc菌控制納入中國藥典2020年版增補本(目前該標準草案處于審議階段,可持續關注中國藥典2020年版增補本的動態),2021年11月26日發布的《化學藥品創新藥上市申請前會議藥學共性問題及相關技術要求》通告中規定:對于吸入、口服、粘膜、皮膚和鼻腔給藥的水溶液非無菌制劑,一般應參照相關技術要求對Bcc菌進行研究,制定相應的控制策略。即,目前藥典委和CDE均關注到了Bcc菌。
Bcc菌是一組革蘭氏陰性菌,包括20多種有效菌種。該菌屬于有害微生物之一,對免疫力低下的人群傷害較大,可能會引起感染甚至死亡。制藥用水和生產過程中使用的天然成分是藥品中Bcc菌的主要來源,即Bcc菌在固體制劑中出現的風險較小,其主要出現在水性非無菌藥品中。由于Bcc菌污染而導致的不良反應事件及藥品召回越來越多,所以建議生產商在生產水性非無菌藥品時嚴格遵循GMP,以更好保證產品的微生物質量:
★為工藝操作的設計和控制建立風險管理計劃,以防止Bcc菌污染;
★使用強悍的工藝用水系統(生產商必須對水系統進行穩健的設計,包括旨在防止有害微生物的控制措施以及用于監測、清潔和維護的程序);
★確保各組分均符合微生物負荷量的適當標準;
★對設備進行恰當的消毒和清潔;
★采用經驗證的抽樣程序,以定期對Bcc菌的存在進行中控檢測和成品測試。
Bcc菌的危害性較大,為保證產品質量及患者安全,生產商在水性非無菌藥品生產中需重點關注該菌的污染問題。我國監管部門也在近期出臺了相關技術要求,在現有微生物限度檢查的基礎上,對水性非無菌藥品中的Bcc菌提出新的要求,建議對水性非無菌藥品開展Bcc菌檢查和風險評估,以更好控制水性非無菌藥品的微生物質量。
案例分析:洋蔥伯克霍爾德氏菌(Burkholderia cepacia,以下簡稱Bcc菌)對口服溶液的污染
FDA執法報告(2012年至2019年)顯示,Bcc菌是非無菌藥物召回的首要原因,有102次。其中,2016年5月,美國疾病控制與預防中心(CDC)向FDA通報了涉及Bcc菌污染的9個州13家醫院患者患嚴重疾病和死亡的案例,這款被Bcc菌污染的產品是一種用于治療便秘的水性OTC藥品。FDA和CDC的檢測顯示,超過10批口服液產品被Bcc菌污染。Bcc菌臨床分離株與產品分離株相匹配。調查還發現,該公司用于生產該產品的水系統中含有Bcc菌。FDA和CDC確定合同生產商是這次污染的源頭,設計不良的水系統(冷系統;不連續循環)、系統監控不足、生產控制不善以及微生物檢測方法不充分,這些都給消費者帶來了嚴重的風險。合同生產商生產的所有液體產品最終都被召回。
案例分析和討論:制藥用水和生產過程中使用的天然成分是藥品中Bcc菌的最可能來源。因此,嚴格執行cGMP對確保產品質量和患者安全至關重要,包括設計良好的水系統、完善的生產過程控制及日常監測、經過充分驗證的有效的微生物檢測方法等等,通過以上控制措施,使水性非無菌藥品免受Bcc菌污染,更好保證產品質量和患者安全。
四、小結
Bcc菌是一種新型的控制菌,中國藥典尚未正式收錄該控制菌。由于Bcc菌的危害較大,故建議生產商重點關注水性非無菌產品中的Bcc菌污染問題。在現有微生物限度檢查的基礎上,對水性非無菌藥品中的Bcc菌提出新的要求,以更好保證藥品的微生物質量及患者安全。由于Bcc菌的檢測方法比較復雜,美國藥典已在通則USP<60>中詳細描述了Bcc菌的檢測方法,建議中國藥典也盡快將Bcc菌的檢測列入制修訂計劃。
參考文獻
1.Analysis of FDA Enforcement Reports (2012-2019) to Determine the Microbial Diversity in Contaminated Non-Sterile and Sterile Drugs. https://www.americanpharmaceuticalreview.com/Featured-Articles/518912-Analysis-of-FDA-Enforcement-Reports-2012-2019-to-Determine-the-Microbial-Diversity-in-Contaminated-Non-Sterile-and-Sterile-Drugs/
2.Microbiological Quality Considerations in Non-sterile Drug Manufacturing.FDA.2019-09. https://www.fda.gov/media/152527/download
3. USP<1112>.APPLICATION OF WATER ACTIVITY DETERMINATION TO NONSTERILE PHARMACEUTICAL PRODUCTS
4. 王似錦,余萌,胡昌勤,等.14 株伯克霍爾德菌的鑒定分析[J].中國抗生素雜志,2019,44( 10) : 1214-1219

來源:藥事縱橫


