您當(dāng)前的位置:檢測資訊 > 科研開發(fā)
嘉峪檢測網(wǎng) 2021-05-30 16:56
元素雜質(zhì)控制的法規(guī)背景
藥品中的元素雜質(zhì)不能給患者帶來任何治療益處,其需要被限制在一定限度,否則其進(jìn)入人體可能造成急性或慢性中毒。國際人用藥品注冊技術(shù)協(xié)調(diào)會ICH在2014年12月公布了元素雜質(zhì)指南Q3D,期待其執(zhí)行以保護(hù)所有患者的公共健康。接著各大藥監(jiān)機(jī)構(gòu)也陸續(xù)公布了具體指南和藥典附錄要求,如美國在2018年8月公布Elemental Impurities in Drug Products Guidance for Industry指南并要求執(zhí)行美國藥典<232> ELEMENTAL IMPURITIES—LIMITS和<2232> ELEMENTAL CONTAMINANTS IN DIETARY SUPPLEMENTS;歐盟在2018年12月頒布CERTIFICATION POLICY DOCUMENT Content of the dossier for chemical purity and microbiological quality并在EP5.20. Elemental impurities和2.4.20 Determination of elemental impurities項(xiàng)下注明具體要求;日本在JP上要求執(zhí)行Controlof Elemental Impurities in Drug Products和2.66 Elemental Impurities Procedures;中國CDE2020年10月在網(wǎng)站上已經(jīng)公開征求ICH指導(dǎo)原則《Q3D(R2):元素雜質(zhì)指導(dǎo)原則》的征求意見稿,并在中國藥典第四部附錄2321中包含了砷、鉻、汞、鉛測定法。如今,原料藥企業(yè)按照ICHQ3D基于風(fēng)險進(jìn)行內(nèi)部的系統(tǒng)評估和控制是基本的要求,同時在向各大藥監(jiān)系統(tǒng)提交原料藥DMF中也需要提供必要的信息。如:EDQM在2019年1月執(zhí)行的前述CEP遞交要求申請文件包含的內(nèi)容中3.2impurities項(xiàng)下明確規(guī)定企業(yè)必須進(jìn)行元素雜質(zhì)的評估,自行決定是否提交評估報告,但至少提交在評估基礎(chǔ)上的元素雜質(zhì)的討論信息。筆者在2021年3月收到EDQM的缺陷信中包含“Itis necessary to provide more details how RMS for elemental impuritieshas been evaluated”的缺陷。類似的,F(xiàn)DA在2017年10月頒布的完整性評估指南Completeness Assessments for Type II API DMFs Under GDUFA Guidance forIndustry中沒有明確提到必須包含元素雜質(zhì)內(nèi)容,但筆者在也收到FDA有關(guān)以下的要求“Werecommend that your risk assessment for elemental impurities besubmitted to your DMF and provide to each ANDA applicant whoreferences your DMF. If batch data is provided, please include thetype of analytical method used and the LOD of eachelement”發(fā)補(bǔ)信。作為原料藥質(zhì)量和注冊要素之一,相信原料藥企業(yè)的銷售部或質(zhì)保部一定收到了來著世界各地客戶的元素雜質(zhì)問卷調(diào)查。雖然格式千差萬別,但核心內(nèi)容基本一致—元素雜質(zhì)評估和如何控制。
原料藥中元素雜質(zhì)來源與評估
如何評估原料藥中元素雜質(zhì)的來源呢?
首先,原料藥企業(yè)要由質(zhì)量部牽頭建立一個元素雜質(zhì)的評估團(tuán)隊(duì),至少應(yīng)包括QA、QC、研發(fā)部、生產(chǎn)部、物控部、工程設(shè)備部等人員。評估團(tuán)隊(duì)?wèi)?yīng)參考ICHQ9指南中的風(fēng)險管理原則,從原輔料、生產(chǎn)設(shè)備、生產(chǎn)工藝、包裝容器、生產(chǎn)環(huán)境等方面對原料藥中可能存在的元素雜質(zhì)進(jìn)行識別和評估;然后根據(jù)評估情況,測定或者預(yù)測原料藥中的某個元素雜質(zhì)的水平,并與ICHQ3D中已建立的允許PDE值及允許濃度值比較和分析;進(jìn)一步總結(jié)評估和分析工作,建立原料藥元素雜質(zhì)控制策略;最后將上述所有信息形成書面的風(fēng)險評估報告,經(jīng)批準(zhǔn)后執(zhí)行。
在評估過程中,評估團(tuán)隊(duì)梳理原料藥A生產(chǎn)過程中涉及到的所有要素,并逐一評估每個要素,以確定元素雜質(zhì)的潛在來源,以及潛在元素雜質(zhì)的種類。

圖1原料藥中元素雜質(zhì)來源的魚骨圖
說明:
①生產(chǎn)設(shè)備引入已知的或可能存在的元素雜質(zhì)的風(fēng)險,可通過對生產(chǎn)過程的正確理解、對生產(chǎn)設(shè)備的適當(dāng)選擇、儀器設(shè)備的有效驗(yàn)證及GMP的良好執(zhí)行來降低。應(yīng)根據(jù)與藥品成分接觸的生產(chǎn)設(shè)備的部件成分知識,對特別關(guān)注的元素雜質(zhì)進(jìn)行評估。
②工藝用水為飲用水,應(yīng)回顧本公司每年委外測試的數(shù)據(jù),特別是元素雜質(zhì)。
③總結(jié)生產(chǎn)中所使用的所有物料,判斷它們是否本身含有這些元素雜質(zhì),以及是否潛在含有這些元素雜質(zhì)。可以尋求物料供應(yīng)商/生產(chǎn)商的幫助,以識別潛在的元素雜質(zhì)。
④梳理廠區(qū)特別是生產(chǎn)、倉儲等區(qū)域所處的環(huán)境情況,重點(diǎn)是物料暴露工序,識別可能的風(fēng)險。
⑤調(diào)研并判斷包裝材料引入元素雜質(zhì)的風(fēng)險水平。如判斷具有高風(fēng)險,則識別出具體元素雜質(zhì)并采取篩查等措施。
簡單來說,在評估過程中應(yīng)當(dāng)利用工藝流程圖為線索評估工藝反應(yīng)和控制以及環(huán)境引入元素雜質(zhì)情況;評估生產(chǎn)過程所涉及的所有設(shè)備和工器具可能引入元素雜質(zhì)情況;評估所有原輔包裝材料包括飲用水可能直接引入元素雜質(zhì)情況,特別地,原輔包裝材料評估需要采用供應(yīng)商調(diào)查問卷的輔助完成。
1.從工藝流程方面進(jìn)行評估(原料藥A工藝流程圖)

評估團(tuán)隊(duì)中研發(fā)人員為主的意見如下:
除催化劑鈀炭外,其余物料均不含刻意添加的元素雜質(zhì)。因此催化劑鈀炭中的鈀殘留應(yīng)重點(diǎn)考慮;
化學(xué)反應(yīng)過程和后續(xù)處理過程均不涉及激烈的反應(yīng)和強(qiáng)腐蝕性或者極端環(huán)境(高溫高壓等),溶劑和試劑以及反應(yīng)液難以對設(shè)備和管道造成侵蝕,不會產(chǎn)生元素雜質(zhì)污染產(chǎn)品;
本工藝中用到大量的飲用水可能還有一定的鐵,中和用碳酸氫鈉中的鈉,會在大量水清洗和溶劑溶解后離心清洗中去除,特別是粗品和精制品制備時不使用水,僅采用甲醇和二氯甲烷作為結(jié)晶溶劑,鐵、鈉等元素雜質(zhì)存在的幾率極低,同時鐵和鈉作為其他類元素,內(nèi)毒性相對較低不用進(jìn)一步考慮。
生產(chǎn)工藝過程中與物料接觸的部件材質(zhì)主要為304型號不銹鋼,304型號不銹鋼所含成分為鐵、鎳、錳和鉻,它們在工藝過程中和GMP條件下,特別是常規(guī)反應(yīng)對直接接觸部分影響小,同時因兩步精制僅使用溶劑甲醇和二氯甲烷結(jié)晶。不銹鋼中的四種元素進(jìn)入產(chǎn)品可能性很低,而且鐵、錳屬于其他元素類,鉻屬于3類元素,因這三種元素的內(nèi)在毒性較低可以不做進(jìn)一步篩查,但鎳作為2A類元素豐度稍高需要進(jìn)一步測試評估。
2.生產(chǎn)設(shè)備的評估
生產(chǎn)設(shè)備引入已知的或可能存在的元素雜質(zhì)的風(fēng)險,可通過對生產(chǎn)過程的正確理解、對生產(chǎn)設(shè)備的適當(dāng)選擇、儀器設(shè)備的有效驗(yàn)證及GMP的良好執(zhí)行來降低。應(yīng)根據(jù)與產(chǎn)品成分接觸的生產(chǎn)設(shè)備的部件成分知識,對特別關(guān)注的元素雜質(zhì)進(jìn)行評估。
評估團(tuán)隊(duì)梳理了原料藥A生產(chǎn)過程中使用到的設(shè)備和器具,并列出了這些材質(zhì)中可能存在的元素雜質(zhì)見表1。
表1原料藥A生產(chǎn)設(shè)備中元素雜質(zhì)來源

評估團(tuán)隊(duì)中以工程設(shè)備部為主的意見認(rèn)為,從設(shè)備材質(zhì)和生產(chǎn)工藝以及GMP管理結(jié)合來考慮,設(shè)備設(shè)施和管道以及工具等與物料直接接觸的部分很難進(jìn)入物料并傳遞到成品中,即便有極微量的鐵、錳、鋁、鎳、鉻、銅、鈦進(jìn)入也會被后續(xù)工序去除。同時根據(jù)ICHQ3D指南,鐵、錳、鋁、鈦屬于其他元素類,鉻和銅屬于3類元素,因這四種元素的內(nèi)在毒性較低且沒有在生產(chǎn)過程中特地加入,可以不做進(jìn)一步篩查;因極微量的鉛、鎘、砷和汞廣泛存在有人體毒性,屬于1類元素雜質(zhì),而鎳屬于2A類元素雜質(zhì),故鉛、鎘、汞、砷和鎳需要進(jìn)一步進(jìn)行篩查。
3.生產(chǎn)物料的評估
物控部對所有原輔料供應(yīng)商進(jìn)行了元素雜質(zhì)的問卷調(diào)查,調(diào)查結(jié)果結(jié)合質(zhì)量標(biāo)準(zhǔn)和元素測試情況進(jìn)行了匯總,結(jié)果見下表2。
表2原料藥A原輔料的元素雜質(zhì)可能來源

說明:
冰醋酸的供應(yīng)商在生產(chǎn)過程中沒有增加額外的元素去處理,符合國標(biāo)“GB1886.10-2015食品添加劑 冰乙酸”的要求,其中砷和重金屬以鉛計(jì)的限度分別為1ppm和2ppm,實(shí)際測定值低于限度。每生產(chǎn)1批原料藥A(約100kg),需要消耗醋酸約53kg。砷和鉛作為I類元素需要進(jìn)行考慮。
醋酐的供應(yīng)商在生產(chǎn)過程中沒有增加額外的元素去處理,符合國標(biāo)“GB10668-2000 工業(yè)醋酐”的要求,其中僅元素鐵的限度為2ppm,實(shí)際測定值低于限度。每生產(chǎn)1批原料藥A(約100kg),需要消耗醋酐約76kg。鐵作為其他類元素內(nèi)在毒性較低因此不會造成風(fēng)險。
乙醇的供應(yīng)商在生產(chǎn)過程中沒有增加額外的元素去處理,符合國標(biāo)“GB30610-2014食品添加劑 乙醇”的要求,其中控制重金屬以鉛計(jì)的限度為0.8ppm,實(shí)際測定值低于限度。每生產(chǎn)1批原料藥A(約100kg),需要消耗乙醇約80kg。鉛作為I類元素需要進(jìn)行考慮。
四氫呋喃的供應(yīng)商在生產(chǎn)過程中沒有增加額外的元素去處理,符合國標(biāo)“GB/T24772-2009”的要求,國標(biāo)中沒有金屬元素的控制指標(biāo)。每生產(chǎn)1批原料藥A(約100kg),需要消耗四氫呋喃約350kg。因此不會造成風(fēng)險。
原甲酸三乙酯的供應(yīng)商在生產(chǎn)過程中沒有增加額外的元素去處理,符合供應(yīng)商企業(yè)標(biāo)準(zhǔn),沒有控制金屬元素的指標(biāo)。每生產(chǎn)1批原料藥A(約100kg),需要消耗原甲酸三乙酯約189kg。因此不會造成風(fēng)險。
對甲苯磺酸的供應(yīng)商在生產(chǎn)過程中沒有增加額外的元素去處理,符合供應(yīng)商企業(yè)標(biāo)準(zhǔn),沒有控制金屬元素的指標(biāo)。每生產(chǎn)1批原料藥A(約100kg),需要消耗對甲苯磺酸約18kg。因此不會造成風(fēng)險。
化合物B的供應(yīng)商在生產(chǎn)過程中沒有增加額外的元素去處理,符合供應(yīng)商企業(yè)標(biāo)準(zhǔn),沒有控制金屬元素的任何指標(biāo)。每生產(chǎn)1批原料藥A(約100kg),需要消耗化合物B約62kg。因此不會造成風(fēng)險。
甲醛的供應(yīng)商在生產(chǎn)過程中沒有增加額外的元素去處理,符合國標(biāo)“工業(yè)用甲醛溶液GB9009-2011”的要求,其中控制鐵的限度為10ppm,供應(yīng)商提供報告書實(shí)際測定值低于1ppm。每生產(chǎn)1批原料藥A(約100kg),需要消耗甲醛約30kg。鐵作為其他類元素內(nèi)在毒性較低因此不會造成風(fēng)險。
鹽酸的供應(yīng)商在生產(chǎn)過程中沒有增加額外的元素去處理,根據(jù)其的出廠檢驗(yàn)報告,且符合GB320-93工業(yè)用合成鹽酸標(biāo)準(zhǔn),鐵和砷有控制,限度分別為2%和1ppm。每生產(chǎn)1批原料藥A(約100kg),需要消耗鹽酸300kg。鐵作為其他類元素內(nèi)在毒性較低,而砷作為I類元素需要考慮引入產(chǎn)品風(fēng)險。
環(huán)己烷的供應(yīng)商在生產(chǎn)過程中沒有增加額外的元素去處理,符合供應(yīng)商企業(yè)標(biāo)準(zhǔn)和GB17602-2008標(biāo)準(zhǔn),沒有控制金屬元素的指標(biāo)。每生產(chǎn)1批原料藥A(約100kg),需要消耗環(huán)己烷約60kg。因此不會造成風(fēng)險。
N,N-二甲基甲酰胺的供應(yīng)商在生產(chǎn)過程中沒有增加額外的元素去處理,符合供應(yīng)商企業(yè)標(biāo)準(zhǔn)和“GB17521-1998”的要求,其中僅元素鐵的限度為10ppm,實(shí)際測定值低于限度。每生產(chǎn)1批原料藥A(約100kg),需要消耗N,N-二甲基甲酰胺約12500kg。鐵作為其他類元素內(nèi)在毒性較低因此不會造成風(fēng)險。
鈀炭的供應(yīng)商在生產(chǎn)過程中沒有增加額外的元素去處理,但鈀原料中包含一定量的鐵、鉛、銅,其符合供應(yīng)商企業(yè)標(biāo)準(zhǔn)和GB23518-2009標(biāo)準(zhǔn)要求,元素雜質(zhì)主要是鐵/鉛/銅,每種雜質(zhì)要求不得過5%,供應(yīng)商進(jìn)行了主成分鈀的測試。因鐵銅為其他類元素內(nèi)在毒性較低,因此需要嚴(yán)格控制鈀殘留和鉛殘留問題。
二氯甲烷的供應(yīng)商在生產(chǎn)過程中沒有增加額外的元素去處理,符合供應(yīng)商企業(yè)標(biāo)準(zhǔn)和“GB4117-2008工業(yè)用二氯甲烷”的要求,沒有控制金屬元素的指標(biāo)。考慮是精制用溶劑,本公司制定了遠(yuǎn)嚴(yán)格于國標(biāo)的內(nèi)控質(zhì)量標(biāo)準(zhǔn),經(jīng)測試符合內(nèi)控標(biāo)準(zhǔn)。每生產(chǎn)1批原料藥A(約100kg),需要消耗二氯甲烷約670kg,僅作為溶劑,因此不會造成風(fēng)險。
甲醇的供應(yīng)商在生產(chǎn)過程中沒有增加額外的元素去處理,符合供應(yīng)商企業(yè)標(biāo)準(zhǔn)和“GB338-2011工業(yè)用甲醇”的要求,沒有控制金屬元素的指標(biāo)。考慮是精制用溶劑,本公司制定了遠(yuǎn)嚴(yán)格于國標(biāo)的內(nèi)控質(zhì)量標(biāo)準(zhǔn),經(jīng)測試符合內(nèi)控標(biāo)準(zhǔn)。每生產(chǎn)1批原料藥A(約100kg),需要消耗甲醇約1400kg,僅做為溶劑,因此不會造成風(fēng)險。
活性炭的供應(yīng)商在生產(chǎn)過程中沒有增加額外的元素去處理,其放行標(biāo)準(zhǔn)規(guī)定重金屬限度不得過30ppm;供應(yīng)商提供的COA上顯示控制鐵不得過0.05%。每生產(chǎn)1批原料藥A(約100kg),需要消耗活性炭1-2kg。鐵作為其他類元素內(nèi)在毒性較低,因此不會造成風(fēng)險。
精制用的硅膠的供應(yīng)商在生產(chǎn)過程中沒有增加額外的元素去處理,符合供應(yīng)商內(nèi)部標(biāo)準(zhǔn),沒有控制金屬元素的指標(biāo)。經(jīng)檢索,硅膠在生產(chǎn)過程中控制鐵鉛砷元素。每生產(chǎn)1批原料藥A(約100kg),需要消耗硅膠2kg,且僅用于助濾。鐵作為其他類元素內(nèi)在毒性較低,而鉛砷需要考慮進(jìn)入產(chǎn)品風(fēng)險。
吡啶的供應(yīng)商在生產(chǎn)過程中沒有增加額外的元素去處理,符合供應(yīng)商企業(yè)標(biāo)準(zhǔn)和GB27267-2011標(biāo)準(zhǔn),沒有控制金屬元素的指標(biāo)。每生產(chǎn)1批原料藥A(約100kg),需要消耗吡啶約60kg。因此不會造成風(fēng)險。
碳酸氫鈉的供應(yīng)商在生產(chǎn)過程中沒有增加額外的元素去處理,符合供應(yīng)商企業(yè)標(biāo)準(zhǔn)和“GB1606-2008”的要求,其中元素鐵的限度為50ppm,鈣不得過0.05%,砷不得過1ppm,實(shí)際測定值低于限度。每生產(chǎn)1批原料藥A(約100kg),需要消耗碳酸氫鈉約70kg。鐵和鈣作為其他類元素內(nèi)在毒性較低,而砷作為I類元素需要進(jìn)一步考慮。
飲用水在產(chǎn)品生產(chǎn)過程中作為水析介質(zhì)和無機(jī)雜質(zhì)清洗的溶劑。本公司飲用水是由XX市自來水公司統(tǒng)一提供的,本公司按照內(nèi)控標(biāo)準(zhǔn)每月測試合格,也每年一次委托外部有資質(zhì)的單位全檢,結(jié)果符合GB5749-2006,具體數(shù)據(jù)見下表3。
表3飲用水中元素雜質(zhì)測試信息表

每生產(chǎn)1批原料藥A(約100kg),需要消耗飲用水約2300kg,因飲用水使用量大,本公司根據(jù)測試結(jié)果計(jì)算各元素完全進(jìn)入成品中的理論含量見上表理論總量。由上述結(jié)果可知,即使全部進(jìn)入原料藥中也遠(yuǎn)遠(yuǎn)小于ICHQ3D指南可接受標(biāo)準(zhǔn),事實(shí)上經(jīng)過后續(xù)一系列的溶解、分離、精制其基本會得到去除。同時根據(jù)ICHQ3D指南鉻、錳、銅、鋅、硒和鋁作為3類或其它元素內(nèi)在毒性較低,且含量低不考慮。故飲用水引入需要考慮砷,鎘,汞,鉛等分布較廣元素的殘留問題。
起始原料XXXX生產(chǎn)中使用了含鎂的格氏試劑做催化劑,但是格氏反應(yīng)后經(jīng)過后續(xù)多個步驟的處理,如水解反應(yīng),洗滌,精制等等,因此殘留的鎂有限。生產(chǎn)過程中使用了碳酸氫鈉和碳酸鉀,此類無機(jī)物均溶于水,很容易在后續(xù)一系列的處理過程中去除。同時鎂、鈉、鉀作為其他元素內(nèi)在毒性較低,因此僅對起始原料中砷鉻汞鉛等1類元素需要考慮。
綜上所述,根據(jù)客戶問卷調(diào)查中元素雜質(zhì)引入情況反饋和原輔料制備工藝分析以及當(dāng)前公司GMP管理現(xiàn)狀下的物料管理操作流程,如:液體物料專用槽車或?qū)S猛啊⑷訒r和使用前檢查外觀等等。評估團(tuán)隊(duì)認(rèn)為原輔料可能引入催化劑鈀的殘留以及砷、鎘、汞、鉛等分布廣泛的元素雜質(zhì),需要考慮產(chǎn)品中這些元素的殘留情況。
4.環(huán)境的評估
本公司生產(chǎn)場地位于XXXX工業(yè)園區(qū)內(nèi),園區(qū)內(nèi)企業(yè)以制劑和原料藥以及醫(yī)藥中間體生產(chǎn)為主。本公司處于園區(qū)的上風(fēng)口,上風(fēng)口方向遠(yuǎn)處均為居民區(qū),上風(fēng)口和平行方向附近沒有粉塵產(chǎn)生,特別是含有元素雜質(zhì)的粉塵。本產(chǎn)品生產(chǎn)區(qū)域的門窗通常處于關(guān)閉狀態(tài),特別是原料藥最終暴露在空氣中的工序均是在D級潔凈區(qū)進(jìn)行的,且時間相對很短,故從空氣中帶入元素雜質(zhì)的風(fēng)險極低。
5.包裝材料的評估
原料藥A的內(nèi)包材為雙層低密度聚乙烯袋,用塑料扎帶密封,外包材為紙板桶或鋁聽。鑒于原料藥A是固體原料藥,元素雜質(zhì)從LDPE袋遷移到產(chǎn)品中的可能性非常小。因此不需要進(jìn)行更深入的評估。另外,LDPE袋生產(chǎn)廠家在生產(chǎn)過程中,未刻意添加元素雜質(zhì)。生產(chǎn)商提供的申明明確其確實(shí)未添加輔助材料,且符合USP/EP的食品/藥品級要求,因此包裝材料引入元素雜質(zhì)的風(fēng)險也極低。
綜上所述,本公司從生產(chǎn)工藝、原輔料、生產(chǎn)設(shè)備、生產(chǎn)環(huán)境和包裝材料五個方面一一評估后,確定了原料藥A中需要考察的元素及限度要求,詳見下表4。
表4原料藥A中需要考慮的元素雜質(zhì)及限度要求

注:*本公司原料藥A最終的劑型為口服制劑,因此表中各元素允許PDE值和需要考慮的元素均根據(jù)ICHQ3D指南中口服制劑相關(guān)信息而來。若為最終劑型為注射劑或吸入制劑的,應(yīng)根據(jù)相應(yīng)表格進(jìn)行調(diào)整,且注射劑或吸入制劑需要考慮的元素更多,如:注射劑和吸入制劑還需評估鋰、銻、銅,吸入制劑更進(jìn)一步增加鋇、鉬、錫、鉻等的考察評估。
**本公司原料藥A最大日攝入量為1g,根據(jù)ICHQ3D指南中的計(jì)算公式各元素的口服允許濃度即可計(jì)算得到。同樣的允許濃度與劑型有關(guān),注射劑和吸入制劑允許的濃度可能不同,需要根據(jù)指南進(jìn)行核對計(jì)算,如:本公司生產(chǎn)過程中使用的鈀,口服制劑允許濃度為10μg/g,其注射劑和吸入制劑允許濃度分別為1μg/g和0.1μg/g。若產(chǎn)品中某元素雜質(zhì)的PDE值和濃度超過指南的允許值,應(yīng)根據(jù)ICHQ3D指南評估合理性,必要時采取措施降低元素雜質(zhì)的含量。
本公司為進(jìn)一步考察原料藥A中上述元素的具體含量,化驗(yàn)室進(jìn)行兩項(xiàng)測試。一是采用ICP-MS對原料藥A中的鈀殘留測試方法進(jìn)行了摸索,在確定了原料藥A中的鈀測試方法后隨即展開了方法學(xué)驗(yàn)證。驗(yàn)證結(jié)果分別為:系統(tǒng)適應(yīng)性試驗(yàn)波動SD在0.1-1%范圍內(nèi);專屬性良好;0-25ppm的線性相關(guān)系數(shù)r=0.9999;重復(fù)進(jìn)樣的精密度RSD為1%;中間精密度RSD為2%;定量限、100%和150%濃度下測得的準(zhǔn)確度回收率為95%-100%;LOQ為1ppm。方法驗(yàn)證的結(jié)論是本方法能有效控制本公司生產(chǎn)的原料藥A中的鈀殘留。化驗(yàn)室對工藝驗(yàn)證連續(xù)5批原料藥A中的鈀殘留進(jìn)行了測試,結(jié)果均為<1ppm。二是對原料藥A工藝驗(yàn)證連續(xù)前3個批次的1類和2A元素雜質(zhì)進(jìn)行了測試,3批的測試數(shù)據(jù)基本一樣,具體結(jié)果見表5.
表5原料藥A中1類和2A類元素雜質(zhì)測試結(jié)果
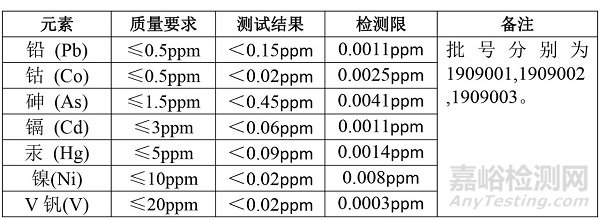
總評估結(jié)論:
根據(jù)各方面元素雜質(zhì)可能存在的情況和化驗(yàn)室進(jìn)一步測試的結(jié)果可知,本公司生產(chǎn)的原料藥A中包含的元素雜質(zhì)符合ICHQ3D中限度的要求。
注:若經(jīng)評估和測試后發(fā)現(xiàn)元素雜質(zhì)的濃度超過限度要求,通常應(yīng)考慮采取以下措施來處理。1)、改進(jìn)生產(chǎn)工藝過程,采用有針對性的純化步驟降低元素雜質(zhì)。如:筆者曾在CEP申請中被EDQM要求降低催化劑鈀的殘留,后研發(fā)部門通過工藝摸索采用硅膠吸附降低了鈀的殘留,最終獲得了CEP證書。2)、在引入元素雜質(zhì)步驟或后續(xù)某步驟采用降低元素雜質(zhì)的措施,并在該步驟的中間體質(zhì)量標(biāo)準(zhǔn)中制定元素雜質(zhì)測試指標(biāo)和限度,確保成品中的元素雜質(zhì)符合限度要求。3)、建立嚴(yán)格的原輔料元素雜質(zhì)質(zhì)量指標(biāo)和限度,從源頭控制元素雜質(zhì)引入成品中的含量。4)、若直接原料藥的包裝材料與原料藥相互作用導(dǎo)致包裝材料中的元素雜質(zhì)進(jìn)入原料藥進(jìn)而使原料藥中元素雜質(zhì)超過限度要求的,應(yīng)重新選擇更合適的包裝材料。5)、若原料藥生產(chǎn)步驟短或工藝相對比較特殊,對元素雜質(zhì)工藝控制難度大的,應(yīng)考慮原料藥的質(zhì)量標(biāo)準(zhǔn)中包含元素雜質(zhì)指標(biāo)和限度;等等。
原料藥中元素雜質(zhì)的控制策略
本公司經(jīng)過評估后對原料藥A制定了以下控制策略。一是對生產(chǎn)過程中用到的催化劑鈀炭的鈀殘留指標(biāo)訂入原料藥A的成品質(zhì)量標(biāo)準(zhǔn),限度為不得過10ppm,從而控制成品中鈀的殘留量,作為產(chǎn)品放行的常規(guī)測試指標(biāo)之一;二對1類元素砷鎘汞鉛和2A類元素,因其測試結(jié)果小于ICHQ3D限度指標(biāo)的30%,不納入原料藥A的質(zhì)量標(biāo)準(zhǔn)的常規(guī)檢測項(xiàng),但是作為帶下角星號的定期檢測項(xiàng)目,檢測頻率為2年/次,每次測試原料藥A連續(xù)三個批次,測試結(jié)果納入原料藥A的年度質(zhì)量回顧內(nèi)容并評估。同時,本公司規(guī)定至少在以下變更情況,原料藥A的元素雜質(zhì)需要重新評估,如:元素雜質(zhì)的測試方法改變;鈀炭供應(yīng)商或鈀炭濃度發(fā)生變化;鈀炭催化工序及后續(xù)工序的工藝發(fā)生變化等等。

來源:藥事縱橫


