您當前的位置:檢測資訊 > 科研開發
嘉峪檢測網 2021-05-10 11:11
本文中出現的幾個術語:
MRA:mutagen risk assessment ,誘變物風險評估。
MIs:mutagenic impurities
PMIs:potentially mutagenic impurities,含有警示結構但未經Ames確證。
降解雜質的誘變風險評估
一、穩定性研究相關的MRA
進行誘變雜質風險評估(MRA),首先是要確定降解途徑和降解產物。
強制降解研究
ICH Q1 中描述的設計完善的強制降解實驗將會產生一系列的降解產物,這些降解產物的化學結構可以包括在基因雜質的風險評估中。
不過這些降解物屬于“潛在的”,因為它們在長期和加速穩定性研究期間可能會形成,也可能不會形成。
加速穩定性研究
加速實驗的降解物也應包括在風險評估中。
加速研究可以包括一系列穩定性條件,從露天儲存到在最終包裝產品中進行的研究。這些條件下形成的降解物歸屬于“潛在降解產物”的集合中。
長期穩定性研究
長期穩定性儲存條件形成的降解物也應包括在MRA中,并歸屬于“實際降解物”集合中。

降解產物MRA的一個關鍵點是和法規要求等價,不能避重就輕,最好也不要過度研究。
應側重于主要降解途徑及其相關的主要降解物;沒有在實驗中觀察到的假設降解物將不需要包括在MRA中。
一旦確定了降解物的結構,就可以通過SAR評估,然后按照M7規則分類。
如果SAR評估為陽性,可以進行Ames實驗繼續確證。
如果Ames也為陽性,一是通過評估該降解物是否屬于藥物的活躍降解途徑,如果該降解途徑非活躍(inactive),該降解物也可以評估后不再進行研究。二是確定在有效期內究竟會產生多少量的MI,通過實際檢測值和安全限度值比較。
如果需要,可以制定相應的減緩和控制等相應策略。
使用長期和加速穩定性研究也可以代替Ames實驗。
如果該降解物在有效期內的形成水平低于安全限值,則可以不納入MRA中進行評估。
二、使用軟件預測潛在降解
在進行強制降解和相關穩定性研究之前,通過計算機軟件預測,有助于考慮潛在的降解途徑,并潛在地指導分析方法的開發。
比較常用的商業預測軟件是來自Lhasa的Zeneth,Zeneth可以借助數據庫中大量的化學原理和專業知識,從不同角度預測藥物分子的詳細降解產物。
Zeneth的最大優點是可以給出比較全面的降解產物,但同時這也是它的最大缺點。
軟件預測一般都會過度預測,很多的產物在實際中不會出現,因此強制降解實驗作為補充驗證是必不可少的。
三、通過強制降解研究選擇鑒定特定降解物
提出了三種強制降解研究的方法:
1:對加速長期產生的降解物進行鑒定
強制降解(在適當水平),以幫助指導加速和長期穩定性研究。
強制降解會導致產生更大數量的降解產物,使降解物更容易通過現有的分析方法進行檢測。
強制降解產物結構不一定都要鑒定,除非在加速或長期穩定性研究中也觀察到它們。
2:通過特定算法選取降解物進行鑒定
第二種方法利用強制降解研究來描述潛在的降解產物和途徑,結構鑒定側重于“主要”降解產物。
該算法來自于Alsante 等人的研究,將主要降解物定義為:
超過總降解物的10%以上的雜質

一次降解實驗中:API總共降解了4.46%,降解量的10%為0.446%,體系中檢測到大于0.446%的雜質有C、D和F,因此該三個雜質為主要降解雜質,需要鑒定結構。
單個最大降解雜質以及大于最大降解雜質25%的降解雜質
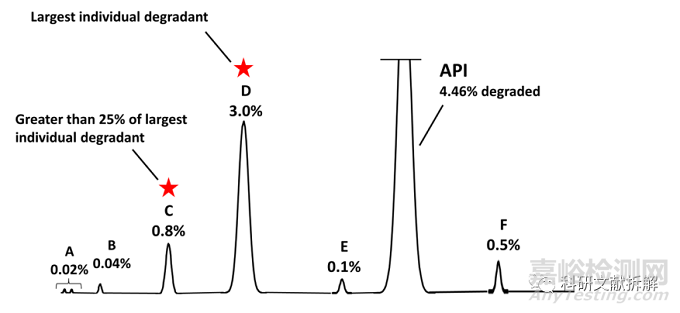
同樣一張圖,最大單雜為D,D的25%為0.75%。使用該種策略,只需要鑒定雜質C和D。
綜合兩種方案,只需要鑒定兩個雜質:
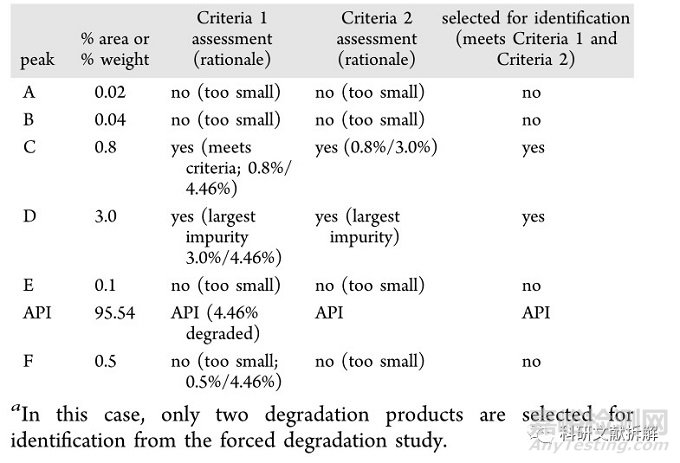
3:通過動力學等效和修正的Q3B閾值來確定降解物閾值
利用動力學等效確定儲存周期
通過 Arrhenius equation可以有效預測反應速率和溫度之間的關系,因此可以開發更加短期的實驗研究數據。
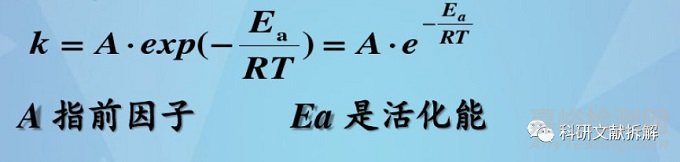
首先要了解藥物的降解活化能Ea;如果Ea值未知,根據美國藥典推薦的Ea值為19.87kcal/mol(83.14kJ/mol),作為計算平均動態溫度的保守方法。
不同Ea值對降解速率影響很大:
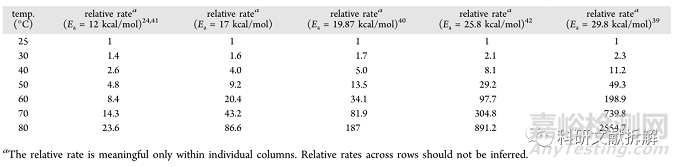
計算在40°C/75%RH下6個月動力學等效所需的天數如下:

如果溫度升高到80℃,可以在4.9天完成40℃時6個月的等效降解。
由于Arrhenius equation沒有考慮濕度對降解的影響,因此在不同溫度條件下降解研究時,應該保持濕度一致。
強制降解物的鑒定閾值制定
ICH Q1A等法規問答中對誘變降解物鑒定進行了解釋:長期穩定性研究中形成的降解物,如果低于ICH鑒定閾值,則不需要對該降解物進行結構鑒定。
根據該條說明,可以制定強制降解實驗中的降解物鑒定閾值。
保守估計藥物在有效期內降解值為2%,強制降解實驗中藥物降解率為5~10%,是正常降解的2.5~5倍。因此強制降解實驗中的降解物鑒定閾值應該是正常條件的2.5~5倍。
不同降解值對應的ID閾值。
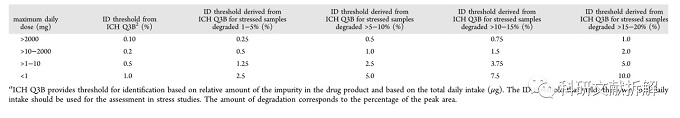
四、案例研究
案例中:
假設降解產物:根據化學機理推測
潛在降解產物:通過強制降解發現的降解產物
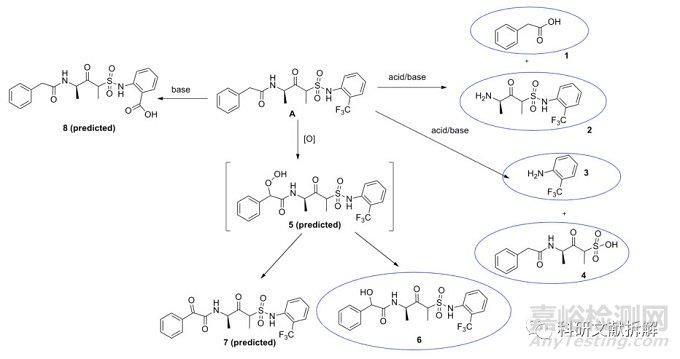
畫圈的結構是在穩定性研究中發現超過特定閾值的降解物,并已經被鑒定。
需要進行MRA的降解物
降解物1-4和6應包括在MRA中,因為它們是在強制降解和/或穩定性研究期間觀察到的。降解物7和8是假設的降解物,在強制降解期間沒有觀察到,因此不需要包括在MRA中。
降解物5是6降解途徑中的中間體,在強制降解實驗中未觀察到,根據以上理論5可能不需要包括在MRA中;但是由于API到6的降解途徑比較活躍,5是6的中間體,所以需要進一步研究確認。
降解物進行SAR評估
通過評估可以得到降解物3(苯胺結構)和5(過氧化物結構)具有突變性,因此需要對藥物在有效期內評估3和5的生成風險。
繼續評估有誘變的降解物
降解物3可以在穩定性試驗中觀察到,但是降解物5沒有觀察到。
5來源于芐基位置的自氧化,這在藥物中是一種普遍的現象,烷基過氧化物通常不穩定,會進一步形成穩定的降解產物,所以在最終產物中無法觀察到。
通過RG12915藥物的研究數據進行說明:作者在200h發現體系中存在可以測量的氫過氧化物,但是在400h時幾乎完全消失,并且在氫過氧化物消失的同時,二次氧化的產物在逐漸增加。因此可以證明中間態的氫過氧化物無法穩定的存在于最終產物中。
化合物5應該包括在風險評估中但是結論是不需要進一步評估研究。
化合物3如果降解水平較高,需要進一步研究,需要開發合適的方法將API水解生成的苯胺3控制到安全水平。
五、其他考慮因素
輔料、包裝
基于幾十年的長期使用,現有的輔料被認為是人類在醫療產品中使用的安全藥物,沒有任何重大問題。
雖然輔料本身不存在風險,但是要了解輔料在穩定性以及和藥物相容性方面的影響。
可提取物和可浸出物和藥品問題相關,可能需要評估。
參考文獻:Strategies To Address Mutagenic Impurities Derived from Degradation in Drug Substances and Drug Products
DOI:10.1021/acs.oprd.5b00091

來源:科研文獻拆解


