您當前的位置:檢測資訊 > 科研開發
嘉峪檢測網 2021-01-15 09:08
1. 溶解:是指一種或一種以上物質(溶質)以分子或離子狀態分散在另一種物質(溶劑)中形成均勻分散體系的過程;
2. 溶液:是指由溶解過程所形成的分散體系;
3. 相互作用力:范德華力、氫鍵力和偶極力;一般來說,偶極力>氫鍵力>范德華力;
4. 溶解度(solubility):指在一定溫度(氣體在一定壓力)下,在一定量溶劑中達到飽和時溶解藥物的最大量;
5. 特性溶解度(intrinsic solubility):是指不含任何雜質的化合物,在溶劑中不發生解離、締合,不與溶劑中的其他物質發生相互作用時所形成的飽和溶液的濃度;
6. 平衡溶解度(equilibrium solubility):是指在測定藥物溶解度時不排除溶劑、其他成分影響,此時測得的溶解度稱為平衡溶解度或表觀溶解度;
7. 溶出度(dissolution):系指在規定的溶劑中,藥物從片劑、膠囊等固體制劑中溶出的速度和程度。
詳細介紹
一.溶解度的測定
1.《中國藥典》2015版規定
稱取(或量取)供試品置于25℃一定容量溶劑中,每隔5min強力振搖30s,觀察30min內的溶解情況,若看不到溶質顆粒或液滴,視為完全溶解。以此判斷藥物的溶解度
2. 特性溶解度的測定
? 依據相容原理圖確定

? 以藥物濃度為縱坐標,以藥物質量/溶劑體積的比值為橫坐標,直線外推值比例為零,此時得到的即為特性溶解度;
3.平衡溶解度的測定
? 可查詢相關資料或法規得到,或用法規規定方法進行測定;

4.平衡溶解度的測定
? 溫度:兼顧貯存和使用情況(4~5℃,25℃,37℃);
? pH值:往往需要測定不同pH值時的溶解度,為溶出介質的選擇提供參考;
? 恒溫攪拌和達到平衡的時間
二.影響溶解度的因素
1. 藥物極性
? 藥物的溶解度是藥物與溶劑相互作用的結果;
? 若藥物與溶劑形成分子間氫鍵,在極性溶劑中溶解度大,但在非極性溶劑中溶解度小;
? 若藥物與溶劑形成分子內氫鍵,在極性溶劑中溶解度小,但在非極性溶劑中溶解度增大;
? (針對藥物結構)形成可溶性鹽或在分子中引入親水基團——增加水中溶解度;
2. pH值和同離子效應
? 大多數藥物為弱酸或弱堿,其溶解度與pH有關;pH值不僅能影響藥物的溶解度,還對藥物的有效性、安全性和穩定性有影響,所以在進行pH調節時應綜合考慮各方面的因素;
? 由于胃腸道較為復雜的pH梯度變化,因此,在胃腸道生理pH范圍的溶解度差的藥物,往往生物利用度低;
? 此外,一般在難溶性鹽類飽和溶液中,加入相同離子化合物時,會降低其溶解度;例如:有些鹽酸鹽類藥物+生理鹽水(0.9%氯化鈉)配伍時,溶解度會降低;
3. 溫度
? 取決于溶解過程是吸熱過程還是放熱過程;
? 若為吸熱過程,則溶解度隨溫度升高而增大;
? 若為放熱過程則相反,升高溫度,溶解度反而減小;
? 若溶解過程既不吸熱也不放熱,則溶解度不受溫度的影響;如氯化鈉的溶解;
4. 溶劑化作用和水合作用
? 藥物離子的水合作用與離子性質有關;通常情況下,陽離子與水之間的相互作用力更強;
? 離子大小和離子表面積是水分子極化的決定因素;
5. 藥物的晶型——多晶型(polymorphism)
? 多晶型:是同一物質具有兩種或兩種以上的空間排列和晶胞參數,形成多種晶型的現象;
? 不同晶型具有不同的理化特性,對藥物的溶解度和體內生物學行為影響很大;
通常,穩定型:熔點高、溶解度小;
亞穩定型或無定形:熔點低、溶解度大;
? 此外,多晶型藥物還應特別注意晶型轉化問題;
? 近年研究顯示,藥物共晶可以顯著增加藥物溶解度,如卡馬西平共晶,其溶解度提高近百倍;
6. 粒子大小
? 對于水溶性藥物和粒徑大于2μm的難溶性藥物,粒徑大小對藥物溶解度的影響不大;
? 對于難溶性藥物,粒徑小于100nm時,藥物的溶解度與粒徑大小有關;并且隨著粒徑的減小,溶解度增大;
? 目前常用的微粉化技術如氣流粉碎,僅能達到微米級別,故對藥物溶解度的影響不大;
7. 粒子的其他性質
三.增加溶解度的方法
1. 增溶(solubilization)
? 增溶劑:具有增溶作用的表面活性劑;(膠束增溶)
? 影響增溶的因素:
增溶劑種類:如極性藥物,非離子表面活性劑的HLB值越大,增溶效果越好;HLB 15~18;
藥物的性質:一般,藥物分子量越大,增溶量越少;
加入順序:一般藥物先與增溶劑混合后再加入溶劑;
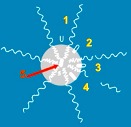
1→親水性藥物;2~4→兩親性藥物;5→疏水性藥物
2. 助溶(hydrotropy)
? 助溶劑:難溶性藥物與加入的第3種物質在溶劑中形成可溶性分子間配伍物、復鹽或締合物等以達到增加溶解度的目的,第3種物質即為助溶劑;
? 助溶劑的分類:
有機酸及其鈉鹽:如苯甲酸鈉、水楊酸等——咖啡因、核黃素等;
酰胺化合物:烏拉坦、尿素、煙酰胺等——鹽酸奎寧等;
無機鹽:如碘化鉀——碘。
3. 潛溶(cosolvency)
? 潛溶劑(cosolvent):顯著增加藥物溶解度的復合溶劑;
? 如水+極性溶劑(如乙醇、丙二醇、甘油、PEG等)(乙醇,肌注:濃度宜盡量低,減小刺激;丙二醇,口服:有辛辣不適感);
? 注意:潛溶并不是所有的比例都能顯著的增加藥物的溶解度,這種混合溶劑需要在特定的比例,特定的范圍之內才能達到最佳的增溶效果;
? 影響因素:
混合溶劑中各溶劑的不利:最佳比例需實驗確定,應注意混合及滴注過程中可能由于溶劑比例的變化,而導致溶解度變化,產生沉淀或其他不良反應;同時,滴注速度宜緩慢;
混合溶劑種類:水性注射劑,多選丙二醇、甘油、PEG,如苯巴比妥:35%苯二醇或乙醇,如尼莫地平注射液,50%乙醇。
4.制成鹽類
? 如難溶性弱酸、弱堿——成鹽
? 弱酸類:如苯巴比妥類、磺胺類——氫氧化鈉、碳酸氫鈉等堿成鹽;
? 弱堿類:普魯卡因、可卡因等——鹽酸、磷酸、枸櫞酸等酸成鹽;
? 注意問題:除了影響溶解度,還可能引起穩定性、刺激性等方面的變化;如乙酰水楊酸鈣要比乙酰水楊酸鈉更穩定;奎尼丁鹽酸鹽刺激性小于奎尼丁葡萄糖酸鹽;
5.藥物共晶
? 藥物共晶:藥物活性分子與共晶試劑通過分子間作用力(如氫鍵)形成的新晶型。——不破壞藥物共價結構;
? 例如:
卡馬西平——煙酰胺:化學穩定性提高;
呋塞米——腺嘌呤:10%乙醇溶液中的溶解度提高6~11倍;
美洛昔康——阿司匹林:溶解度提高40幾倍;
6. 其他方法
? 微粉化技術:促進溶出,但對藥物溶解度影響不大;
? 包合技術:改善水溶性;
? 固體分散技術:提高分散度,增加溶解度;
7. 補充
? 值得注意的是,在增加藥物溶解度的同事,要兼顧考慮藥物的穩定性、療效和安全性。
四.溶出速度
1. 溶出度(dissolution)
? 系指在規定的溶劑中,藥物從片劑、膠囊等固體制劑中溶出的速度和程度;
2. 溶出過程
? 溶質分子從固體表面溶解,形成飽和層;
? 經過擴散層,進入溶液內。
3.Noyes-Whitney方程
? dC/dt=kS(Cs-C);
式中,k:溶出速率常數;S:藥物顆粒表面積;Cs:藥物溶解度;
當Cs?C時,公式簡化為:dC/dt=kSCs;
漏槽條件(sink condition):即藥物溶出后立即移除,或溶出介質的量很大,溶液中的藥物濃度很低;
五.影響藥物溶出速度的因素
1. 固體的粒徑與表面積
崩解、粒徑
2. 藥物的溶出速率常數
攪拌、溫度、黏度
? 擴散系數——受介質黏度和藥物分子大小的影響;
? 擴散層厚度——攪拌;
3. 藥物的溶解度
溫度、晶型、制劑工藝
4. 劑型因素
處方、工藝

來源:艾特森制藥裝備


