您當(dāng)前的位置:檢測(cè)資訊 > 科研開(kāi)發(fā)
嘉峪檢測(cè)網(wǎng) 2025-04-22 08:58
導(dǎo) 語(yǔ)
你是否想過(guò),未來(lái)的心臟起搏器可以像米粒般微小,術(shù)后無(wú)需開(kāi)胸取器?《自然》最新研究帶來(lái)顛覆性突破!科學(xué)家團(tuán)隊(duì)研發(fā)出一款毫米級(jí)生物可吸收光電子起搏系統(tǒng),僅米粒大小(1.8×3.5×1毫米),卻集無(wú)線控制、自供電、多部位同步起搏于一身!傳統(tǒng)臨時(shí)起搏器需開(kāi)胸或血管手術(shù)植入,易引發(fā)感染、心肌損傷等風(fēng)險(xiǎn)。而這項(xiàng)“黑科技”可通過(guò)微創(chuàng)注射直接植入心肌,術(shù)后1-2年內(nèi)被人體自然吸收,免除二次手術(shù)痛苦!更神奇的是,設(shè)備搭載智能皮膚貼片,實(shí)時(shí)監(jiān)測(cè)心電圖,一旦發(fā)現(xiàn)心律失常,立即通過(guò)近紅外光無(wú)線觸發(fā)起搏,實(shí)現(xiàn)閉環(huán)精準(zhǔn)治療!
1.研究背景
在臨床醫(yī)療場(chǎng)景中,臨時(shí)起搏器是救治術(shù)后等短期心動(dòng)過(guò)緩患者的關(guān)鍵技術(shù),廣泛應(yīng)用于心臟術(shù)后護(hù)理、心梗急救及藥物過(guò)量等緊急情況,尤其對(duì)兒科和成年心臟手術(shù)患者而言不可或缺。然而,傳統(tǒng)臨時(shí)起搏器依賴心外膜或經(jīng)靜脈植入起搏導(dǎo)線,需實(shí)施開(kāi)胸手術(shù)或血管內(nèi)介入手術(shù) —— 前者伴隨術(shù)后恢復(fù)慢、住院周期長(zhǎng)及明顯手術(shù)瘢痕等問(wèn)題,后者對(duì)存在禁忌證的成年患者及體型小、生長(zhǎng)發(fā)育快的兒科患者操作難度大。此外,臨床實(shí)踐中還面臨導(dǎo)線感染、心肌撕裂穿孔、外部設(shè)備移位等并發(fā)癥風(fēng)險(xiǎn),對(duì)患者安全構(gòu)成威脅。盡管生物可吸收材料與植入設(shè)備的研究已取得進(jìn)展,但現(xiàn)有技術(shù)受限于物理尺寸、手術(shù)創(chuàng)傷、患者負(fù)擔(dān)及控制機(jī)制,難以滿足臨床對(duì)微創(chuàng)化、智能化電療設(shè)備的需求。
基于上述挑戰(zhàn),本文聚焦一種毫米級(jí)生物可吸收光電子系統(tǒng)的研發(fā),該系統(tǒng)集成內(nèi)置電源與無(wú)線光學(xué)控制機(jī)制,旨在通過(guò)超小尺寸實(shí)現(xiàn)經(jīng)皮注射、血管內(nèi)輸送等微創(chuàng)植入,為臨時(shí)心臟起搏及神經(jīng)再生、傷口治療等電療領(lǐng)域提供全新解決方案。
2.研究概述
針對(duì)傳統(tǒng)臨時(shí)起搏器依賴侵入性手術(shù)、并發(fā)癥風(fēng)險(xiǎn)高及設(shè)備移除不便等臨床痛點(diǎn),本文報(bào)道了一種毫米級(jí)生物可吸收光電子系統(tǒng),通過(guò)跨學(xué)科設(shè)計(jì)實(shí)現(xiàn)了自供電、無(wú)線光學(xué)控制與微創(chuàng)植入的創(chuàng)新融合。
該設(shè)備尺寸僅 1.8mm×3.5mm×1mm(約米粒大小),以鎂合金(陽(yáng)極)與三氧化鉬(陰極)為核心電極,利用心臟組織液作為電解質(zhì)形成原電池,通過(guò)近紅外光激活硅基光電晶體管控制電流輸出,無(wú)需外接導(dǎo)線或電池。
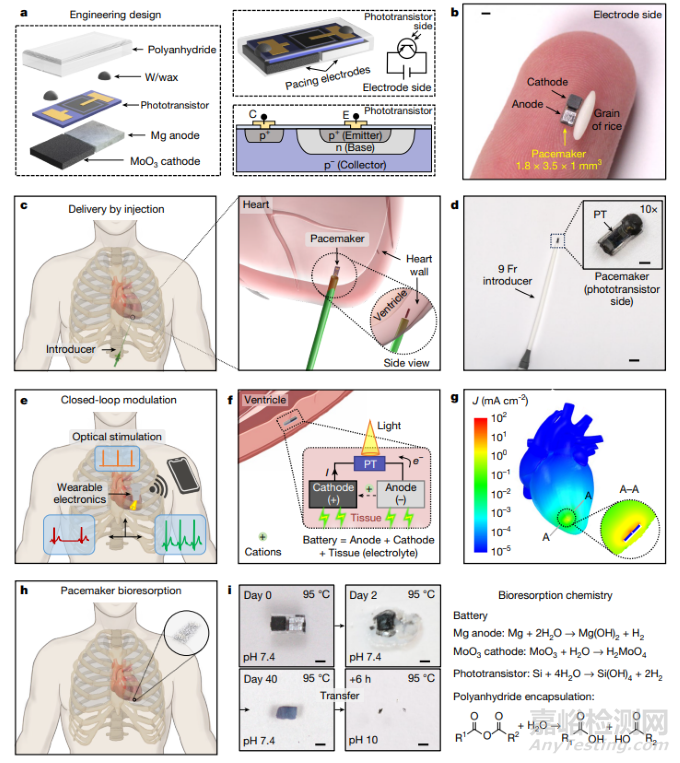
可注射、自供電、生物可吸收的無(wú)線光電子控制心臟起搏器設(shè)計(jì)
(圖片來(lái)自論文)
體外測(cè)試中,在 Langendorff 灌流的豬和人類心臟表面植入設(shè)備,證明其可通過(guò)光強(qiáng)、頻率和占空比精準(zhǔn)調(diào)控起搏電流、速率及脈沖寬度,成功實(shí)現(xiàn)單部位及多部位(左心室、右心室、希氏束)起搏。

人類和豬心臟的光電特性及離體起搏研究
(圖片來(lái)自論文)
體內(nèi)植入于小鼠、大鼠、犬類模型,經(jīng)皮注射或血管內(nèi)輸送后,近紅外光穿透皮膚激活設(shè)備,在犬類心臟實(shí)現(xiàn) 240 次 / 分穩(wěn)定起搏,閉環(huán)系統(tǒng)結(jié)合皮膚接口設(shè)備實(shí)時(shí)監(jiān)測(cè)心電圖,自動(dòng)觸發(fā)心律失常時(shí)的起搏干預(yù)。

犬類模型中起搏器注射及閉胸起搏的體內(nèi)演示
(圖片來(lái)自論文)
臨床場(chǎng)景拓展中,通過(guò)波長(zhǎng)分復(fù)用技術(shù)(WDM)實(shí)現(xiàn)雙腔及雙心室同步起搏,改善心力衰竭患者的心室電活動(dòng)同步性,并創(chuàng)新性地將多個(gè)設(shè)備集成于經(jīng)導(dǎo)管主動(dòng)脈瓣置換術(shù)(TAVR)支架,在離體人類心臟模型中驗(yàn)證了預(yù)防術(shù)后房室傳導(dǎo)阻滯的可行性。

犬類模型中多部位時(shí)間同步起搏的體內(nèi)演示
(圖片來(lái)自論文)
3.研究意義
該系統(tǒng)的核心優(yōu)勢(shì)在于:超微創(chuàng)植入(可通過(guò) < 3mm 直徑導(dǎo)管注射)、生物可吸收特性(材料降解產(chǎn)物為水溶性物質(zhì),1.2-2.5 年內(nèi)完全吸收,避免二次手術(shù)移除)、兼容性(支持 MRI/CT 成像)及多功能拓展(可適配神經(jīng)再生、傷口治療等電療場(chǎng)景)。從材料篩選(鎂 / 鋅電極、聚酸酐封裝)到機(jī)制驗(yàn)證(有限元分析電流密度、蒙特卡洛模擬光穿透深度),再到多物種模型(小鼠至人類心臟)的跨尺度實(shí)驗(yàn),研究系統(tǒng)性論證了其安全性與有效性,為短期電療設(shè)備提供了 “即置即用、無(wú)需移除” 的全新解決方案,推動(dòng)心臟起搏技術(shù)向微型化、智能化、生物整合化邁進(jìn)。
文章來(lái)源:Zhang, Y., Rytkin, E., Zeng, L. et al. Millimetre-scale bioresorbable optoelectronic systems for electrotherapy. Nature 640, 77–86 (2025). https://doi.org/10.1038/s41586-025-08726-4

來(lái)源:Internet


