您當(dāng)前的位置:檢測(cè)資訊 > 生產(chǎn)品管
嘉峪檢測(cè)網(wǎng) 2025-03-29 10:21
摘 要
堅(jiān)持“六統(tǒng)一”,控制中藥材生產(chǎn)和質(zhì)量的各種影響因素,規(guī)范中藥材生產(chǎn)全過程,中藥材全產(chǎn)業(yè)鏈質(zhì)量可追溯,是中藥材生產(chǎn)質(zhì)量管理規(guī)范(GAP)的核心。本文通過對(duì)廣東省中藥材GAP 延伸檢查情況進(jìn)行統(tǒng)計(jì)與分析,聚焦延伸檢查的內(nèi)容與流程,探討了中藥材GAP 基地建設(shè)工作中的亮點(diǎn)、普遍存在的問題和需要重視的問題,并對(duì)中藥材GAP 實(shí)施與基地建設(shè)工作提出了思考。中藥材GAP 基地投入恰當(dāng)合理、運(yùn)作模式規(guī)范適用,中藥材品質(zhì)穩(wěn)定可控、安全、有效,中藥材產(chǎn)業(yè)才能可持續(xù)發(fā)展,進(jìn)而加強(qiáng)中藥全產(chǎn)業(yè)鏈質(zhì)量管理,推動(dòng)中藥產(chǎn)業(yè)高質(zhì)量發(fā)展,促進(jìn)中醫(yī)藥傳承創(chuàng)新發(fā)展。
Ensuring the "six unifications", controlling key factors affecting the production and quality of Chinese medicinal materials, standardizing the entire production process, and achieving full traceability across the supply chain are core principles of good agricultural practice (GAP) for traditional Chinese medicine (TCM). This paper presents an analysis of GAP extended inspections conducted in Guangdong Province, focusing on key inspection aspects and processes. It highlights best practices,common challenges, and critical issues in GAP base construction and offers recommendations for improvement. A wellstructured and appropriately invested GAP base, supported by a standardized operating model, is essential to ensuring stable,controllable, safe, and effective TCM quality. Strengthening GAP implementation and base development is crucial for sustainable industry growth, improving supply chain quality management, and promoting the high-quality development of the TCM industry.
關(guān)鍵詞
中藥材;生產(chǎn)質(zhì)量管理規(guī)范;延伸檢查;廣東省;工作思考
Chinese crude drugs; good agricultural practice; extended inspection; Guangdong Province; work reflections
2021 年5 月,國(guó)家藥監(jiān)局印發(fā)《藥品檢查管理辦法(試行)》;2022 年3 月,國(guó)家藥監(jiān)局、農(nóng)業(yè)農(nóng)村部、國(guó)家林草局、國(guó)家中醫(yī)藥局聯(lián)合發(fā)布《中藥材生產(chǎn)質(zhì)量管理規(guī)范》(以下簡(jiǎn)稱新版中藥材GAP),并在公告中明確新版中藥材GAP 的實(shí)施方式為延伸檢查[1]。2023 年6 月國(guó)家藥監(jiān)局綜合司印發(fā)了《〈中藥材生產(chǎn)質(zhì)量管理規(guī)范〉監(jiān)督實(shí)施示范建設(shè)方案》,由安徽、廣東、四川、甘肅省藥品監(jiān)管部門作為任務(wù)承擔(dān)單位推進(jìn)示范建設(shè),以推進(jìn)中藥材GAP 有序?qū)嵤瑥?qiáng)化中藥材質(zhì)量控制,從源頭提升中藥質(zhì)量,促進(jìn)中藥材產(chǎn)業(yè)規(guī)范化高質(zhì)量發(fā)展。國(guó)家藥監(jiān)局食品藥品審核查驗(yàn)中心于2023 年6 月發(fā)布了《中藥材GAP 實(shí)施技術(shù)指導(dǎo)原則》《中藥材GAP 檢查指南》[2],中藥材GAP 延伸檢查是中藥材GAP 實(shí)施成效的檢查手段,其目的在于確保中藥材從種植到采收、加工、儲(chǔ)存等各環(huán)節(jié)的質(zhì)量與安全,是中藥產(chǎn)業(yè)健康、有序發(fā)展的重要保障與基礎(chǔ)。
2023 年7 月廣東省藥監(jiān)局印發(fā)《推進(jìn)〈中藥材生產(chǎn)質(zhì)量管理規(guī)范〉監(jiān)督實(shí)施示范建設(shè)工作實(shí)施細(xì)則》,對(duì)工作目標(biāo)、重點(diǎn)任務(wù)、進(jìn)度安排、任務(wù)分工、工作要求進(jìn)行了詳細(xì)部署。2023 年8月廣東省藥監(jiān)局組建中藥材GAP監(jiān)督實(shí)施示范建設(shè)專家工作組,明確中藥材GAP 專家包括從事中藥材種子種苗研究、種植/ 養(yǎng)殖、采收加工、質(zhì)量控制及品質(zhì)評(píng)價(jià)和行政管理等領(lǐng)域的專業(yè)人員。
中藥材GAP 延伸檢查的實(shí)施涉及多個(gè)層面和環(huán)節(jié),注重從源頭上把控中藥材質(zhì)量。通常包括對(duì)企業(yè)申報(bào)材料的審查、現(xiàn)場(chǎng)檢查、記錄與文件檢查、質(zhì)量追溯體系檢查等多個(gè)方面,從而對(duì)中藥材生產(chǎn)企業(yè)的質(zhì)量管理體系、生產(chǎn)環(huán)境、種植技術(shù)、采收加工等方面進(jìn)行全面評(píng)估。現(xiàn)場(chǎng)檢查主要關(guān)注中藥材生產(chǎn)基地的環(huán)境條件、種植技術(shù)、采收加工等,以確保其符合GAP 的要求;文件審查側(cè)重于查看企業(yè)的質(zhì)量管理體系文件、操作規(guī)程、培訓(xùn)記錄、內(nèi)審與自檢記錄等,以驗(yàn)證企業(yè)質(zhì)量管理體系的適用性與規(guī)范性;質(zhì)量追溯體系則是確保中藥材從種植源頭到工業(yè)使用端的每一個(gè)環(huán)節(jié)都能得到有效監(jiān)控和可追溯,從而保障中藥材生產(chǎn)全環(huán)節(jié)的質(zhì)量安全,同時(shí)對(duì)每批中藥材的質(zhì)量進(jìn)行取樣檢測(cè),進(jìn)一步確認(rèn)中藥材的內(nèi)在質(zhì)量。本文通過對(duì)2023~2024 年廣東省中藥材GAP 延伸檢查情況進(jìn)行分析,總結(jié)了基地建設(shè)的成效與不足,并給出了工作思考及建議,以期為推進(jìn)中藥材規(guī)范化種植和產(chǎn)業(yè)高質(zhì)量發(fā)展提供決策參考。
1. 檢查實(shí)踐與工作亮點(diǎn)
1.1 檢查實(shí)踐
廣東省于2023 年8 月啟動(dòng)GAP 延伸檢查工作,遴選出8 家企業(yè)重點(diǎn)中藥材品種21 個(gè)(扣除不同企業(yè)的相同中藥材品種數(shù),實(shí)際涉及中藥材品種為19 種),均為植物類中藥材品種。8 家企業(yè)包括中藥配方顆粒生產(chǎn)企業(yè)2家、中藥注射劑生產(chǎn)企業(yè)2 家以及其他中成藥生產(chǎn)企業(yè)4 家。當(dāng)前,8 家企業(yè)21 個(gè)重點(diǎn)中藥材品種已進(jìn)行了GAP 延伸檢查(流程見圖1),企業(yè)對(duì)缺陷項(xiàng)目進(jìn)行整改并提交整改報(bào)告。經(jīng)專家評(píng)審,最后提交廣東省藥監(jiān)局審評(píng)審批,8 家企業(yè)21 個(gè)品種均能達(dá)到GAP 要求[3-14]。

1.2 工作亮點(diǎn)
1.2.1 延伸檢查機(jī)制創(chuàng)新
廣東省藥監(jiān)局藥品檢查中心創(chuàng)新檢查機(jī)制,充分發(fā)揮中藥材GAP 專家在中藥材良種、良田、良法、良采等農(nóng)學(xué)領(lǐng)域的專業(yè)特長(zhǎng),探索性組建由中藥材GAP專家、藥品監(jiān)管部門人員、藥品檢驗(yàn)機(jī)構(gòu)人員等組成的中藥材GAP 延伸檢查組,實(shí)現(xiàn)中藥材GAP 延伸檢查全面覆蓋各板塊專業(yè)技術(shù)要點(diǎn),全面檢查被檢查對(duì)象GAP 全環(huán)節(jié)實(shí)施情況。
1.2.2 中藥材GAP 延伸檢查準(zhǔn)備工作充分、檢查后整改積極到位
所有企業(yè)檢查工作準(zhǔn)備都很充分,配備了熟悉基地種植情況和質(zhì)量管理的技術(shù)人員專門跟蹤檢查組的檢查。部分企業(yè)的技術(shù)人員對(duì)中藥材GAP 檢查指南非常熟悉,檢查文件資料按照檢查章節(jié)進(jìn)行整理,方便檢查人員查閱,大大提高了工作效率,檢查員可以及時(shí)準(zhǔn)確地找到所需的文件、記錄。對(duì)于檢查組現(xiàn)場(chǎng)檢查中發(fā)現(xiàn)的缺陷項(xiàng)目,大部分企業(yè)都能立即落實(shí)整改,部分企業(yè)不能立即整改、需要一定周期進(jìn)行改進(jìn)的,也都制定了切實(shí)可行的整改計(jì)劃方案。
1.2.3 種質(zhì)資源收集、種苗自繁技術(shù)、種植模式的探索
廣東省云浮市的國(guó)家南藥種苗繁育標(biāo)準(zhǔn)化示范區(qū)建立了三叉苦、廣藿香種質(zhì)資源圃,從廣東、廣西、云南等主產(chǎn)地收集了不同地區(qū)的三叉苦野生種質(zhì)資源17份;從肇慶高要、四會(huì),茂名化州、電白,陽江陽春,海南萬寧等地收集到廣藿香種質(zhì)資源15 份。
三叉苦、九里香、崗梅、兩面針相關(guān)企業(yè)摸索了種苗自繁技術(shù),并申請(qǐng)了多個(gè)專利和團(tuán)體標(biāo)準(zhǔn);種苗選育方面,九里香選育品種“999華香01”“999 華香02”和崗梅選育品種“999 華崗01”已獲得國(guó)家林草局植物新品種權(quán)授權(quán);采用組織培養(yǎng)技術(shù),實(shí)現(xiàn)了廣藿香種苗的快速繁殖,并選擇出優(yōu)良植株,通過穴盤快繁技術(shù)進(jìn)行批量化操作,提高了育苗效率,可規(guī)模化快速繁育優(yōu)良一致的種苗。
金銀花種植基地由原有的散戶粗放式種植,逐步形成了“中藥生產(chǎn)企業(yè)+ 中藥材生產(chǎn)企業(yè)+產(chǎn)地加工”的優(yōu)質(zhì)原料供應(yīng)鏈體系和以優(yōu)質(zhì)種苗繁育、規(guī)范化種植管理、集中采摘加工的核心示范基地為主,協(xié)同帶動(dòng)周邊種植合作社、農(nóng)戶的基地生產(chǎn)模式,進(jìn)一步保證藥材質(zhì)量,提升品種價(jià)值。
1.2.4 倉(cāng)儲(chǔ)新技術(shù)的研究與應(yīng)用
以黨參為例,利用氣調(diào)養(yǎng)護(hù)技術(shù)長(zhǎng)期保存對(duì)黨參藥材的質(zhì)量穩(wěn)定起到了良好作用。其做法是將待儲(chǔ)存的黨參包裝后放置于多層共擠復(fù)合膜底套上,然后在待儲(chǔ)存物表面放氣調(diào)劑、干燥劑等;最后將復(fù)合膜熱封,形成密閉空間。氣調(diào)劑短時(shí)間內(nèi)將密閉空間內(nèi)氧氣反應(yīng)消除,基本達(dá)到無氧儲(chǔ)存狀態(tài)并長(zhǎng)期維持穩(wěn)定。氣調(diào)養(yǎng)護(hù)技術(shù)的優(yōu)點(diǎn)是可隔絕空氣,長(zhǎng)期維持低氧儲(chǔ)存,儲(chǔ)存過程不受環(huán)境濕度的影響,可防蟲、防霉、抑制微生物生長(zhǎng)、降低有效成分氧化分解速度;過程中使用的氣調(diào)劑主要成分為亞鐵離子,可與氧氣反應(yīng),使氧氣含量極低,無化學(xué)藥劑殘留,綠色環(huán)保。
但氣調(diào)養(yǎng)護(hù)技術(shù)也存在一定的不足,比如應(yīng)用時(shí)需提前將待儲(chǔ)存物規(guī)則擺放,且不能有堅(jiān)硬部位露出,否則儲(chǔ)存期間會(huì)破壞復(fù)合膜,影響儲(chǔ)存效果;另外,該技術(shù)的復(fù)合膜與氣調(diào)劑均為一次性消耗品,成本較高。因此,各中藥材企業(yè)需根據(jù)中藥材的不同特性,自主探索適合本企業(yè)的倉(cāng)儲(chǔ)技術(shù)。
1.2.5 中藥材野生轉(zhuǎn)仿野生種植、野生轉(zhuǎn)家種卓有成效
黃芪的野生轉(zhuǎn)仿野生種植,崗梅、三叉苦的野生轉(zhuǎn)家種,既降低了對(duì)野生中藥材環(huán)境的破壞,也能保證中藥材的質(zhì)量。種植技術(shù)規(guī)程合理,可操作性強(qiáng)。符合GAP 種植的中藥材“專供”下游中成藥,可從源頭上保證藥品的質(zhì)量安全。
1.2.6 文件體系完整,中藥生產(chǎn)企業(yè)質(zhì)量管理體系延伸到中藥材產(chǎn)地
部分企業(yè)的GAP 管理體系完整、文件規(guī)范,中藥生產(chǎn)企業(yè)與中藥材生產(chǎn)企業(yè)管理銜接精準(zhǔn)流暢,基地管理人員、工作人員等對(duì)GAP 要求掌握熟練,對(duì)種植基地的培訓(xùn)、監(jiān)督落實(shí)到位。
2. 存在問題分析
《中藥材GAP 檢查指南》中的“第二節(jié) 檢查要點(diǎn)”共有13 章,植物類藥材檢查要點(diǎn)共183 項(xiàng)[2]。檢查結(jié)果的判定參照國(guó)家藥監(jiān)局發(fā)布的《藥品生產(chǎn)現(xiàn)場(chǎng)檢查風(fēng)險(xiǎn)評(píng)定指導(dǎo)原則》執(zhí)行,缺陷分為“嚴(yán)重缺陷”“主要缺陷”和“一般缺陷”。
按照GAP 延伸檢查要點(diǎn),分析檢查中發(fā)現(xiàn)的主要問題。本文列出了檢查中缺陷項(xiàng)目出現(xiàn)頻次較高的條款及對(duì)應(yīng)的條款編號(hào),分析問題產(chǎn)生的原因并嘗試提出改進(jìn)方法。
2.1 質(zhì)量管理部分
大部分植物類中藥材由于其自身的特點(diǎn),需要擴(kuò)展種植區(qū)域,進(jìn)行輪種,以保證質(zhì)量與產(chǎn)量,實(shí)現(xiàn)可持續(xù)發(fā)展。但是部分企業(yè)在進(jìn)行種植前質(zhì)量風(fēng)險(xiǎn)評(píng)估時(shí),沒有輪種研究及輪種方案,沒有長(zhǎng)期發(fā)展規(guī)劃,沒有提供種植品種本身環(huán)境適應(yīng)性的相關(guān)文獻(xiàn)材料(0201)。此外,部分企業(yè)的質(zhì)量管理體系中,對(duì)種植基地生產(chǎn)單元未建立有效的監(jiān)督管理機(jī)制(0203),對(duì)基地的巡查記錄不完善(0204),不能確保對(duì)中藥材生產(chǎn)基地關(guān)鍵環(huán)節(jié)進(jìn)行現(xiàn)場(chǎng)指導(dǎo)和監(jiān)督。種植周期中,不同年份種苗有自留種與外購(gòu)種,種苗未做到完全統(tǒng)一(0205)。中藥材生產(chǎn)質(zhì)量追溯體系有待完善,對(duì)農(nóng)業(yè)投入品(如肥料、農(nóng)藥)施用追溯內(nèi)容不完善(0208),例如施用投入品的名稱、批號(hào)等信息記錄不全。
2.2 設(shè)施、設(shè)備與工具部分
部分企業(yè)自身的加工場(chǎng)地?zé)o法匹配基地產(chǎn)能,如采收時(shí)曬場(chǎng)面積不夠(0401);臨時(shí)曬場(chǎng)防鳥、防禽畜措施不足(0808);加工場(chǎng)所生產(chǎn)設(shè)備狀態(tài)標(biāo)識(shí)不完善,維護(hù)保養(yǎng)措施不足(0409)。GAP 要求配備必要的設(shè)施,包括但不限于種植或者養(yǎng)殖設(shè)施、產(chǎn)地加工設(shè)施、中藥材貯存?zhèn)}庫(kù)、包裝設(shè)施,要求有遮陽、防雨、防鼠、防塵、防蟲、防禽畜措施。初加工是藥用部位收獲后至形成中藥材的過程,是保證中藥材質(zhì)量的重要環(huán)節(jié)之一。絕大多數(shù)藥材需要在產(chǎn)地進(jìn)行初加工,目的是清除異物,將藥材“殺青”、干燥,以便運(yùn)輸和貯藏。加工場(chǎng)地通常應(yīng)就近設(shè)置,環(huán)境須寬敞、整潔、通風(fēng)良好并配備相應(yīng)設(shè)施、設(shè)備。
2.3 基地選址部分
部分中藥材種植基地的空氣質(zhì)量情況無氣象部門監(jiān)測(cè)數(shù)據(jù)(0506);無土壤檢驗(yàn)檢測(cè)報(bào)告、無禁用農(nóng)藥調(diào)查情況報(bào)告(0507)。中藥材生產(chǎn)基地的選擇對(duì)藥材質(zhì)量具有關(guān)鍵性作用,藥材生產(chǎn)需要在適宜的環(huán)境條件下進(jìn)行,中藥材種植應(yīng)選擇空氣、水、土壤未受污染,農(nóng)業(yè)生態(tài)環(huán)境質(zhì)量良好的地區(qū)。企業(yè)應(yīng)按照國(guó)家有關(guān)標(biāo)準(zhǔn)定期收集大氣、水、土壤質(zhì)量檢測(cè)數(shù)據(jù),并評(píng)估中藥材種植的適宜性。有些藥材在采挖的過程中容易出現(xiàn)水土流失等生態(tài)環(huán)境問題,企業(yè)應(yīng)提高對(duì)保護(hù)生態(tài)環(huán)境的重視程度,并采取相應(yīng)措施,實(shí)現(xiàn)生態(tài)種植。
2.4 種子種苗或其他繁殖材料部分
部分企業(yè)種子種苗管理規(guī)范性方面相對(duì)較弱。如基原報(bào)告不規(guī)范(0601),表現(xiàn)為:基原報(bào)告只有文字描述,無圖片記錄;無標(biāo)本采集地點(diǎn)、標(biāo)本份數(shù)等記錄,或者記錄的樣本數(shù)量不規(guī)范(樣本只有1 份,不具有重復(fù)性);鑒定植物特征完全按照《中國(guó)植物志》的描述,沒有針對(duì)植物特征配以相應(yīng)的圖片進(jìn)行描述鑒定,或鑒定依據(jù)是蠟葉標(biāo)本而描述的特征在標(biāo)本上根本沒有;鑒定人未手寫簽名等。建議建立并使用統(tǒng)一的基原報(bào)告模板,包括基原植物性狀特征(配照片),或蠟葉標(biāo)本性狀特征,復(fù)雜品種需要佐以顯微鑒定等。企業(yè)購(gòu)買的種苗無基原鑒定記錄(0603);種苗標(biāo)準(zhǔn)過于簡(jiǎn)單,流于形式,可操作性不強(qiáng), 或缺少種苗分級(jí)的具體標(biāo)準(zhǔn), 如種苗苗齡、苗高、地徑等, 不利于實(shí)際操作(0606);種子種苗檢驗(yàn)報(bào)告不規(guī)范(0610)。良種繁育問題普遍不重視,未建立中藥材種子種苗或其他繁殖材料的良種繁育規(guī)程(0607)。種子種苗產(chǎn)地不能做到明確、固定(0609),跨縣域檢疫證明不規(guī)范或缺失(0611)。
GAP 要求種子種苗等繁殖材料應(yīng)制定檢驗(yàn)及檢疫制度,在生產(chǎn)、轉(zhuǎn)運(yùn)過程中進(jìn)行檢驗(yàn)及檢疫并出具報(bào)告書,種子種苗是中藥材生產(chǎn)最重要的生產(chǎn)資料,應(yīng)嚴(yán)格按照《中華人民共和國(guó)種子法》等相關(guān)法規(guī)的要求制定相應(yīng)的檢驗(yàn)檢疫制度并實(shí)施。
2.5 種植與養(yǎng)殖部分
投入品管理欠規(guī)范是較多企業(yè)出現(xiàn)的問題。不少企業(yè)使用自制有機(jī)肥,但未制定有機(jī)肥制作及使用技術(shù)規(guī)程(0702);較多企業(yè)未制定突發(fā)性病蟲害等的防治預(yù)案(0704);沒有對(duì)種植技術(shù)規(guī)程中的一些技術(shù)條件做探索性研究,以確定最佳種植模式(如播種、套種、輪種等方式)(0710)。企業(yè)對(duì)種植模式進(jìn)行優(yōu)化探索,有利于提高中藥材種植的產(chǎn)量和質(zhì)量,提高種植收益。部分企業(yè)在購(gòu)置農(nóng)藥、肥料等農(nóng)業(yè)投入品時(shí)缺少供應(yīng)商資質(zhì)和合格證、品牌、種類等信息(0712)。部分企業(yè)未按照技術(shù)規(guī)程使用農(nóng)藥,未開展針對(duì)性培訓(xùn)、指導(dǎo)和巡檢(0718)。GAP 要求對(duì)從事中藥材生產(chǎn)的有關(guān)人員進(jìn)行定期培訓(xùn)與考核,企業(yè)應(yīng)加強(qiáng)對(duì)各類人員的技術(shù)培訓(xùn),不斷提高規(guī)范化種植水平。建議根據(jù)不同層次的培訓(xùn)對(duì)象,制定科學(xué)合理的培訓(xùn)計(jì)劃。培訓(xùn)內(nèi)容應(yīng)規(guī)范實(shí)用,輔以必要的考核,注重實(shí)效。種植基地的各級(jí)人員,包括管理人員、檢驗(yàn)人員、技術(shù)人員、田間工作人員等,均應(yīng)接受規(guī)定的培訓(xùn)。
2.6 采收與產(chǎn)地加工部分
采收期管理、加工設(shè)施與過程管控等方面存在易被企業(yè)忽視的問題。
采收環(huán)節(jié):部分企業(yè)沒有按照傳統(tǒng)采收要求采收,但又沒有現(xiàn)代研究數(shù)據(jù)來證明采收規(guī)程與對(duì)應(yīng)標(biāo)準(zhǔn)要求不一致的合理性,未明確采收年限范圍,未確定基于物候期的適宜采收時(shí)間并明確規(guī)定采收期(0801、0802)。此外,采收的具體操作(如采收時(shí)間、采收標(biāo)準(zhǔn))與藥品標(biāo)準(zhǔn)或者企業(yè)標(biāo)準(zhǔn)不完全一致也有培訓(xùn)不到位的原因(0309 )。
加工環(huán)節(jié):人員健康管理、防鼠措施等是容易被忽略的方面(0311、0833);加工技術(shù)規(guī)程需要進(jìn)一步完善(0801);中藥材采收后未及時(shí)運(yùn)輸?shù)郊庸?chǎng)地,對(duì)藥材采收后到進(jìn)行初加工的過程未規(guī)定合理的時(shí)限(0820)。
2.7 文件部分
部分企業(yè)中藥材生產(chǎn)過程記錄不完整,沒有按生產(chǎn)單元進(jìn)行記錄,沒有覆蓋生產(chǎn)過程的主要環(huán)節(jié),必要照片或者圖像等佐證資料不足, 可追溯性不強(qiáng), 電子追溯系統(tǒng)終端可操作性不強(qiáng)(1009);中藥材種植記錄過于簡(jiǎn)單,未包括一些重要環(huán)節(jié),如農(nóng)藥、肥料的施用時(shí)間、施用量和施用方法等(1010)。
GAP 要求每種中藥材的生產(chǎn)全過程關(guān)鍵環(huán)節(jié)均應(yīng)詳細(xì)記錄,必要時(shí)可附照片或圖像。企業(yè)應(yīng)該記錄每批中藥材在生產(chǎn)中各工序的情況,電子追溯系統(tǒng)應(yīng)當(dāng)易于現(xiàn)場(chǎng)終端操作。
2.8 質(zhì)量檢驗(yàn)部分
部分企業(yè)未能提供購(gòu)買的種子種苗的檢驗(yàn)記錄, 未向供應(yīng)商索取合格證或質(zhì)量檢驗(yàn)報(bào)告(1103);委托檢驗(yàn)無委托檢驗(yàn)合同(1104)。
2.9 小結(jié)
綜合分析現(xiàn)場(chǎng)檢查及企業(yè)反饋的問題,主要集中在以下10 個(gè)方面:①選址與生產(chǎn)未充分考慮生態(tài)環(huán)境保護(hù)。②中藥材品種環(huán)境適生性、道地性論證不充分。③種植周期良種選育未得到充分重視。④基原鑒定報(bào)告不規(guī)范,科學(xué)性、嚴(yán)謹(jǐn)性不夠。⑤對(duì)農(nóng)藥、化肥等農(nóng)業(yè)投入品施用的統(tǒng)一化培訓(xùn)不充分。⑥購(gòu)買種苗無基原鑒定記錄,種苗標(biāo)準(zhǔn)過于簡(jiǎn)單,專屬性要求不明確。⑦技術(shù)規(guī)程制定不夠細(xì)化,可操作性不強(qiáng)。⑧中藥材生產(chǎn)全過程記錄不完善,可追溯性有待加強(qiáng)。⑨政策支持力度不夠,對(duì)符合GAP 要求的中藥材、中藥飲片及中成藥,在招標(biāo)采購(gòu)及其他市場(chǎng)活動(dòng)中,尚不能充分體現(xiàn)“優(yōu)質(zhì)優(yōu)先、優(yōu)質(zhì)優(yōu)價(jià)”。⑩針對(duì)野生中藥材GAP如何實(shí)施與認(rèn)定,目前尚無明確的技術(shù)性指南。
3. 工作思考
3.1 確立中藥材GAP 實(shí)施的正確路徑與方向
各地藥品監(jiān)管、農(nóng)業(yè)農(nóng)村、林草、中醫(yī)藥管理等相關(guān)部門應(yīng)形成合力,同時(shí)需加強(qiáng)培訓(xùn)與宣傳,提高企業(yè)和社會(huì)公眾對(duì)中藥材GAP 的認(rèn)識(shí)和理解。在推進(jìn)中藥材GAP 的實(shí)踐過程中引入生態(tài)農(nóng)業(yè)的理念與方法[15],發(fā)展中藥生態(tài)農(nóng)業(yè),對(duì)落實(shí)國(guó)家中藥農(nóng)業(yè)發(fā)展各項(xiàng)部署、轉(zhuǎn)變中藥農(nóng)業(yè)發(fā)展方式、加強(qiáng)農(nóng)業(yè)生態(tài)治理等意義重大。中藥材GAP 的實(shí)施要大力推廣生態(tài)種植,促進(jìn)生態(tài)保護(hù)與經(jīng)濟(jì)發(fā)展協(xié)調(diào)統(tǒng)一[16],要嚴(yán)格在生產(chǎn)基地選址和建設(shè)、農(nóng)藥使用、肥料使用、藥材采收、藥材初加工等方面把關(guān),以實(shí)現(xiàn)中藥材生產(chǎn)可持續(xù)發(fā)展。不能僅為了追求經(jīng)濟(jì)效益而破壞環(huán)境,只有中藥材基地持續(xù)健康發(fā)展,才能保證中藥材質(zhì)量安全均一、供給穩(wěn)定可控。
3.2 建立健全質(zhì)量管理體系
中藥材的質(zhì)量受多種因素影響,如種植環(huán)境、采收時(shí)機(jī)、加工方法等,因此需要建立更加科學(xué)、系統(tǒng)的質(zhì)量管理體系,以確保中藥材質(zhì)量的穩(wěn)定性和可控性。必須提高企業(yè)的GAP 質(zhì)量管理水平和意識(shí),強(qiáng)化中藥材生產(chǎn)企業(yè)的主體責(zé)任。企業(yè)應(yīng)嚴(yán)格按照GAP 標(biāo)準(zhǔn)進(jìn)行生產(chǎn)和管理,加強(qiáng)內(nèi)部質(zhì)量控制和風(fēng)險(xiǎn)管理,確保中藥材的質(zhì)量安全,建立健全質(zhì)量管理體系[17-18]。
首先,作為生產(chǎn)主體,企業(yè)必須把工作重心放在生產(chǎn)的每一個(gè)環(huán)節(jié)上。企業(yè)應(yīng)當(dāng)配備足夠數(shù)量并具有和崗位職責(zé)相對(duì)應(yīng)資質(zhì)的生產(chǎn)和質(zhì)量管理人員。中藥生產(chǎn)企業(yè)必須對(duì)建設(shè)的中藥材GAP基地進(jìn)行整體規(guī)劃,明確基地建設(shè)的目標(biāo)和措施,制定相應(yīng)的制度、規(guī)程等,并形成文件體系加以確定,即“ 寫我要做”。其次,企業(yè)一定要基于基地建設(shè)的實(shí)際情況,實(shí)事求是確定目標(biāo)和措施,標(biāo)準(zhǔn)不能低于新版中藥材GAP的要求,也不要制定難以達(dá)成的目標(biāo)、提出后續(xù)無法做到的措施,一旦“寫”下了要做的內(nèi)容,后續(xù)就一定要實(shí)施,不能漏,不能少。企業(yè)應(yīng)當(dāng)按所“寫”內(nèi)容,包括目標(biāo)和措施等,開展基地建設(shè)和生產(chǎn)。堅(jiān)決實(shí)施所“寫”內(nèi)容,即“做我所寫”。最后,重要環(huán)節(jié)必須重點(diǎn)把控,如農(nóng)藥、化肥的使用一定要有規(guī)范統(tǒng)一的培訓(xùn),種植、采收與加工要根據(jù)技術(shù)標(biāo)準(zhǔn)來做,不能隨意更改技術(shù)流程和標(biāo)準(zhǔn)。保證中藥材生產(chǎn)、質(zhì)量控制、質(zhì)量保證等活動(dòng)可控可追溯,按照實(shí)際情況記錄關(guān)鍵環(huán)節(jié)的操作和數(shù)據(jù),保證記錄真實(shí)完整,記錄所做過程的關(guān)鍵數(shù)據(jù),即“記我所做”,使中藥材種植、采收、加工、儲(chǔ)運(yùn)全環(huán)節(jié)可追溯。
3.3 良種選育,構(gòu)建“四良體系”
2002 年發(fā)布的《中藥材生產(chǎn)質(zhì)量管理規(guī)范(試行)》就指出藥材種子種苗是最薄弱的環(huán)節(jié),進(jìn)行種質(zhì)資源優(yōu)化是最為重要的工作之一。栽培技術(shù)不成熟導(dǎo)致的中藥材GAP 規(guī)模生產(chǎn)風(fēng)險(xiǎn)較大[19-20]。在GAP 延伸檢查中發(fā)現(xiàn),種子種苗問題目前仍是藥材生產(chǎn)過程中最容易忽視的問題。“六統(tǒng)一”中種子種苗的統(tǒng)一是根本,多數(shù)企業(yè)對(duì)于種子種苗的繁育重視程度不夠。優(yōu)質(zhì)的種子種苗是優(yōu)質(zhì)藥材的前提條件,品種不夠優(yōu)良,產(chǎn)量不高,藥材品質(zhì)不夠好,投入與產(chǎn)出就無法符合經(jīng)濟(jì)效益模式。此外,選址不當(dāng)(環(huán)境污染、環(huán)境破壞等),氣候環(huán)境不適宜(GAP 要求有種植史、一般應(yīng)當(dāng)選址于道地產(chǎn)區(qū),在非道地產(chǎn)區(qū)選址應(yīng)當(dāng)提供充分文獻(xiàn)或者科學(xué)依據(jù)證明其適宜性),以及種植、采收及加工方法不當(dāng)?shù)龋矔?huì)影響產(chǎn)量和質(zhì)量。
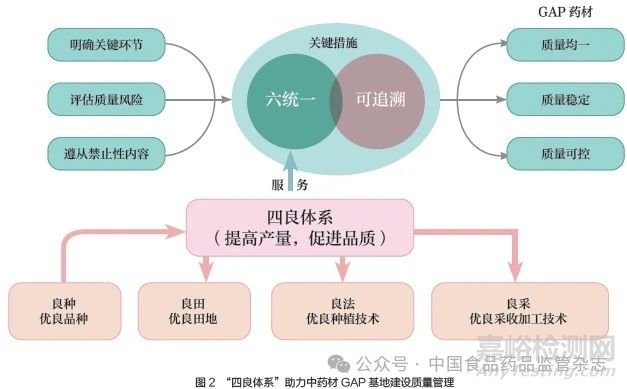
為了企業(yè)中藥材種植與收獲長(zhǎng)期穩(wěn)定、優(yōu)質(zhì),本文擬制了中藥材生產(chǎn)“四良體系”(良種、良田、良法、良采)模式以供參考,如圖2 所示。堅(jiān)持“四良體系”,更具體地落實(shí)中藥材GAP 基地各項(xiàng)工作,基地建設(shè)才能進(jìn)入良性循環(huán),持續(xù)生產(chǎn)出優(yōu)質(zhì)的中藥材。在藥材種植過程中,中藥企業(yè)的關(guān)注點(diǎn)側(cè)重于藥材的質(zhì)量,而種植戶和中藥材生產(chǎn)企業(yè)則側(cè)重于產(chǎn)量。建議相關(guān)企業(yè)建立相應(yīng)的中藥基原植物種質(zhì)資源圃及良種繁育基地,開展區(qū)域栽培試驗(yàn)、品種選育等研究,選育出優(yōu)質(zhì)高產(chǎn)、抗逆性強(qiáng)的優(yōu)勢(shì)品種。
3.4 部門協(xié)同,政策支持
中藥材GAP 延伸檢查涉及多個(gè)部門和環(huán)節(jié),應(yīng)加強(qiáng)各監(jiān)管部門之間的協(xié)作與配合,形成中藥材質(zhì)量監(jiān)管合力。不管是進(jìn)行GAP 基地的建設(shè),還是對(duì)于日常推行GAP 的維護(hù),均需要花費(fèi)大量的人力、物力、財(cái)力,且投資大、周期長(zhǎng),按照GAP 標(biāo)準(zhǔn)種植出來的中藥材,在生產(chǎn)種植成本上高于一般中藥材,但目前沒有相關(guān)政策措施保障符合GAP 標(biāo)準(zhǔn)的中藥材及人工制成品在招標(biāo)采購(gòu)中“優(yōu)質(zhì)優(yōu)先、優(yōu)質(zhì)優(yōu)價(jià)”,建議相關(guān)部門結(jié)合實(shí)際情況,制定相應(yīng)正面激勵(lì)措施并加強(qiáng)組織實(shí)施。此外,當(dāng)企業(yè)遇到技術(shù)難題時(shí)可予以技術(shù)指導(dǎo)或服務(wù)。例如,廣東的企業(yè)科技特派員制度有助于企業(yè)獲得更科學(xué)的種植、采收加工等技術(shù)指導(dǎo);廣東省藥監(jiān)局于2019 年開展的“中藥飲片全產(chǎn)業(yè)鏈質(zhì)量標(biāo)準(zhǔn)體系構(gòu)建”(編號(hào)2019KT1261)課題研究,加強(qiáng)了產(chǎn)學(xué)研合作,幫助了中藥相關(guān)企業(yè)中藥飲片全產(chǎn)業(yè)鏈質(zhì)量標(biāo)準(zhǔn)體系的構(gòu)建;廣東省的“百縣千鎮(zhèn)萬村高質(zhì)量發(fā)展工程”等相關(guān)政策措施,可以有效促進(jìn)GAP 工作的實(shí)施與開展。醫(yī)保部門、集采平臺(tái)對(duì)于通過GAP 延伸檢查、有 GAP 標(biāo)識(shí)的相關(guān)品種,可以給予“優(yōu)質(zhì)優(yōu)先、優(yōu)質(zhì)優(yōu)價(jià)”激勵(lì)措施;鼓勵(lì)GAP 實(shí)施主體申報(bào)農(nóng)業(yè)補(bǔ)貼和相關(guān)優(yōu)惠政策;行政服務(wù)方面(相關(guān)社會(huì)服務(wù)職責(zé)履行到位),如農(nóng)業(yè)農(nóng)村部門的跨縣域種子種苗檢疫,科技部門可出臺(tái)政策支持GAP 基地建設(shè)主體的良種繁育課題、種植技術(shù)優(yōu)化課題;優(yōu)化技術(shù)服務(wù),如廣東省科技廳、廣東省農(nóng)業(yè)農(nóng)村廳、廣東省教育廳均出臺(tái)政策和服務(wù)項(xiàng)目支持“百縣千鎮(zhèn)萬村高質(zhì)量發(fā)展工程”“嶺南中草藥種質(zhì)資源庫(kù)建設(shè)”“廣東南藥種植技術(shù)服務(wù)中心的建設(shè)”等項(xiàng)目。
GAP 的實(shí)施要堅(jiān)持產(chǎn)學(xué)研結(jié)合,強(qiáng)化科技支撐引領(lǐng)作用,加強(qiáng)中藥材種植關(guān)鍵技術(shù)的研究,提高中藥材種植水平,做到在優(yōu)質(zhì)基礎(chǔ)上高產(chǎn),在高產(chǎn)基礎(chǔ)上優(yōu)質(zhì)。建議由各地科技部門和農(nóng)業(yè)農(nóng)村部門牽頭,藥品監(jiān)管、經(jīng)貿(mào)等部門參與,組織有關(guān)專家對(duì)中藥種質(zhì)資源與良種選育、種植區(qū)劃與分區(qū)布局[21] 等進(jìn)行深入研究及科學(xué)評(píng)價(jià)。只有在中藥材的種植、采收、加工、儲(chǔ)存等環(huán)節(jié)嚴(yán)把質(zhì)量關(guān),才能保證中藥材的質(zhì)量穩(wěn)定、可靠。
3.5 細(xì)化缺陷風(fēng)險(xiǎn)評(píng)級(jí)
根據(jù)《中藥材GAP 檢查指南》,檢查結(jié)果的判定參照《藥品生產(chǎn)現(xiàn)場(chǎng)檢查風(fēng)險(xiǎn)評(píng)定指導(dǎo)原則》執(zhí)行,主要是工業(yè)生產(chǎn)環(huán)節(jié)的風(fēng)險(xiǎn)等級(jí)評(píng)定,尚不能完全契合中藥材生產(chǎn)實(shí)際,尤其是在種子種苗、種植技術(shù)與管理等方面,風(fēng)險(xiǎn)評(píng)級(jí)還需要結(jié)合GAP 延伸檢查特點(diǎn)進(jìn)一步改進(jìn)和細(xì)化。
3.6 提升檢查能力
《國(guó)家藥監(jiān)局 農(nóng)業(yè)農(nóng)村部 國(guó)家林草局 國(guó)家中醫(yī)藥局關(guān)于發(fā)布〈中藥材生產(chǎn)質(zhì)量管理規(guī)范〉的公告》中第一次明確“省級(jí)藥品監(jiān)督管理部門……必要時(shí)對(duì)相應(yīng)的中藥材生產(chǎn)企業(yè)開展延伸檢查”。根據(jù)《〈中藥材生產(chǎn)質(zhì)量管理規(guī)范〉監(jiān)督實(shí)施示范建設(shè)方案》,廣東省承擔(dān)中藥材GAP 示范建設(shè)任務(wù),需按要求建立和培訓(xùn)一支符合中藥材GAP 檢查特點(diǎn)的檢查員隊(duì)伍,以確保高效完成示范建設(shè)工作以及之后的各項(xiàng)檢查任務(wù)。目前,廣東省已組建由中藥材GAP專家、藥品監(jiān)管部門人員、藥品檢驗(yàn)機(jī)構(gòu)人員等組成的檢查隊(duì)伍,基本覆蓋檢查需要的各個(gè)專業(yè)板塊。但因中藥材GAP 延伸檢查仍處在探索階段,檢查組的專業(yè)技術(shù)能力與現(xiàn)場(chǎng)檢查能力仍有待進(jìn)一步提升。
4. 總結(jié)
廣東省以承擔(dān)國(guó)家藥監(jiān)局監(jiān)督實(shí)施示范建設(shè)為契機(jī),聚焦本省實(shí)際,通過統(tǒng)籌監(jiān)管和服務(wù),優(yōu)化完善延伸檢查模式,以中藥生產(chǎn)企業(yè)將質(zhì)量管理體系延伸到中藥材生產(chǎn)基地為著力點(diǎn),強(qiáng)化嶺南特色中藥材GAP 示范建設(shè)與創(chuàng)新發(fā)展為突破點(diǎn), 推動(dòng)以產(chǎn)地政府為主導(dǎo)的廣東省中藥材GAP 監(jiān)督實(shí)施重點(diǎn)區(qū)域建設(shè),引導(dǎo)中藥生產(chǎn)企業(yè)使用符合GAP的中藥材,促進(jìn)中藥全產(chǎn)業(yè)鏈質(zhì)量管理與追溯體系構(gòu)建。2023 年以來共完成8 家中藥生產(chǎn)企業(yè)申報(bào)的中藥材GAP 符合性延伸檢查,共涉及41 個(gè)藥品品種、21個(gè)中藥材品種,派出檢査員71 名(含國(guó)家藥監(jiān)局中藥材GAP 專家3 名、廣東省藥監(jiān)局中藥材GAP專家13 名)。
實(shí)施GAP 的根本目的在于提高中藥材的生產(chǎn)質(zhì)量,保證中藥飲片和中成藥的質(zhì)量,確保公眾用藥安全有效。實(shí)施GAP 的基本要求就是中藥材生產(chǎn)必須堅(jiān)持科學(xué)化、規(guī)范化、規(guī)模化,以保證中藥材質(zhì)量穩(wěn)定可控、資源合理利用和可持續(xù)。中藥材GAP實(shí)施的優(yōu)劣,取決于對(duì)相關(guān)文件貫徹執(zhí)行的程度,特別是生產(chǎn)基地建設(shè)和生產(chǎn)技術(shù)及質(zhì)量管理是否到位。實(shí)施主體應(yīng)針對(duì)薄弱環(huán)節(jié), 根據(jù)中藥材GAP 的要求,有的放矢地加強(qiáng)軟件管理,強(qiáng)化人員培訓(xùn),改進(jìn)硬件設(shè)施,強(qiáng)化質(zhì)量管理體系建設(shè)。通過以上措施,推進(jìn)中藥材規(guī)范化生產(chǎn),加強(qiáng)中藥材質(zhì)量控制,促進(jìn)中藥產(chǎn)業(yè)高質(zhì)量發(fā)展。
引用本文
徐貽權(quán),莫結(jié)麗,嚴(yán)振,曾祥衛(wèi),歐陽蒲月*,賴盼,鄭聰敏.中藥材生產(chǎn)質(zhì)量管理規(guī)范延伸檢查的實(shí)踐與思考[J].中國(guó)食品藥品監(jiān)管.2025.2(253):118-127.

來源:中國(guó)食品藥品監(jiān)管雜志


