單克隆抗體制品(以下簡(jiǎn)稱“單抗”)病毒污染風(fēng)險(xiǎn)控制是一項(xiàng)系統(tǒng)工程,本文梳理了單抗原液生產(chǎn)工藝流程,全生命周期病毒污染風(fēng)險(xiǎn)控制總體策略知識(shí),重點(diǎn)在滿足藥品生產(chǎn)質(zhì)量管理規(guī)范(2010年修訂)和相關(guān)廠房設(shè)計(jì)規(guī)范的前提下,針對(duì)單抗原液生產(chǎn)的工藝特性,從原液生產(chǎn)工藝流程和除病毒工藝布置方面對(duì)單抗原液生產(chǎn)車間的工藝設(shè)計(jì)進(jìn)行分析。
1、單抗原液生產(chǎn)工藝流程分析
抗體藥物的原液生產(chǎn)大體可分為上游工藝(又稱細(xì)胞培養(yǎng))、下游工藝(又稱純化)2個(gè)環(huán)節(jié),每個(gè)環(huán)節(jié)都擁有其核心技術(shù),這些核心技術(shù)環(huán)環(huán)相扣,形成了抗體藥物生產(chǎn)企業(yè)的核心競(jìng)爭(zhēng)力。一個(gè)典型的抗體藥物原液生產(chǎn)工藝流程如下圖:
典型的抗體藥物原液生產(chǎn)工藝流程
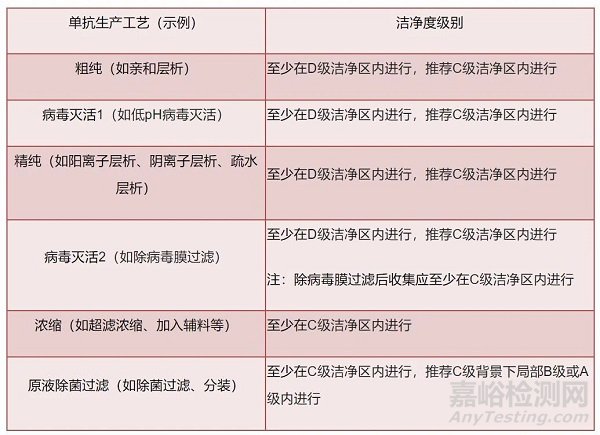
單抗制品下游工藝(又稱純化)的商業(yè)化生產(chǎn)流程一般采用以下步驟:粗純(如親和層析)→病毒滅活1(如低pH病毒滅活)→精純(如陽離子層析、陰離子層析、疏水層析)→病毒滅活2(如除病毒膜過濾)→濃縮(如超濾)→除菌過濾→抗體藥物原液。
2、單抗全生命周期病毒污染風(fēng)險(xiǎn)控制總體策略
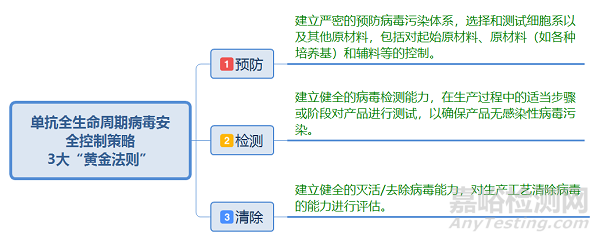
病毒污染可能會(huì)對(duì)單抗質(zhì)量和產(chǎn)品供應(yīng)的潛在影響,可能產(chǎn)生重大后果,生物藥企需要謹(jǐn)慎管理病毒污染風(fēng)險(xiǎn),降低病毒污染的風(fēng)險(xiǎn),并制定相應(yīng)風(fēng)險(xiǎn)控制措施,將病毒污染風(fēng)險(xiǎn)控制在最低限度,單抗病毒安全保障需建立整體策略,根據(jù)2020《中國藥典》三部生物制品病毒安全性控制中提到,“應(yīng)明確影響病毒清除效果的關(guān)鍵工藝參數(shù)及控制范圍,并在此基礎(chǔ)上建立充分的產(chǎn)品制備工藝過程的控制策略。”,根據(jù)ICHQ5A《來源于人或動(dòng)物細(xì)胞系生物技術(shù)產(chǎn)品的病毒安全性評(píng)價(jià)》提煉出從以下三方面入手建立單抗制品全過程病毒安全綜合保障策略,即單抗制品全生命周期病毒安全控制策略的3大“黃金法則”:
3、GMP對(duì)生物制品的廠房要求
1)法規(guī)1—藥品生產(chǎn)質(zhì)量管理規(guī)范(2010年修訂,2011年3月1日施行)
第四十六條 為降低污染和交叉污染的風(fēng)險(xiǎn),廠房、生產(chǎn)設(shè)施和設(shè)備應(yīng)當(dāng)根據(jù)所生產(chǎn)藥品的特性、工藝流程及相應(yīng)潔凈度級(jí)別要求合理設(shè)計(jì)、布局和使用,并符合下列要求:
(一)應(yīng)當(dāng)綜合考慮藥品的特性、工藝和預(yù)定用途等因素,確定廠房、生產(chǎn)設(shè)施和設(shè)備多產(chǎn)品共用的可行性,并有相應(yīng)評(píng)估報(bào)告。
(二)生產(chǎn)特殊性質(zhì)的藥品,如生物制品(如卡介苗或其他用活性微生物制備而成的藥品),必須采用專用和獨(dú)立的廠房、生產(chǎn)設(shè)施和設(shè)備。
(六)藥品生產(chǎn)廠房不得用于生產(chǎn)對(duì)藥品質(zhì)量有不利影響的非藥用產(chǎn)品。
第四十七條 生產(chǎn)區(qū)和貯存區(qū)應(yīng)當(dāng)有足夠的空間,確保有序地存放設(shè)備、物料、中間產(chǎn)品、待包裝產(chǎn)品和成品,避免不同產(chǎn)品或物料的混淆、交叉污染,避免生產(chǎn)或質(zhì)量控制操作發(fā)生遺漏或差錯(cuò)。
第四十八條 應(yīng)當(dāng)根據(jù)藥品品種、生產(chǎn)操作要求及外部環(huán)境狀況等配置空調(diào)凈化系統(tǒng),使生產(chǎn)區(qū)有效通風(fēng),并有溫度、濕度控制和空氣凈化過濾,保證藥品的生產(chǎn)環(huán)境符合要求。潔凈區(qū)與非潔凈區(qū)之間、不同級(jí)別潔凈區(qū)之間的壓差應(yīng)當(dāng)不低于10帕斯卡。必要時(shí),相同潔凈度級(jí)別的不同功能區(qū)域(操作間)之間也應(yīng)當(dāng)保持適當(dāng)?shù)膲翰钐荻取?/span>
第四十九條 潔凈區(qū)的內(nèi)表面(墻壁、地面、天棚)應(yīng)當(dāng)平整光滑、無裂縫、接口嚴(yán)密、無顆粒物脫落,避免積塵,便于有效清潔,必要時(shí)應(yīng)當(dāng)進(jìn)行消毒。
第五十六條 生產(chǎn)區(qū)內(nèi)可設(shè)中間控制區(qū)域,但中間控制操作不得給藥品帶來質(zhì)量風(fēng)險(xiǎn)。
2)法規(guī)2—GMP附錄《生物制品》(2020年修訂,2020年7月1日施行)
第十三條 生物制品生產(chǎn)環(huán)境的空氣潔凈度級(jí)別應(yīng)當(dāng)與產(chǎn)品和生產(chǎn)操作相適應(yīng),廠房與設(shè)施不應(yīng)對(duì)原料、中間體和成品造成污染。
第十四條 生產(chǎn)過程中涉及高危因子的操作,其空氣凈化系統(tǒng)等設(shè)施還應(yīng)當(dāng)符合特殊要求。
第十五條 生物制品的生產(chǎn)操作應(yīng)當(dāng)在符合下表中規(guī)定的相應(yīng)級(jí)別的潔凈區(qū)內(nèi)進(jìn)行,未列出的操作可參照下表在適當(dāng)級(jí)別的潔凈區(qū)內(nèi)進(jìn)行:
|
潔凈度級(jí)別 |
生物制品生產(chǎn)操作示例 |
|
B級(jí)背景下的局部A級(jí) |
附錄一無菌藥品中非最終滅菌產(chǎn)品規(guī)定的各工序灌裝前不經(jīng)除菌過濾的制品其配制、合并等 |
|
C級(jí) |
1. 體外免疫診斷試劑的陽性血清的分裝、抗原與抗體的分裝 |
|
D級(jí) |
1. 原料血漿的合并、組分分離、分裝前的巴氏消毒 |
|
2. 口服制劑其發(fā)酵培養(yǎng)密閉系統(tǒng)環(huán)境(暴露部分需無菌操作) |
|
3. 酶聯(lián)免疫吸附試劑等體外免疫試劑的配液、分裝、干燥、內(nèi)包裝 |
第十七條 滅活疫苗(包括基因重組疫苗)、類毒素和細(xì)菌提取物等產(chǎn)品滅活后,可交替使用同一灌裝間和灌裝、凍干設(shè)施。每次分裝后,應(yīng)當(dāng)采取充分的去污染措施,必要時(shí)應(yīng)當(dāng)進(jìn)行滅菌和清洗。
第二十八條 生產(chǎn)過程中被病原體污染的物品和設(shè)備應(yīng)當(dāng)與未使用的滅菌物品和設(shè)備分開,并有明顯標(biāo)志。
3)法規(guī)3—GMP附錄《血液制品》(2020年修訂,2020年10月1日施行)
第十一條 血液制品的生產(chǎn)廠房應(yīng)當(dāng)為獨(dú)立建筑物,不得與其他藥品共用,并使用專用的生產(chǎn)設(shè)施和設(shè)備。
第十四條 原料血漿破袋、合并、分離、提取、分裝前的巴氏滅活等工序至少在D級(jí)潔凈區(qū)內(nèi)進(jìn)行。
第十五條 血漿融漿區(qū)域、組分分離區(qū)域以及病毒滅活后生產(chǎn)區(qū)域應(yīng)當(dāng)彼此分開,生產(chǎn)設(shè)備應(yīng)當(dāng)專用,各區(qū)域應(yīng)當(dāng)有獨(dú)立的空氣凈化系統(tǒng)。
第十六條 血液制品生產(chǎn)中,應(yīng)當(dāng)采取措施防止病毒去除和/或滅活前、后制品的交叉污染。病毒去除和/或滅活后的制品應(yīng)當(dāng)使用隔離的專用生產(chǎn)區(qū)域與設(shè)備,并使用獨(dú)立的空氣凈化系統(tǒng)。
4、單抗原液生產(chǎn)工藝布局分析
單抗生產(chǎn)過程中嚴(yán)格執(zhí)行GMP,以上法規(guī)對(duì)單抗原液車間生產(chǎn)工藝布局和潔凈區(qū)環(huán)境級(jí)別有具體明確的要求,根據(jù)目前國內(nèi)實(shí)踐經(jīng)驗(yàn),單抗下游生產(chǎn)工藝的潔凈區(qū)域劃分原則建議見下表:
另外建議根據(jù)所生產(chǎn)產(chǎn)品特性、工藝、預(yù)定用途和設(shè)備等因素,使用風(fēng)險(xiǎn)評(píng)估的手段,采取相應(yīng)的預(yù)防差錯(cuò)、交叉污染、安全防護(hù)措施,包括但不限于:
(1)采取必要的措施,防止病毒滅活/去除后的產(chǎn)品被污染;
(2)已經(jīng)過病毒去除/滅活處理的產(chǎn)品與尚未處理的產(chǎn)品應(yīng)有明顯區(qū)分和標(biāo)識(shí),并應(yīng)采用適當(dāng)?shù)姆椒ǚ乐刮锲坊煜?/span>
(3)若使用敞門容器或設(shè)備操作時(shí),應(yīng)有避免污染的措施;
(4)盡量避免同一設(shè)備用于不同階段的純化操作;
(5)如果使用同一設(shè)備,應(yīng)當(dāng)采取適當(dāng)?shù)那鍧嵑拖敬胧?duì)清潔和消毒的效果進(jìn)行驗(yàn)證,防止病毒通過設(shè)備或環(huán)境由前次純化操作帶入后續(xù)純化操作。