您當前的位置:檢測資訊 > 科研開發
嘉峪檢測網 2022-09-16 05:22
目前為止皮膚創面修復仍然是醫護人員面臨的一個問題。皮膚噴霧劑是一種仍在臨床評估中的創新技術,與傳統的傷口愈合治療方法相比,皮膚噴霧劑具有顯著的優勢,如可進行更大區域傷口治療的可能性,以及均勻噴涂藥物。在這篇文章中,我們回顧了這項技術的最新進展,詳細描述了其研究性和目前商用的脫細胞和細胞皮膚噴霧產品,用于各種疾病和應用不同的實驗材料。
01、研究內容簡介
皮膚是人體最大的器官,也是抵御病原體和熱、機械和化學危害的最重要的防御機制之一,因為它是最外層的保護鞘,與外部環境直接接觸。皮膚由三個主要層組成,淺表皮和較深的真皮,其次是皮下結締組織層。表皮由幾層角化上皮組成,是動態可持續自我更新的。角質形成細胞是表皮的主要細胞類型,它們能夠分化和合成多種結構蛋白和脂質,在皮膚功能中發揮重要作用。這些脂質對表皮再生至關重要。表皮內的其他細胞是提供色素沉著的黑素細胞和有助于免疫監視的朗格漢斯細胞。角質細胞(去核死亡細胞)被發現嵌在表皮最上層的脂質基質中,這起著抑制成分的吸收和失水的作用。真皮是一層較厚的結締組織,主要由細胞(如成纖維細胞、內皮細胞、平滑肌細胞和肥大細胞)、細胞外基質(ECM)和膠原蛋白和彈性蛋白纖維等結構成分組成,提供機械強度和彈性,以及皮膚營養的血管叢。表皮和真皮之間的基底膜,一個高度專業化的ECM結構,由不同的糖蛋白和蛋白多糖,提供了一個穩定但動態界面和這兩層之間的擴散屏障,和皮膚附件如毛囊、汗腺和神經都嵌入。這些皮膚附屬物維持身體的水合作用,并構成一個保護層,幫助保護身體免受惡劣環境,以及其他功能。連接真皮和底層結構的是皮下組織,即結締組織,包括成纖維細胞和脂肪組織,以儲存和保護脂肪,作為皮膚的減震器和身體的隔熱器。人類皮膚的厚度約為1.5-2.5mm,但它根據其解剖定位和支持身體重量的功能而有所不同。
皮膚傷口或損傷可能由燒傷和其他物理和化學創傷、遺傳不規則、皮膚病(如糖尿病足潰瘍、肛瘺或大皰性表皮松解)或手術期間切除皮膚。根據損傷的深度,皮膚傷口可分為表皮傷口、淺表部分厚度傷口、深部部分厚度傷口和全層傷口。為了獲得最佳治療,傷口必須早期診斷,盡管有些病例可能難以通過早期評估進行準確分類。由于皮膚的自愈合功能,表皮和淺表部分厚度的傷口通常可以再生,而不需要治療干預。
這篇綜述主要討論和總結皮膚再生的主要方法和技術,特別關注皮膚噴霧技術的最新進展,包括調查和目前可用的商業化脫細胞和細胞產品,和他們的監管途徑的解釋。最后,我們對使用噴霧劑治療各種皮膚狀況的臨床試驗進行了詳盡的搜索,并提出了皮膚噴霧劑生物技術的未來更可行的臨床應用趨勢。
2.1.傷口愈合的常規治療方法:皮膚移植
深層傷口的傳統治療包括分裂和全層自體皮膚移植,包括從患者身體未受傷的部位切割一塊皮膚,并將其移植到受傷部位。這種治療方法是有效的,是治療二度到三度燒傷最常見的方法,但它會給患者帶來更多的疼痛,并使需要治愈的區域增加一倍。此外,自體移植的使用受到可用的未受傷的供體皮膚的大小,這導致使用不太理想的選擇如臨時覆蓋其他類型的皮膚移植,如同種異體移植和異種移植,攜帶免疫反應和疾病傳播的風險。一個減少的供體皮膚部位可以通過網狀技術擴大到一個更大的尺寸,以獲得網狀的分裂厚度的自體移植物。然而,它們通常伴有供體部位和網狀間隙的瘢痕,當其擴張率大于1:4時,由于難以處理,因此受到限制。復發性的解決方案用于燒傷護理是自體細胞放大數量,獲得培養自體上皮移植(CEAs),首次由萊茵瓦爾德和綠色在1975年,但它可能需要幾周的組織培養成熟,成為可用于移植,而嚴重燒傷患者增加生存的機會當傷口切除和移植早期。盡管有很多報告成功的臨床應用和更好的美容結果相比寬網格自體移植相比,不斷培養角質形成細胞片的過程是昂貴的,耗時和勞動密集型,和床單顯示脆弱,低效率,可變的移植和可憐的附件。此外,CEAs大多由一種細胞類型(角質形成細胞祖細胞)生長而來,因此缺乏完整皮膚結構所需的完整細胞元素(如黑素細胞、毛囊和汗腺)。如圖1,展現了用于燒傷和傷口愈合應用的不同移植技術。

Fig. 1. Conventional grafting approaches for wound healing. Autologous skin grafts can be obtained from a biopsy of the patient’s own undamaged skin, and this autograft can be either applied directly over the wound, or expanded by meshing techniques or cell culturing prior to application. On the other hand, skin grafts obtained from another individual as a donor (allograft) or from an animal (xenograft), respectively, can be applied temporarily to cover the patient’s wound.
2.2.目前的治療策略
由于生物合成皮膚替代品的發展,一些材料已被作為皮膚替代產品應用于臨床或制藥工程等,包括水凝膠、薄膜、細胞懸浮液、細胞片,或3D皮膚支架,由不同的TE方法如3D生物打印、靜電紡絲,包括細胞噴霧設備等(第三節中更廣泛的討論)。這些產品可以分化為脫細胞和細胞皮膚替代品,都需要使用生物相容性和生物降解材料,也能夠保持潮濕的環境,減少促炎反應,有滿意的機械性能和多孔足以促進細胞增殖和生物分子的運輸,營養和代謝廢物。
2.2.1.用于皮膚替代品的生物材料
各種生物材料,包括天然的和合成的,已被廣泛地用作皮膚的替代品。它們形成三維聚合物網絡,旨在模擬天然ECM的結構和功能,也可作為細胞定位、粘附和分化的平臺,從而刺激皮膚再生。為了制造重現皮膚生理條件的皮膚替代品,已經使用了幾種天然材料,如膠原蛋白、纖維蛋白原、明膠、絲、透明質酸(HA)或海藻酸鹽。
其中,膠原蛋白具有良好的生物相容性,是真皮ECM的主要結構蛋白,具有高度的仿生性。具有良好的生物降解性,低免疫原性,多孔結構具有良好的滲透性。市上有許多板材、凝膠、膠格或海綿敷料;但這些敷料往往生物穩定性差,機械強度低,而且純膠原蛋白價格昂貴,且容易引起傷口收縮和瘢痕。因此,可以通過膠原蛋白的物理或化學分子間交聯,或通過混合膠原蛋白與其他材料,如糖胺聚糖(GAGs)、瓊脂糖、或殼聚糖等,來改變其力學性能。
傷口的一個重要生物聚合物愈合是纖維蛋白原,轉化為凝血酶凝血級聯,它已被廣泛用于制備纖維蛋白膠或密封膠劑,覆蓋傷口和提供一個直接臨時矩陣,將入侵修復細胞在傷口床上。纖維蛋白原具有生物相容性和可生物降解性,可以從患者自身的血液中分離出來,因此限制了免疫原性。此外,纖維蛋白水凝膠已被報道可促進傷口愈合、表皮再生和血管生長;并減少疤痕的形成。纖維蛋白具有較高的彈性變形能力和較大的拉伸能力,但它也是最軟的聚合物纖維之一,力學性能較低。然而,纖維蛋白凝膠的力學性能可以通過調整一些因素,如pH或纖維蛋白原和凝血酶的濃度來優化;或通過將纖維蛋白與不同的材料結合,,如HA、明膠或聚乙二醇(PEG)。
另一種生物材料殼聚糖由去乙酰化幾丁質衍生,在傷口愈合和TE方面具有許多優勢,包括生物相容性、生物降解性、止血活性、抗菌性能和刺激再上皮化等。此外,它還可以很容易地制成薄膜、凝膠或海綿。然而,它的力學性能需要改進,因為一旦它被干燥,它就會遭受嚴重的收縮和變形,這限制了純殼聚糖制造皮膚替代品的應用。因此,為了克服這些限制,殼聚糖通常是交聯,通過結構修飾,或與其他天然和合成聚合物結合,如明膠、瓊脂糖或膠原等。例如,Soriano-Ruiz等人(2019)開發了基于三種gag(HA、硫酸軟骨素和硫酸皮膚素)和膠原蛋白的四級混合物的殼聚糖水凝膠,用于傷口愈合。
明膠是一種膠原蛋白衍生的蛋白質,已經以海綿或薄膜的形式進行了研究。其優點包括促進上皮化和肉芽組織形成的能力,其高生物降解性和生物相容性,與膠原蛋白相比成本較低,但其低機械強度,使其只有在與其他聚合物結合時才有效。例如,明膠已與殼聚糖聯合使用,廣泛用于制造皮膚水凝膠,但這種混合水凝膠的機械強度仍然較差,可以通過添加其他材料,如HA或聚己內酯(PCL)來改善。
從家蠶中獲得的絲狀纖維素,具有良好的傷口愈合性能。它具有良好的生物相容性和生物降解性、止血性能、低免疫原性和非炎癥特性,是無毒、非致癌的。此外,已知它可以加速傷口愈合,促進細胞增殖、膠原合成和再上皮化,并為細胞附著提供支持。其良好的力學性能和易于制造,使絲纖維成為一種有趣的皮膚TE生物材料。然而,絲纖維素沒有抗菌特性,這往往會導致傷口感染,但這一問題可以通過添加其他抗菌材料來解決。對于皮膚傷口愈合,絲素通常以膜、水凝膠、海綿或納米纖維支架的形式使用,或單獨或結合其他材料,如藻酸鹽或殼聚糖等。Roh等人(2006)比較了絲纖維海綿、藻酸海綿和絲纖維/藻酸混合海綿在大鼠全層傷口模型中的愈合效果,發現三種海綿較對照組提高了傷口愈合率,但混合海綿的傷口愈合率較高。
海藻酸鹽是一種天然多糖聚合物,因其生物相容性、生物降解性、可承受性、無毒、非免疫原性和螯合能力等突出特性,在近十年來受到廣泛關注。各種水凝膠、電紡墊和海綿形式的傷口敷料都是基于海藻酸鹽,因為它對傷口愈合有許多優點,包括其止血和溫和的防腐性能、符合性、促進肉芽組織形成和快速上皮化。海藻酸鹽是高度親水的,加上它保持水的能力,它允許維持一個潮濕的傷口環境,可以避免傷口床干燥。此外,其結構缺乏細胞粘附的信號序列,這使其成為傷口管理的重要材料,因為避免了海藻酸鹽基敷料剝離時的繼發性損傷。然而,海藻酸鹽的結構完整性和力學性能較差,但可以通過與其他材料(如殼聚糖、纖維蛋白原或明膠)結合來改善;通過固定特定的配體;或通過交聯。離子交聯,使用二價陽離子如ca2+,交聯是藻酸鹽最常見的凝膠的方法,但這些二價陽離子可以釋放并與周圍介質中的其他一價陽離子交換,導致藻酸鹽凝膠的溶解。盡管如此,海藻酸鹽水凝膠也可以通過共價交聯、熱凝膠、細胞交聯、自由基聚合和“點擊”反應來促凝膠。
GAGs(包括HA、硫酸軟骨素、硫酸肝素、硫酸皮膚素和硫酸角蛋白)在傷口愈合的所有階段都起著至關重要的作用,這使它們成為表皮再生配方的必要成分。HA具有良好的生物相容性和生物降解性,具有較高的保水能力,以及抗炎、粘附和粘彈性性能。并能抑制組織粘附和瘢痕組織形成。目前市場上有一些HA衍生產品,但可溶性HA由于力學性能差,透明質酸酶降解速度快,臨床應用受到限制。
另一方面,合成聚合物是更便宜和更可靠的材料來源,因為它們具有大量的均勻性,可以定制提供廣泛的物理性質。其中,聚氨酯(PU)具有生物相容性和良好的機械性能,對細菌和水和對氣體保持濕潤環境,是傷口愈合的理想材料。PU產品具有成本效益,但它們對傷口床的粘附性有限。尼龍、聚(乙醇酸)和聚(乳酸)已以網狀形式用于一些商業皮膚替代品。然而,其他聚合物,包括PCL或聚(l-乳酸酯),已經顯示出有限的臨床成功,因為它們的細胞附著和增殖率低,由于有限的生物信號。
總的來說,天然聚合物具有良好的生物相容性,促進細胞粘附和增殖,但它們的一些局限性包括機械強度低,收縮或收縮,處理困難,在某些情況下,成本高;而合成聚合物具有良好的力學性能,但它們缺乏天然聚合物中存在的生物信號。因此,為了獲得更好的機械強度和保持良好的生物相容性,天然聚合物和合成聚合物通常以不同的方式組合,例如通過混合或交聯聚合物溶液;用天然聚合物涂覆合成網;或通過在合成針織網格的開口處形成天然聚合物的微海綿來構建混合網格。
如前所述,皮膚替代品可以不同的形式用于臨床使用,如水凝膠、薄膜、細胞懸液、細胞薄片或3D皮膚支架。這些產品是使用前面描述的不同的生物材料制造的,在細胞替代品的情況下,也與異體細胞或自體細胞結合。這些細胞可以在獲得后直接使用,也可以在用于制造皮膚替代品之前進行培養以放大它們的數量。三維支架是構建人工皮膚替代品的支柱,是細胞粘附和增殖的平臺。針對皮膚TE的不同支架設計(如納米纖維基質、微孔支架、聚合物網絡、晶格或網格等)。可以通過傳統的方法制備,如冷凍干燥或顆粒浸出,或通過新的TE技術,如三維生物打印、靜電紡絲或噴涂(如圖2)。
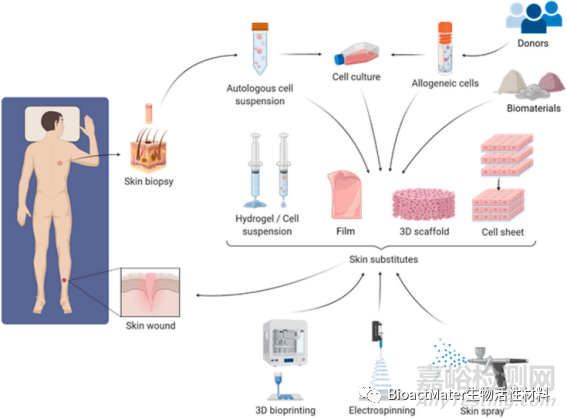
Fig. 2. Current therapeutic approaches for wound healing. Skin wounds can be covered and treated with different skin substitutes such as cell suspensions, hydrogels, cell sheets, films, or 3D scaffolds, which can be fabricated by techniques like 3D bioprinting, electrospinning or skin sprays. Skin sprays allow the delivery of hydrogels and/or cells to the wound. Cells used for cellular skin substitutes can either be autologous (obtained from a biopsy of the patient’s skin) or allogeneic (obtained from skin samples of donors); and they can be used directly, or they can be cultured to amplify their number prior their application.
在過去的幾十年里,使用水凝膠局部噴霧劑或細胞懸液噴霧劑治療急性和慢性傷口一直備受臨床關注,這歸功于它們的優勢,例如可以治療大傷口或噴灑區域具有不利的地形,減少的應用時間,以及噴涂懸浮液的均勻分布。
3.1.無細胞皮膚噴霧劑,脫細胞皮膚噴霧劑通常由水凝膠組成,當它們噴在傷口上時形成薄層,作為敷料,保護傷口免受感染和液體流失。此外,一些水凝膠可能有助于增強傷口愈合過程,其中一些具有抗菌特性或可以作為藥物傳遞系統。纖維蛋白是最廣泛用于皮膚噴霧劑的水凝膠,經常直接噴灑在較輕的傷口上,作為止血敷料或移植物,以促進粘附和吸收率
3.1.1.非商業性脫細胞皮膚噴霧劑
到目前為止,已經有幾項研究在傷口上應用了不同的實驗水凝膠,保護它們免受感染,避免水分流失。表1總結了它們。這些具體的研究只在體外或動物模型中進行,通常使用一個簡單的噴淋泵作為噴涂裝置,并且大部分的噴涂參數沒有明確規定。

3.1.2.商業脫細胞皮膚噴霧劑產品,在商業無細胞噴霧劑中,他們中的許多人使用纖維蛋白作為他們的產品。其中最受歡迎的是Baxter的TISSEL®(在某些國家/地區以TISSUCOL®商標授權),這是一種纖維蛋白膠水,自90年代初以來一直被廣泛用作開放手術和腹腔鏡檢查中的止血和密封的輔助手段,來自人血漿。它提供滴灌和噴霧器,連接到雙注射器(一個用于纖維蛋白原溶液,另一個用于凝血酶溶液),允許外科醫生根據患者的個體需求來選擇正確的工具。作為一種噴霧劑,許多研究已經在體外和體內使用了TISSEEL®纖維蛋白密封膠,單獨或與細胞一起使用。有時使用TISSOMAT®噴霧,這是巴克斯特公司的加壓噴霧模塊(空氣壓縮機),其噴霧套件有一個雙注射器,支持其他材料的共同應用,如細胞懸浮液。使用組織 TISSEEL®(總結見表2)的研究報道,當纖維蛋白加入細胞治療(如自體角質形成細胞和成纖維細胞,或自體間充質干細胞)時,與單獨使用細胞治療的傷口相比,傷口愈合加速,傷口收縮更少。TISSEEL®纖維蛋白密封膠是一種優秀的液體細胞傳遞載體,在加入凝血酶后快速聚合,形成嵌在纖維蛋白網中的細胞粘附細胞網絡,仍保持其生長和分化的能力。
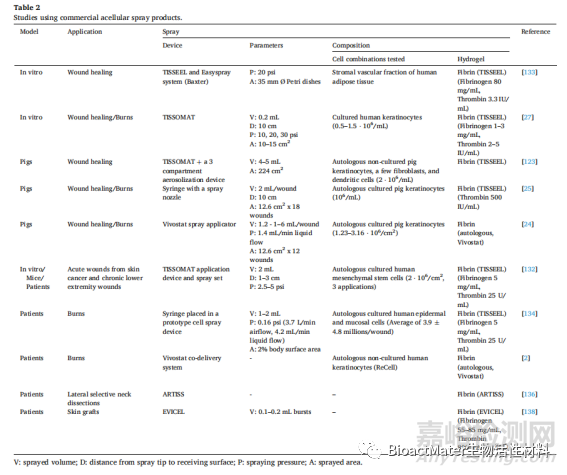
3.2.細胞噴霧劑,多種細胞類型已被用于細胞噴霧劑的體外傷口愈合研究,但自體表皮細胞主要用于體內研究和臨床試驗。細胞噴霧自體移植是一種仍在臨床評估中的創新技術,包括從患者未受損皮膚的小活檢中取出自體皮膚細胞,或將細胞直接噴灑在傷口上,或在噴灑前培養細胞以擴大其數量。與傳統的自體薄片移植相比,細胞噴霧自體移植是一種簡單而有效的方法,它避免了水泡的形成,需要更小的供體部位,從而減少愈合時間,減少并發癥。
3.2.1.非商業性細胞性皮膚噴霧劑,通過噴霧或氣溶膠輸送細胞已經在許多進行了評估,表3收集了使用實驗性細胞噴霧懸浮液進行燒傷和傷口愈合應用的主要研究結果,通常使用帶有噴嘴或噴槍的注射器作為輸送裝置。表3所示的體外研究證明了噴霧劑作為成纖維細胞和角質形成細胞傳遞系統的可行性。在這些情況下,盡管細胞活性會隨著噴灑壓力的增加而降低,但在噴灑后依舊保持良好的增殖能力。

3.2.2.商業細胞性皮膚噴霧劑產品,1993年,澳大利亞外科醫生菲奧娜木材博士開發了一種氣溶膠系統噴霧一層病人的皮膚干細胞在受傷區域,稱為“噴霧皮膚”,包括一個小活檢從病人的未受損的皮膚,懸浮皮膚細胞的解決方案,然后噴灑說燒傷傷口的解決方案。這使得覆蓋的面積是活檢面積的80倍。基于此,Avita醫療公司推出了一種試劑盒,稱為ReCell,它含有一種酶溶液,可以從活檢中分離和分離皮膚細胞。最后,細胞懸浮在10 mL注射器中的乳酸鈉溶液中,并且可以滴入傷口(如果注射器中的體積小于2 mL)或通過附著到注射器上的噴嘴噴灑(如果注射器中的體積大于或等于2 mL)。細胞懸液可以直接噴灑到部分厚度的傷口上,或在全層傷口的網狀自體移植物上。細胞已廣泛用于燒傷,也用于治療其他皮膚病和疾病,如白癜風、白癜風、白斑病、治療疤痕等。表4總結了使用ReCell的一些研究。他們報告說,在噴灑過程中細胞破裂最小,由于非培養細胞收獲后立即應用的時間減少,傷口愈合速度加快,供體細胞收獲面積小,而ReCell試劑盒的額外成本和更長的準備時間。

本研究發現共有104項關于皮膚噴霧劑的臨床試驗,其中9項為觀察性研究,其余為介入性研究。大多數介入性試驗處于2期試驗(23項試驗)或3期試驗(22項試驗),隨后是20項試驗處于4期試驗。與此同時,只有7個試驗處于第1階段,其他一些試驗處于第1和第2階段之間,或在第2和第3階段之間。此外,有16項試驗表現為“不適用”(N/A),因此沒有fda定義的階段(如圖3)

如圖4所示,銀屑病是與皮膚噴霧劑相關的臨床試驗最多的皮膚狀況,共有45項試驗發現。隨后是16項針對慢性傷口的試驗(其中7項是腿部靜脈潰瘍,7項是糖尿病足潰瘍,1項是壓瘡,1項是所有這些試驗:靜脈足、糖尿病足和壓瘡)。之后,有9項針對燒傷的試驗,9項針對皮炎和濕疹的臨床試驗,包括特應性皮炎、放射性皮炎,以及1項針對由嬰兒尿布引起的皮炎的試驗。包括傷口愈合的8個試驗是針對各種條件或外科手術程序進行的,這些試驗的主要目的是愈合傷口。有7項脫發試驗,將噴霧劑應用于患者的頭皮上。3項試驗針對尋常痤瘡,另外3項試驗針對白癜風和高血壓。最后,還有其他5項針對不同情況的試驗:酒渣鼻、紅斑、毛狀角化病和2項針對足癬的試驗。

Fig. 4. Number of clinical trials per condition. The graph shows the number of trials found for each skin condition or disease, with psoriasis being the most numerous, with 45 trials. It is followed by ulcers and chronic wounds (16 trials), burns (9 trials), dermatitis and eczema (9 trials), wound healing applications (8 trials), alopecia (7 trials), acne (3 trials), vitiligo (3 trials) and other conditions (5 trials).
如圖五展示臨床試驗中使用的皮膚噴霧劑類型:(a)根據治療類型不同的臨床試驗數量:84個非細胞噴霧劑臨床試驗和18個細胞噴霧劑試驗。在細胞組中,14個使用自體細胞,4個使用異體細胞;(b)使用每種細胞類型的臨床試驗數量:12個使用來自ReCell的自體表皮細胞,1個使用自體表皮基底細胞,1次使用自體角質形成細胞,4次使用異體人成纖維細胞和產品HP802-247的角質形成細胞。

不同皮膚狀況的治療可使用不同類型的噴霧,可分為脫細胞(補充表1)和細胞(補充表2),后者為明顯較大的組(圖5a)。這些臨床試驗的細胞噴霧劑包含表皮細胞,通常是角質形成細胞和成纖維細胞,其中大部分是從患者自身獲得的自體細胞;除了那些評估產品HP802-247的試驗,如前所述,該產品含有異體人成纖維細胞和角質形成細胞與纖維蛋白結合(圖5b)。相比之下,臨床研究中的大多數脫細胞皮膚噴霧劑是防腐溶液或抗炎藥物,如皮質類固醇,大多數時候沒有明確說明。然而,在這些試驗中,一些脫細胞噴霧劑包括高分子生物材料,如纖維蛋白、殼聚糖或葡聚糖,而其他一些則應用自體富血小板血漿(PRP)(圖6)。只有兩項觀察性研究沒有對患者進行任何治療,因為它們是對其他介入性三聯征的隨訪研究。

Fig. 6. Percentage of clinical trials depending on the material used for skin sprays. 4 out of the 8 trials using fibrin were in combination with cells (from the product HP802-247), and 1 out of the 3 trials using PRP was in combination with keratinocytes. (PRP: platelet rich plasma; rhPDGF-BB: B isoform dimer of recombinant human Platelet-Derived Growth Factor; rh-bFGF: recombinant human basic Fibroblast Growth Factor).
綜上所述,皮膚再生—特別是在深部傷口中,仍然是許多醫療保健專業人員面臨的一個挑戰。有許多多樣的策略,但沒有一個能提供完美的解決方案。與傳統的皮膚薄片移植或生物工程皮膚替代品相比,使用噴霧劑作為水凝膠和細胞的輸送系統,可以更輕松地治療大型受傷區域,并縮短時間。市場上有一些皮膚噴霧產品,但細胞噴霧移植目前仍在臨床評估中。到目前為止,只有少數設備被批準商業化和臨床使用。許多臨床前研究使用簡單的注射器和噴霧泵,它們不太關注壓力、距離、角度或體積等噴霧參數,因此,這些研究可能難以重復,因為這些參數會顯著影響結果。新的噴涂裝置應能夠調節這些參數,特別是壓力(例如,通過在設備上增加一個壓力計或壓力表)和體積。優化該設備和所用材料的這些參數是很有必要的新研究,因為使用不同的材料,如在隨后的幾層中噴灑不同的復合水凝膠,也可以用于模擬皮膚的不同層,可大大改善深部傷口的愈合。

來源:BioactMater生物活性材料


