您當前的位置:檢測資訊 > 科研開發
嘉峪檢測網 2022-08-15 21:39
口服給藥依然是最受歡迎的給藥途徑,它簡單便利,對患者的依從性好。但是,片劑和膠囊劑對部分患者具有難以吞咽的缺點,同時,也會影響部分會具有首過效應藥物的生物利用度。
為了獲得預期的治療效果,藥物應該以一定的速率和濃度輸送到體內,以達到最優的治療效果和最小的不良反應。口腔黏膜給藥是一種新型給藥方式,主要劑型有舌下片、舌下膜、口腔黏膜貼片、頰粘膜黏附膜和口頰黏膜溶液等,在制劑領域能幫助患者建立他們對治療方式的依從性,同時降低生產成本和提高藥物的生物利用度(尤其是在兒科和老年科)。
本文總結了近年來已發布的口腔黏膜給藥系統的優點、需要考慮的因素,以已上市藥物為例,幫助大家更好的了解口腔黏膜給藥系統及未來發展趨勢。
01、優勢
與傳統口服給藥相比,口服給藥薄膜具有一系列顯著的優點,包括藥物吸收快、生物利用度高、易于使用以及避免胃腸道和肝臟的首過效應,對有吞咽困難的兒童和老年人有更好的患者依從性,成功地使粘液粘附膜和口腔分散膜成為令人滿意的藥物遞送平臺。口腔薄膜無論是在設計天然和合成聚合物的配方方面、開發生產方法方面、實際應用方面都取得了重大進展。此外,活性藥物還可以被封裝成納米顆粒或包合物,分布在所制備的口腔薄膜中,不僅可以很好地增強靶向口腔黏膜的生物粘附性,還可以充分提高相應藥物的溶解性和滲透性,因此,可以充分促進藥物吸收,大大提高生物利用度。例如,阿塞那平的口服絕對生物利用度小于2%,開發為舌下片(Saphris®)后絕對生物利用度提高至46%~65%;鹽酸司來吉蘭1.25mg口崩片(Zelapar™)的AUC與10mg普通片的AUC相當。
02、舌下和口腔給藥途徑的挑戰
為了通過舌下或口腔給藥途徑的有效藥物遞送,在藥物配方設計和開發中應考慮很多因素。這些因素可能會影響藥物的生物利用度、穩定性、功效和安全性。
載藥量:裝載難溶性藥物仍處于起步階段。片劑和膠囊可以攜帶藥物進入體內溶解。而口腔給藥主要是依靠聚合物來增加藥物的溶解度。因此,還需要開發相應的處方來提高口腔膜劑的載藥量。晶型的研究是其中一種辦法,通過改變API的晶型使其在同樣含量下提高藥物溶解度及生物利用度。目前,研究者們正在探索更多相應的技術,以尋找增加難溶性藥物在口腔薄膜中溶解度的新方法。
停留時間:藥物的吸收高度依賴于藥物在舌下和頰區域的停留時間。患者和配方不同,停留時間可能會有很大差異。制劑在藥物吸收前需要崩解,這意味著在溶解方面它們會有所不同。對于有些藥物,吞咽還會影響藥物的有效性。
03、影響口腔給藥系統的其他因素
影響藥物在口腔黏膜吸收的生理屏障為口腔上皮細胞組成的滲透屏障、口腔內黏液和唾液組成的擴散屏障及酶屏障。滲透屏障主要存在于口腔上皮最外側200 um處,是藥物透口腔黏膜的主要生理屏障。
藥物的理化性質如分子量、解離度、脂溶性、水溶性等會影響藥物透口腔黏膜的難易程度及藥物在口腔黏膜的吸收途徑,從而影響口腔黏膜給藥系統的藥物動力學性質。經口腔黏膜吸收的藥物分子質量通常應不高于800 Da,分子質量越大越難透過口腔黏膜;藥物在口腔pH值(5.5?7.0)條件下未解離分數越高,藥物越容易透過口腔黏膜。
藥物的脂溶性和水溶性會影響藥物在口腔黏膜的吸收方式。藥物經口腔黏膜吸收的主要途徑為被動擴散,包括細胞旁路途徑(paracellular route)和跨細胞膜途徑(transcellular route)。細胞旁路途徑指通過細胞間隙進入血液循環,跨細胞膜途徑為直接穿透細胞進入血液循環(圖1)。親水性藥物多通過細胞旁路途徑被吸收,這類藥物易溶解在細胞間隙的液體中,如蛋白多肽類藥物;跨細胞膜途徑吸收的藥物要先穿過膜脂質進入細胞,再穿過細胞的親水內部,因而要求藥物具有較強脂溶性的同時還具有一定的水溶性。可選擇水溶性良好的鹽型來改善高親脂性藥物的水溶性,如高親脂性的芬太尼(僅微溶于水)用于透皮制劑,而檸檬酸芬太尼(水中溶解度為25 mg/mL-1)用于口腔黏膜給藥系統。
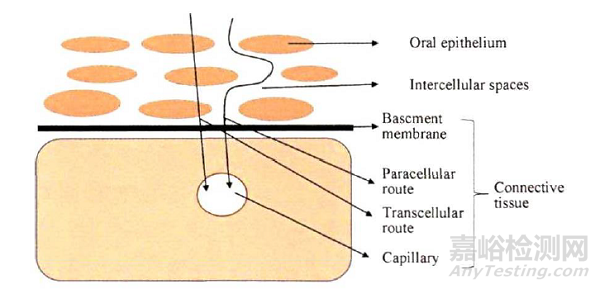
圖1.口腔膜劑藥物吸收途徑示意圖
除了藥物本身的理化性質之外,加入促滲劑、黏膜黏附劑、酶抑制劑及應用納米技術也可以幫助藥物克服在口腔黏膜的吸收屏障,提高藥物生物利用度。促滲劑可以改變上皮細胞間及細胞膜的脂質流動性,從而促進藥物在口腔黏膜的被動轉運。常用的促滲劑有表面活性劑、膽酸及其衍生物、氨基酸及其衍生物、陽離子聚合物等。黏膜黏附劑可以與口腔黏膜的黏蛋白相互作用,延長藥物在口腔黏膜的停留時間,增加藥物在黏膜的吸收。酶抑制劑如抑肽酶、膽酸鹽、纖維素衍生物、谷胱甘肽等可以減少藥物在口腔及黏膜的降解,提高藥物生物利用度。納米技術的應用(如納米粒載藥)可以提高藥物在口腔的穩定性及藥物的水溶性,增加藥物在口腔黏膜的吸收。
05、小結
舌下和口腔給藥途徑已被證明是傳統口服給藥途徑的有效替代品(尤其是在需要藥物快速起效時),對于全身給藥具有著明顯的臨床優勢。此外,它們也適用于在胃腸道中有高肝臟清除或降解的藥物,以及用于吞咽困難的患者。一方面,未來的研究需要關注新劑型處方的研究與開發,不僅要考慮生物相容性和生物利用度,還要考慮提高載藥量等一系列要點。另一方面,需要對生產工藝進行不斷優化,以實現高效的生產口腔薄膜,提高其商業化價值。而對于難溶性藥物的口膜開發,還需對制劑中的固態形式實現有效控制。
參考文獻:
[1] Hannan PA, Khan JA, Khan A, Safiullah S. Oral Dispersible System: A New Approach in Drug Delivery System. Indian J Pharm Sci. 2016;78(1):2-7. doi:10.4103/0250-474x.180244
[2] Hua S. Advances in Nanoparticulate Drug Delivery Approaches for Sublingual and Buccal Administration. Front Pharmacol. 2019;10:1328. Published 2019 Nov 5. doi:10.3389/fphar.2019.01328
[3] 王冰, 劉宏銳, 陳芳,等. 口腔黏膜給藥系統的藥物動力學研究進展[J]. 藥學學報, 2020, 55(2):9.

來源:新陽唯康Nycrist


