您當前的位置:檢測資訊 > 科研開發
嘉峪檢測網 2021-11-04 11:46
微球作為新型遞藥系統,在醫藥領域受到廣泛關注。根據微球微觀結構的不同,可將其分為實心微球、雙層微球、中空微球、多孔微球。不同的微觀結構賦予了微球不同的特性,使微球適用于不同的給藥形式和臨床用途。本文簡要介紹了不同結構微球的特點、制備方法和在醫藥領域的應用。
載藥微球是指藥物溶解或分散在高分子基質材料中形成的球狀微粒。微球制劑可以緩慢釋藥,從而減少給藥次數,降低血藥濃度的波動,發揮長期治療效果。將磁性物質引入微球中或對載體材料進行修飾[1] ,可使微球磁性靶向或主動靶向到病灶處,提高靶部位的有效血藥濃度,降低藥物的全身毒副作用。將微球導入腫瘤動脈中,可通過栓塞治療方式殺死腫瘤細胞,在阻斷腫瘤的營養、血液供給的同時釋放藥物,進一步增加治療效果。此外,微球制劑還可掩蓋藥物的不良氣味,降低刺激性,提高藥物的穩定性。
本文在調研大量文獻的基礎上,從微球制劑結構分類、制備方法和應用角度分別進行闡述,以期為后續研究提供借鑒和參考。
1 微球制劑的分類和結構特點
就國內外研究現狀,根據微球制劑微觀結構的不同可將其分為實心微球、雙層微球、中空微球和多孔微球。
微球制劑被廣泛運用于長效緩釋注射劑的開發。1985 年第一個微球制劑 Enantone ( 亮丙瑞林長效緩釋注射劑) 成功上市,主要用于前列腺癌和乳腺癌的治療。通過合適方法將藥物裝載于聚合物材料中,可得到低孔隙率、表面光滑的實心微球( 圖1A) 。將實心微球通過肌內或皮下注射的方式注入體內,載體材料在體內微環境中緩慢降解,從而引起藥物的釋放,選擇合適降解速率的載體材料可以實現長達數月的藥物釋放周期。如何將其他需長期服用的藥物也成功載入實心微球中,并實現良好的長期治療效果,一度成為緩釋制劑領域的研究熱點。隨著研究的展開,諸多結果顯示,普通實心微球在包載藥物時,特別是水溶性藥物,會在釋放初期短時間內大量釋藥 [2 -3] ,出現突釋現象。較高的突釋量可能導致血藥濃度超過毒性閾值水平,產生毒副作用。

為了改善實心微球的釋藥弊端,有研究者[2,4]提出在原有載藥微球外包裹上一層聚合物外殼,引入無藥外殼作為釋放屏障可以降低藥物的突釋量。這種具有核殼結構,核心由一種聚合物材料構成,另一種聚合物材料包裹內核形成外殼的微球,被稱為雙層微球( 圖 1B) 。藥物的釋放速率可以通過殼層的厚度進行調控,附加的外殼結構也有利于提高藥物的包封率[5] 。
類比雙層微球,只保留球形外殼,球核心處為一空腔的微球,為中空微球,或空心微球( 圖 1C) 。中空微球的空腔結構非常適合藥物的裝載,因此常用作各種疏水性藥物、蛋白質、基因( 核酸) 等小分子物質的遞送載體[6] ; 此外,低密度特性和良好的漂浮性能使得中空微球也常用于胃漂浮給藥系統的研究。
普通實心微球制備過程中,有機溶劑的揮發會在微球的內部或外表面形成微小孔道。而在實心微球的處方基礎上加入致孔劑,可以在微球內外形成大量孔徑大且相互連通的孔隙,得到具有高比表面積、低密度、高孔隙率的多孔微球( 圖 1D) 。通過調節致孔劑的種類和用量可以制備得到具備良好空氣動力學粒徑的微球,因此多孔微球常用于非注射途徑的肺部吸入制劑的研究。這些獨特結構的開發使得微球制劑的應用范圍進一步擴大。
2 微球制劑的制備方法
載藥微球的制備方法繁多,常見的制備方法有溶劑揮發法、噴霧干燥法、相分離法、微流體技術、靜電噴射法等。這些方法在不同結構微球的制備中可能都有使用。但即便是同一方法,用于制備不同結構的微球時,其制備參數、結構形成原理也會有所差別,如溶劑揮發法。以下列舉了在各結構微球的制備中常用的方法。
2.1 實心微球的制備方法
2.1.1 溶劑揮發法
溶劑揮發法是制備微球常用的方法,其操作簡單、工藝參數控制方便[10] 。其制備過程可以簡單概括為將藥物溶解、分散在純化水或有機溶劑中,再與聚合物溶液混合或乳化,最后注入外水相中,隨著有機溶劑的擴散揮發得到固化微球。
Zhao 等[11] 采用溶劑揮發法制備了異哌酮的微球,使用的載體材料為聚乳酸羥基乙酸共聚物( PLGA) 。通過對聚合物濃度、均質化速度和理論載藥量等參數進行優化,制備得到了表面光滑的載藥微球,其平均粒徑為 82 μm,包封率高達 92%。
2.1.2 相分離法
相分離法是將藥物溶解、分散或以乳滴形式混合于溶有聚合物的有機溶劑中,然后向有機溶劑中加入相分離試劑,使得聚合物材料溶解度降低而析出,包裹藥物、形成凝聚相小液滴。最后引入萃取劑,除去有機溶劑和相分離試劑,固化微球 [12] 。
Chen 等[13] 采用相分離法制備了酸醋曲普瑞林微球。通過超聲將藥物粉末分散于 PLGA 溶液中,隨之向其中加入硅油作為非溶劑進行相分離,最后將上述溶液轉移至正庚烷中固化微球。通過對各項處方因素的優化,可制備得到包封率為 71.35%、突釋量低至 0.78%的載藥微球。
2.1.3 噴霧干燥法
噴霧干燥法制備微球快速、操作簡單,比較適合微球的大批量生產。通常將含有藥物和聚合材料的溶液、乳液或混懸液通過噴頭,以霧化狀態噴入熱空氣流中,干燥固化得微球粉末[14 -15] 。
Shi 等[16]采用噴霧干燥法制備了亮丙瑞林PLGA 微球。采用該法制備得到的微球表面一般略顯粗糙或帶有褶皺,聚合物濃度不高時,微球為球形; 聚合物濃度過高時,可能會出現不規則的顆粒物。體外釋放結果顯示,該載藥微球可持續緩慢釋藥 63 d。
2. 2 雙層微球的制備方法
2.2.1 改良的溶劑揮發法
制備過程和“2.1.1”項下基本一致。但制備雙層微球需要使用 2 種聚合物,根據 2 種聚合物材料在不同溶劑中的溶解度不同,在兩聚合物溶液中引入核層聚合物的不良溶劑,使得核層聚合物先固化,隨后殼層材料固化包裹核心形成雙層微球。
Naraharisetti 等[17] 采用改良的溶劑揮發法制備了慶大霉素雙層微球。選用的殼層材料為 PLGA,在二氯甲烷和乙酸乙酯中皆可溶解; 核層材料為聚左旋乳酸( PLLA) ,可溶于二氯甲烷,但不溶于乙酸乙酯。制備時將藥物和 PLLA 分散或溶解于二氯甲烷中,將 PLGA 溶解于乙酸乙酯中。將兩聚合物溶液超聲混合,PLLA 不溶于乙酸乙酯,會自發形成半固態小液滴,PLGA 在其周圍分布。最后將混合溶液轉移到外水相中,隨著溶劑的擴散揮發,核層處PLLA 先析出,外層 PLGA 隨后固化。制備得到的雙層微球粒徑在100 ~600 μm 之間且可持續緩慢釋藥15 d。
2.2.2 微流體技術
微流體技術是一種操控微體積液體的新技術[18] ,其基本原理是互不相溶的兩相溶液在微通道中交匯,在外力或流動的剪切力的作用下被分割成微米級乳液液滴,最后揮去溶劑固化得到微球。
Berkland 等[5] 采用改進的微流體技術,制備了聚乙丙交酯( PLG) 、聚( 1,6-雙羧基苯氧基) 己烷( PCPH) 的雙層微球。將 PLG 和 PCPH 分別溶解于二氯甲烷中,得到內核和外殼溶液。將內核溶液置于雙同軸噴嘴狀管路的內部通道,將外殼溶液置于外部通道。調節兩聚合物溶液的流速,用可控聲波將雙聚合物流體分割成液滴進入外水相中。制備得到的雙層微球粒徑約為 50 μm,具有明顯的核殼結構且內核處于球體的中心位置。控制 2 種聚合物溶液的流速,可調節微球的殼層厚度從2 μm 到數十 μm。
2.2.3 靜電噴射法
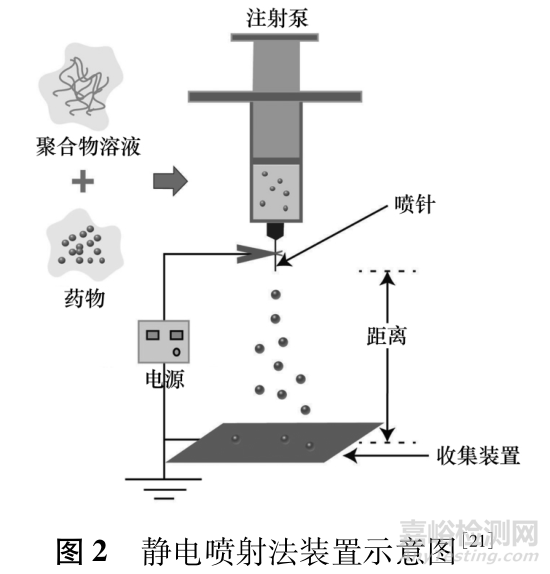
靜電噴射又稱電流體動力霧化,其制備裝置主要由外加電場、注射泵、收集裝置三部分構成( 見圖 2)[19] 。高分子溶液在外加電場的作用下獲得靜電作用力。當靜電作用力大于液滴的表面張力時,溶液在噴頭針尖噴射而出[20] 。帶同種電荷的小液滴在庫侖斥力作用下分散,進入收集裝置,最后干燥、固化,得到微球。
Zhou 等[2] 采用單針靜電噴射的方式制備了以PVA 為內核、聚己內酯( PCL) 為外殼的雙層微球,用于阿霉素的包載。首先,采用納米沉淀法制備得到含藥 PVA 納米粒。然后將 PCL 和 PVA 納米粒溶解或分散到二氯甲烷中,將此混合溶液轉移到注射器中,調節外加電壓的大小、注射針頭到收集裝置的距離、注射器流速,靜電噴射、收集、固化,得到 PVA/PCL 雙層微球。單純 PVA 納米粒體外釋放時,前 5 h的釋放量高達 69.8%,而包裹上 PCL 外殼的雙層微球的突釋量降至 33.8%。
2.3 中空微球的制備方法
2.3.1 溶劑揮發法
溶劑揮發法是制備中空微球的常用方法,操作過程同“2.1.1”。一般會使用 2種溶劑混合溶解載體材料,常用的為乙醇/二氯甲烷的混合液,間或混合異丙醇、丙酮、乙醚等。微球固化干燥階段,在連續相中溶解度較高或揮發性更好的溶劑會較快擴散除去,使得乳滴外部聚合物析出、固化、沉積形成薄膜; 而另一種溶劑緩慢擴散揮發,內部聚合物隨之固化,由內向外收縮,于中心處形成空腔,見圖 3。

Zhu 等[8] 以乙醚和乙醇為溶劑,乙基纖維素和卡波姆934P 為載體材料,通過溶劑揮發法制備了雙嘧達莫中空微球。將藥物、乙基纖維素和卡波姆 934P溶解在乙醇和乙醚混合溶液中,然后轉移到外相液體石蠟中攪拌,形成穩定乳液。乙醚快速擴散揮發,乙醇緩慢揮發除去。制備所得中空微球具有良好的漂浮性,73%以上的微球在胃液中可漂浮近12 h。
2.3.2 模板法
模板法的特點是殼層材料在氫鍵、靜電作用等方式的驅動下被吸附、固化到模板材料上,最后通過溶劑溶解、高溫煅燒、清洗等方法除去模板,得到中空微球,見圖 4。可以做模板的材料有聚合物微球、表面活性劑、膠束、囊泡等[23 -24] 。

Li 等[26]以聚 2-丙烯酰胺-2-甲基丙烷磺酸( PAMPS) 為模板,制備得到聚苯胺中空微球。將PAMPS 溶于乙醇/水混合溶劑,得到穩定膠束溶液,再向其中加入苯胺。PAMPS 分子側鏈中存在大量磺酸基,可以將苯胺吸附、穿插到 PAMPS 膠束上,最后加入過硫酸銨,在過硫酸銨的氧化作用下,苯胺聚合形成聚苯胺。經丙酮處理后,離心、干燥得到聚苯胺中空微球。調節 PAMPS/苯胺摩爾比從 1/40 到1/10 時,微球的外觀由原來的不規則狀逐漸變得均勻且圓整。制備得到的聚苯胺中空微球平均粒徑約為 410 nm,殼層的厚度約為 72 nm。
2.4 多孔微球的制備方法
2.4.1 溶劑揮發法
溶劑揮發法制備多孔微球的操作過程與“2.1.1”項下基本一致,不同之處在于多孔微球的制備需要加入致孔劑,通過調節致孔劑的種類和濃度,可以得到合適孔隙率的多孔微球。致孔劑的種類多樣,主要有氣體生成型致孔劑( 如碳酸氫銨、碳酸氫鈉、過氧化氫) 、滲透型致孔劑( 氯化鈉、氯化鉀等) 和可提取型致孔劑( Pluronic,脂肪酸鹽等) 。
Wang 等[27] 在制備牛血清白蛋白 PLGA 多孔微球時,內水相中加入碳酸氫銨作為致孔劑。碳酸氫銨在制備過程中分解釋放氣體,從微球釋出,形成孔道。
Lee 等[28] 在制備血管內皮生長因子的多孔微球時,選用牛血清白蛋白( BSA) 為致孔劑。BSA 作為滲透性致孔劑,加入內水相中,使得內水相的滲透壓高于外水相。內外水相之間的滲透壓差驅使外水相的水分子滲入內水相中,導致微球形成內外相互連接的多孔結構。
Kim 等[9] 在制備棕櫚酰化醋酸艾塞那肽微球時,致孔劑為 Pluronic。將 PLGA 和 Pluronic F68 加入二氯甲烷中超聲溶解,然后轉移到外水相乳化、揮去有機溶劑。當外水相與二氯甲烷之間發生溶劑交換時,共溶于二氯甲烷的混合物被分為 PLGA 富相和 Pluronic F68 富相。在溶劑揮發過程中,PluronicF68 從有機相被萃取分離到外水相中,形成多孔微球[29] 。
2.4.2 懸浮聚合法
懸浮聚合法也是制備多孔微球常用的方法。在混懸劑的存在下,將聚合單體、引發劑、致孔劑懸浮于液相基質中,進行聚合反應,反應完全后將致孔劑除去,即可得多孔微球。反應中常用的致孔劑為有機溶劑和線性聚合物。
Cai 等[30] 采用懸浮聚合法制備了含環氧基的多孔微球。向圓底燒瓶中加入環氧丙基炔丙醚、1,7-辛二炔、1,3-二巰基丙烷、安息香二乙醚( DMPA) 、聚乙二醇( PEG) 和氯仿,其中 DMPA 為光引發劑,PEG 為聚合物型致孔劑。攪拌均勻后,加入十二烷基苯磺酸鈉溶液,將燒瓶浸入冰水浴中、紫外線照射下攪拌反應。環氧丙基炔丙醚、1,7-辛二炔、1,3-二巰基丙烷在低溫條件下進行光引發的聚合反應。致孔劑 PEG 在反應生成的聚硫醚中不可溶,發生相分離。反應完成后水洗可除去 PEG,得到多孔微球。相比于小分子溶劑型致孔劑( 甲苯、正庚烷等) ,聚合物型致孔劑 PEG 的分子量和黏度較高,有利于相分離和大孔隙的形成。調節 PEG 的用量,可得到孔隙率為62.45%、孔徑5~10 μm、且孔洞連續的多孔微球。
3 微球制劑在醫藥領域的應用
3.1 實心微球的應用
3.1.1 長效緩控釋注射劑
現已有 10 余個注射用緩釋微球產品成功投入市場[31] ,包載的藥物主要為多肽類和精神類藥物。多肽類藥物一般半衰期較短,口服生物利用度極低,因而多采用注射給藥; 若對應病癥需要長期給藥治療,頻繁注射會給患者造成極大痛苦和不便。精神病治療周期較長,患者拒服或漏服藥物都可能加重病情。將上述藥物制成長效微球制劑可顯著提高患者的用藥順應性。
Pervaiz 等[32] 制備了非典型抗精神病藥物奧氮平的 PLGA 微球制劑。將微球懸浮于生理鹽水通過皮下注射進入大鼠體內,以考察載藥微球的體內釋藥行為。結果顯示,合理調控共聚物中乳酸和羥基乙酸的比例和分子量,可以得到低突釋、平穩釋藥 1個月的緩釋微球制劑。
3.1.2 動脈栓塞給藥
微球的動脈栓塞治療,即在X 光照射下,將載藥微球通過導管注入腫瘤動脈中,阻斷腫瘤處血液、氧氣和營養物質的供應[33] ; 同時在病灶部位緩慢釋放抗癌藥物,實現治療腫瘤的目的。目前,已成功上市的栓塞微球產品有英國 Bio-compatibles 公司的 DC Bead 、美國 BioSphere 公司的 Hepasphere 和國內恒瑞公司的 CalliSpheres 和 8Spheres 。其中 CalliSpheres 是國內首創且擁有獨立知識產權的栓塞微球產品,通過物理作用吸附裝載化療藥物,具有載藥量大、可載藥種類多等優勢。
Chen 等[34] 制備了改性絲蛋白動脈栓塞微球。采用兔耳模型對微球的栓塞效果進行了評價,將微球注入兔耳中央動脈后的第 3 周,兔耳動脈萎縮消失,遠心端周圍組織壞死,表明該微球具備良好的栓塞作用。
3.2 雙層微球的應用
3.2.1 改善實心微球的突釋問題
傳統的單層微球裝載藥物時,特別是親水性藥物,會存在突釋過高、包封率不高的情況。而雙層微球中,藥物被包裹在內核聚合物中,無藥外層作為釋放屏障,可以顯著降低藥物的突釋量。
Devrim 等[35] 制備了包載親水性藥物卵清蛋白的雙層微球。采用的2 種聚合物材料是 PLGA ( 50/50)和其他型號 PLGA 或聚乳酸的組合。實驗結果表明,相比單一聚合物 PLGA( 50/50) 制備得的實心微球,雙層微球顯著降低了藥物的突釋量,提高了包封率。單層微球包封率為 64.11%,突釋量為 44.11%;PLGA( 50/50) 、聚乳酸雙層微球突釋量僅為10.36%,包封率可達93.98%。
3.2.2 實現聯合用藥
許多疾病的治療需要多種藥物聯合使用,如腫瘤的化療[36] 、帕金森病后期患者的治療還有高血壓[37] 等疾病的治療。雙層微球可將 2 種藥物分別載入內核和外殼中,發揮協同治療作用[38] 。
Xu 等[39] 制備了聚乳酸殼層包裹 PLGA 內核形成的雙層微球。將阿霉素載入雙層微球的內核,殼聚糖-DNA 納米粒( chi-p53) 載入外殼中。阿霉素通過抑制核酸復制導致癌細胞凋亡; 殼聚糖-DNA 納米粒內含編碼 p53 腫瘤抑制蛋白的基因,可使癌細胞對抗癌藥物敏感。該研究中,雙層微球同時釋放阿霉素和 chi-p53,與分別裝載 Dox 和 chi-p53 的微球或相應的游離藥物相比,對肝癌 HepG2 細胞的增殖具有更高的抑制作用。
3.3 中空微球的應用
3.3.1 胃漂浮給藥系統
胃漂浮給藥系統是一種相對密度低于胃內容物而漂浮于胃液之上的制劑,能延長藥物在胃部滯留時間,提高生物利用度[40] 。中空微球具有低密度特性和良好的漂浮性能,是一種新型、備受關注的多單元胃漂浮給藥系統。相比一單元給藥的漂浮片劑,漂浮微球能顯著減小個體差異,避免藥物劑量“全或無”的不良現象,弱化消化道食物節律帶來的影響[41] 。
Wei 等[42] 制備了乙基纖維素的中空漂浮微球,用于包載抗潰瘍藥物鹽酸雷尼替丁。體外實驗結果顯示,該制劑在人工胃液中的漂浮時間和持續釋藥時間長達 24 h。體內藥動學實驗數據表明,相比市售膠囊劑,該中空微球減少了血藥濃度的波動,且生物利用度約為膠囊劑的 3 倍。
3.3.2 響應性釋放
中空微球主要由球形外殼和內部空腔構成,沒有致密的內核。若選用功能性材料制備中空微球的外殼,可以使中空微球對外部環境刺激( 如 pH、磁場、溫度等) 產生相應變化[43],從而實現藥物的響應性釋放。
Li 等[44] 選用聚乙二醇殼聚糖接枝共聚物( CS-g-PEG) 為陽離子材料,檸檬酸鹽修飾的四氧化三鐵納米粒( Fe?O? -CA) 為陰離子材料,制備了具有 pH 響應性磁性復合中空微球。將抗腫瘤藥物阿霉素通過孵育的方式載入響應性中空微球。該微球的體外釋放結果顯示,在低 pH 的釋放介質中,微球釋藥速度較快,此時 CS-g-PEG 中的氨基被質子化,導致微球殼層膨脹,通透性增加,有助于實現藥物在酸性腫瘤微環境中的釋放。此外,由于Fe?O? -CA的摻入,中空微球的磁化強度為 64.14%,飽和磁化強度為37.23 emu·g-1 ,顯示出良好的磁靶向潛能。
3.4 多孔微球的應用
3.4.1 干粉吸入型肺部給藥
肺部給藥具有無首過效應、吸收迅速等優勢。載藥粒子要實現有效的肺部沉積,要滿足空氣動力學粒徑在 1 ~ 5 μm( 小于 0. 5 μm 時,載藥粒子會被氣流呼出) 、幾何粒徑大于 10 μm( 小于 5 μm 時會被巨噬細胞吞噬清除)[45 -46] 。普通實心微球空氣動力學粒徑和幾何粒徑近乎相等,并不能滿足肺部給藥的要求。而多孔微球可以通過調節粒徑和孔隙率成功在肺部沉積,同時實現藥物的控制釋放,這使得多孔微球成為近年來最受關注的肺部給藥的載體之一[47] 。
Feng 等[48] 制備了包載阿霉素和紫杉醇的多孔PLGA 微球,通過吸入途徑進入肺部,以治療肺癌。制備得到微球的幾何平均粒徑為( 11.47 ±2.71) μm,空氣動力學粒徑為( 3.52 ± 0.83) μm,有利于形成氣溶膠,沉積于肺部。動物實驗結果表明,該載藥多孔微球抑制了 B16F10 細胞致瘤小鼠的肺部癌細胞的擴散增殖,具有良好的肺部抗腫瘤效果。
3.4.2 經皮給藥
由于多孔微球具有比表面積大、吸附性能好等獨特優勢,用于經皮給藥系統時,能有效吸收皮膚表面的分泌物,為創面提供有效保護。多孔微球粒子是微小、惰性球體,不會透過皮膚進入體循環,具有良好的安全性。將藥物載入多孔微球可實現藥物的緩慢釋放,在不降低藥物療效的前提下顯著減少藥物對創面的刺激性。且多孔微球在使用體驗上優于軟膏,不會帶來油膩、黏稠的不適感,同時清洗方便[49] 。
Zhang 等[50] 制備了包載積雪草苷的多孔微球。積雪草苷可促進創面處成纖維細胞增殖、膠原蛋白合成以及血管再生。體外釋放實驗顯示,該積雪草苷多孔微球可穩定持續釋藥 25 h。在大鼠背部創傷部位每 2 d 涂抹一次積雪草苷多孔微球,每 4 d 記錄一次創面面積以考察該制劑對創面愈合的作用。相比游離藥物組和空白對照組,載藥多孔微球組促進傷口愈合的作用趨勢更明顯,并于 d 7 和 d 14 表現出顯著性差異。
3.4.3 組織再生支架
近年來,多孔微球被廣泛應用于組織工程研究中,以幫助細胞生長和修復缺陷組織。多孔微球具有高孔隙率、比表面積大的結構特性,有利于細胞的黏附、遷移和增殖[5,52] 。微球之間的孔隙和微球表面的小孔隙都為血管和細胞的生長提供了空間,同時也可將細胞生長因子等藥物載入多孔微球中,促進組織再生過程中的細胞增殖。
Seong 等[53] 制備了磷酸鈣、膠原蛋白復合多孔微球,以包載促進骨再生的生長因子,其中載體材料磷酸鈣陶瓷具備良好的生物可降解性。將該多孔微球植入髕骨外側脫位的雄兔體內 4 周后,在原骨骼缺陷處生長出了新生骨組織。結果表明,裝載生長因子的多孔微球能有效地促進組織再生。
3.4.4 有望縮短實心微球的釋藥停滯期
藥物從實心微球中的釋放主要由擴散和聚合物降解機制主導,通常呈現出三相釋放模式: 突釋期、釋放停滯階段、釋放后期。骨架材料降解緩慢,藥物無法從微球中擴散釋放時,藥物的釋放會出現較長的停滯期。在釋藥停滯期,為維持有效血藥濃度需要輔助口服給藥[54] ,從而顯著降低了患者的用藥順應性,不利于臨床治療。多孔微球具有較高的孔隙率、比表面積,有利于藥物的擴散和體液的浸入,在縮短停滯期方面具有較高的潛在價值。
Kim 等[55] 分別制備了包載孕酮的多孔、實心PLGA 微球,對 2 種不同結構微球的關鍵質量屬性進行了考察。藥物釋放曲線顯示,多孔微球釋藥速度快于實心微球,且無明顯的停滯期,可持續釋放孕酮長達 16 d,能實現藥物的持續不間斷釋放。
4 結語
微球制劑問世至今,受到了醫藥領域的廣泛關注,現已有數十個微球產品成功上市,主要包括長效緩釋微球和栓塞微球,皆為實心微球。目前對于其他結構微球的研究還處在發展階段,并未有產品獲準進入臨床使用。此外,關于各結構微球的研究尚存在許多不足之處,有待進一步優化。例如,實心微球用于長效緩釋注射劑時,存在著高突釋、中期釋藥停滯等問題; 雙層微球結構重現性差,質量控制困難; 中空微球包載藥物時普遍存在包封效率低等問題; 多孔微球制備過程中加入的致孔劑并不能完全除去,且用作肺部吸入給藥時存在潛在刺激性。
對于已經上市的微球產品而言,建立具備良好體內外相關性的釋放方法、完善現有質量評價標準仍是今后研究中亟待解決的問題。對于還處在研發階段的微球制劑,如何提高包封效率、優化體外釋藥行為、發揮體內治療作用以及實現產業化,都是當下的研究熱點和難點。相信隨著研究工作的深入,關于各結構微球的制備方法、質量評價、應用研究會逐步得到完善。

來源:Internet


