您當前的位置:檢測資訊 > 科研開發
嘉峪檢測網 2021-09-10 10:26
膠原蛋白是人和動物組織中一類重要的結構蛋白,廣泛存在于肌腱、韌帶、軟骨、皮膚及其他結締組織中,是哺乳動物體內含量最多、分布最廣的功能性蛋白質。膠原蛋白作為生物材料具有良好特性,因此在醫藥、組織工程、醫美護膚、食品、化工等領域得到廣泛應用。
動物源為主流,重組膠原為未來更迭趨勢
按來源和加工方法,膠原蛋白生物材料可分為動物組織提取膠原蛋白和重組膠原蛋白兩大類。目前動物膠原仍是膠原蛋白原料的主要來源,天然獲取的膠原一般從牛、豬、鼠、 魚類等動物的肌腱、真皮和尾巴中提取。重組人源膠原蛋白有望成產業技術更迭趨勢,目前可進入工業化生產或已商品化的重組膠原蛋白主要基于大腸桿菌、酵母菌等進行表達。
膠原蛋白產業鏈發展逐漸成熟
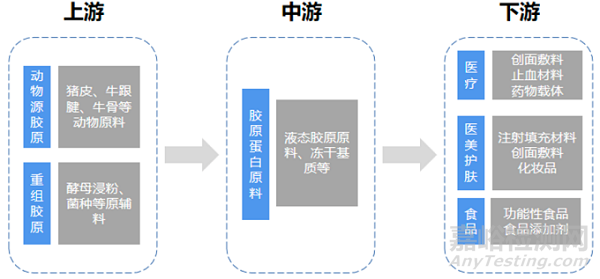
膠原蛋白產業鏈上游由制備膠原蛋白所需的原料供應商組成,動物源膠原生廠商需要采購豬皮、牛跟腱等動物原料,重組膠原生廠商需采購酵母浸粉、菌種等原輔料;產業鏈中游為廠商生產膠原蛋白原料,包括液態膠原原料、凍干基質等;下游膠原蛋白應的用場景廣泛,主要可生產涵蓋醫療、醫美護膚、食品三大領域的終端產品。
膠原賽道成為醫療器械市場新風口
膠原蛋白在醫療領域應用廣泛,已成為未來膠原蛋白市場的重要驅動力。如:
創面敷料:用于皮膚修復、口腔修復、神經外科修復等;
止血材料:尤其對肝、脾等創傷止血效果明顯;
藥物載體:結合抗生素、蛋白類、基因類藥物,構建多樣藥物載體釋放體系。
而在醫療器械領域,膠原蛋白產品主要應用有膠原蛋白縫合線、膠原基骨科填充和修復材料、整形用膠原蛋白植入劑、膠原蛋白組織工程支架材料、膠原蛋白敷料等。
監管部門高度重視膠原產業創新發展
為鼓勵重組膠原蛋白產業研發創新,推動相關領域高質量發展,結合產業發展實際和監管工作需要,2021年來監管部門陸續發布系列文件,具體如下:
2021年3月3日,中檢院醫療器械檢定所對外發布《關于征集重組膠原蛋白標準起草驗證單位和重組膠原蛋白標準化工作工作組專家的通知》;
2021年3月15日,國家藥監局對外發布《重組膠原蛋白生物材料命名指導原則》(2021年第21號通告),進一步規范重組膠原蛋白生物材料命名,推動新型生物材料高質量發展;
2021年3月18日,國家藥監局綜合司發布關于《重組膠原蛋白》和《組織工程醫療器械產品 膠原蛋白 第3部分:膠原蛋白含量檢測-液相色譜儀-質譜法》醫療器械行業標準立項的通知【藥監綜械注〔2021〕34號 】;
2021年4月15日,國家藥監局關于發布《重組膠原蛋白類醫療產品分類界定原則》(2021年第27號通告) ;
2021年7月30日,中檢院在北京召開《重組膠原蛋白》行業標準審查會。
膠原蛋白質量控制,至關重要!
膠原蛋白是具有生物活性的大分子,空間結構復雜,作為醫療產品使用時,它的化學性能、物理性能及生物性能對產品的安全性非常關鍵。因此,膠原蛋白產品的質量評價應從這三個方面來考慮,建立相應的質控項目和指標。同時,根據不同工藝階段樣品特性,選擇和建立合適的樣品處理和檢測方法,并經過驗證。
目前,關于膠原蛋白質量控制的相關標準有國家標準、行業標準、地方標準、技術共識等,主要參考文件有:
YY 0954-2015,《無源外科植入物 Ⅰ型膠原蛋白植入劑》;
YY/T 1453-2016,《組織工程醫療器械產品 I型膠原蛋白表征方法》;
YY/T 1511-2017,《膠原蛋白海綿》;
中國食品藥品檢定研究院醫療器械檢定所,《醫用膠原蛋白類產品的表征和質量控制》技術共識(征求意見稿)


來源:國家藥監局


