您當前的位置:檢測資訊 > 科研開發
嘉峪檢測網 2024-11-08 08:11
摘 要: 建立高效液相色譜法測定熱感賽比斯坦顆粒中的嗎啡含量。采用Waters RP-C18色譜柱(250 mm×4.6 mm,5 μm)為分離柱,以乙腈-0.01 mol/L磷酸二氫鉀和0.05 mol/L庚烷磺酸鈉混合溶液(pH 3.5)(體積比為5∶95)為流動相,流量為1.0 mL/min,檢測波長為230 nm,柱溫為28 ℃。嗎啡的質量濃度在0.24~23.70 μg/mL范圍內與色譜峰面積線性關系良好,相關系數為0.999 9,方法檢出限為0.14 μg/mL,定量限為0.22 μg/mL。樣品加標平均回收率為99.05%,測定結果的相對標準偏差為1.62%。該方法適用于熱感賽比斯坦顆粒及原料藥材罌粟殼中嗎啡含量的測定。
關鍵詞: 熱感賽比斯坦顆粒; 高效液相色譜法; 嗎啡
熱感賽比斯坦顆粒是由艾克木·穆罕默德·艾扎木汗于1874年撰寫的維醫典籍《醫科思熱·愛扎穆》第723頁收藏的經典名方,處方由破布木果、大棗、罌粟殼、甘草等12味藥材組成,其制備工藝為將處方藥材粉碎成粗粉,加水煎煮3次,每次1 h,過濾,合并濾液后濃縮成膏狀,加入糖粉制成顆粒制劑。該中成藥制劑具有清除異常膽液質、止咳、化痰的功效,可用于治療熱性感冒咳嗽、呼吸道感染等癥狀[1]。其處方中的罌粟殼為罌粟科植物罌粟Papaver somniferum L.的干燥成熟果實,味酸澀,性平,專治久咳、久瀉、脫肛、脘腹疼痛[2]。現代藥理及化學研究表明,罌粟殼藥材主要藥效成分為生物堿類,其中以嗎啡為主,具有顯著的鎮痛、鎮咳作用,并能使胃腸道及其括約肌的張力提高、消化液分泌減少、便意遲鈍,從而起到止瀉的作用[3]。在中成藥中罌粟殼藥材常作為處方原料用于治療久咳、久瀉等癥狀[4?5],但同時它具有成癮性,當人體攝入嗎啡達到一定量時會產生精神依賴性[6?7],因此控制制劑中的嗎啡含量尤為重要。
在《中華人民共和國衛生部 藥品標準 維吾爾藥分冊》[8]中僅對熱感賽比斯坦顆粒中藥材罌粟殼進行了定性鑒別,沒有相關含量測定的標準方法,對該制劑的藥品質量和安全性難以進行有效控制。目前對熱感賽比斯坦顆粒中生物堿含量及其他制劑中嗎啡含量的測定已有相關報道[9?10],但對于熱感賽比斯坦顆粒及原料藥材罌粟殼中嗎啡含量的測定還未見報道。劉新豫等對熱感賽比斯坦顆粒中生物堿的含量進行了測定[9],但該方法色譜峰保留時間較短,易受流動相的干擾。筆者通過優化色譜條件和樣品處理條件,建立了高效液相色譜法測定熱感賽比斯坦顆粒及其處方原料藥材罌粟殼中嗎啡的含量。通過測定原料藥材罌粟殼及熱感賽比斯坦顆粒中嗎啡的含量,可明確原料藥材在制劑中的轉移率,以確保臨床應用的安全性和有效性。該方法簡便、準確性、專屬性較好,可為該制劑的質量和用藥安全提供技術保障。
1、 實驗部分
1.1 主要儀器與試劑
高效液相色譜儀:Waters e 2695型,沃特世科技(上海)有限公司。
數控超聲波清洗器:KH-300DE型,昆山禾創超聲儀器有限公司。
電子天平:BT125D型,感量為0.01 mg,德國賽多利斯公司。
甲醇、乙腈:均為色譜純,美國賽默飛世爾科技公司。
嗎啡對照品:質量分數為98%,批號為171201-201123,中國藥品生物制品鑒定所。
熱感賽比斯坦顆粒樣品:批號分別為20200209、20200215、20200224,新疆和田維吾爾藥業股份有限公司。
實驗用水為一級水。
1.2 色譜條件
色譜柱:Waters RP-C18柱(250 mm×4.6 mm,5 μm,美國沃特世科技有限公司);柱溫:28 ℃;檢測波長:230 nm;進樣體積:10 μL;流動相:乙腈-0.01 mol/L磷酸二氫鉀和0.05 mol/L庚烷磺酸鈉混合溶液(PH 3.5) (體積比為5∶95);流量:1.0 mL/min。
1.3 溶液配制
嗎啡對照品溶液:0.237 mg/mL,精密稱取嗎啡對照品適量,置于10 mL容量瓶中,用20%(除特殊說明外,均為體積分數)的甲醇溶液(含5%乙酸)溶解并稀釋至標線,混勻,于4 ℃下避光保存。
嗎啡對照品系列工作溶液:精密量取0.005、0.010、0.025、0.050、0.25、0.50 mL嗎啡對照品溶液,分別置于5 mL容量瓶中,用20%的甲醇溶液(含5%乙酸)定容至標線,搖勻,配制成嗎啡的質量濃度分別為0.24、0.47、1.19、2.37、11.85、23.70 μg/mL的系列工作溶液。
1.4 樣品處理
將熱感賽比斯坦顆粒研細后取3.0 g,精密稱定,置于具塞錐形瓶中,加入4 mL氨水,充分濕潤,靜置10 min,稱量并記錄其質量,加入30 mL三氯甲烷,密封,超聲30 min。冷卻至室溫,再次稱量并記錄其質量,加入三氯甲烷補足減失的質量,然后過濾,取20 mL濾液濃縮至近干,加入甲醇定容至10 mL容量瓶中,搖勻,得樣品溶液[8]。
取罌粟殼藥材粉末約0.5 g,精密稱定,同法制備罌粟殼藥材溶液。
按熱感賽比斯坦顆粒處方中藥材比例及制備工藝,制備缺少罌粟殼藥材的陰性樣品,同法制備陰性樣品溶液。
1.5 定量方法
取對照品溶液、樣品溶液、陰性樣品溶液,按照1.2色譜條件測定,以色譜峰面積外標法計算嗎啡的含量。
2、 結果與討論
2.1 色譜條件優化
2.1.1 流動相選擇
分別選擇乙腈-0.5%乙酸銨溶液(含0.08%三乙胺)、乙腈-0.01 mol/L庚烷磺酸鈉溶液和0.02 mol/L磷酸二氫鉀溶液的等量混合液(用10%磷酸溶液調節pH值至2.8)、乙腈-0.01 mol/L磷酸二氫鉀溶液(用5%磷酸溶液調節pH值至2.7)、乙腈-0.01 mol/L磷酸二氫鉀和0.05 mol/L庚烷磺酸鈉混合溶液(用5%磷酸溶液調節pH值至3.5) (體積比為5∶95)作為流動相[11?14],考察不同流動相體系時目標物的分離效果。結果表明,以乙腈-0.5%乙酸銨溶液(含0.08%三乙胺)、乙腈-0.01 mol/L庚烷磺酸鈉溶液和0.02 mol/L磷酸二氫鉀溶液的等量混合液(pH 2.8)為流動相時,嗎啡出現雙峰;以乙腈-0.01 mol/L磷酸二氫鉀溶液(pH 2.7)為流動相時,色譜峰基線漂移;以乙腈-0.01 mol/L磷酸二氫鉀和0.05 mol/L庚烷磺酸鈉混合溶液(pH 3.5)為流動相時,色譜峰基線平穩,嗎啡色譜峰分離度及峰形良好,因此選擇乙腈-0.01 mol/L磷酸二氫鉀和0.05 mol/L庚烷磺酸鈉混合溶液(pH 3.5) (體積比為5∶95)作為流動相。
2.1.2 波長選擇
波長的選擇對色譜峰面積有較大影響,繼而影響測定結果的準確度。在200~800 nm波長范圍內,掃描嗎啡對照品溶液。結果表明,嗎啡的最大吸收波長為230 nm,故選擇檢測波長為230 nm。
2.1.3 柱溫的選擇
色譜柱溫度對目標物的分離效果有較大影響。考察色譜柱溫度分別為25、28、30 ℃時嗎啡的分離效果[15?17]。結果表明,當色譜柱溫度在25 ℃時,色譜峰有拖尾現象,分離度不佳;當溫度為30 ℃時,色譜峰基線漂移且分離度差;當溫度為28 ℃時,色譜峰基線穩定,分離度好,因此選擇色譜柱溫度為28 ℃。
2.2 樣品處理條件優化
在制備熱感賽比斯坦顆粒樣品溶液時,分別選擇乙腈-0.01 mol/L磷酸二氫鉀和0.05 mol/L庚烷磺酸鈉混合溶液(pH 3.5)[18]、75%乙醇、75%甲醇和氨水4種溶劑濕潤樣品,然后加入三氯甲烷進行提取。結果表明,樣品經氨水濕潤后,加入三氯甲烷超聲提取,提取溶液中嗎啡色譜峰形良好且峰面積最大,因此在制備樣品溶液時用氨水濕潤樣品后加入三氯甲烷超聲提取。
選擇超聲時間分別為20、30、40 min進行試驗。結果表明,當超聲時間為20 min時,嗎啡的色譜峰面積小于超聲時間為30 min和40 min時的色譜峰面積,而超聲時間為30 min和40 min時的色譜峰面積基本相同,考慮到檢測效率,選擇超聲時間為30 min。
2.3 方法專屬性
取嗎啡對照品溶液、熱感賽比斯坦顆粒樣品溶液、罌粟殼藥材溶液、陰性樣品溶液,在1.2色譜條件下分別進樣測定,色譜圖如圖1所示。由圖1可以看出,嗎啡對照品溶液、熱感賽比斯坦顆粒樣品溶液、罌粟殼藥材溶液在相同的保留時間處具有同一色譜峰,嗎啡色譜峰分離度大于1.5,理論塔板數按嗎啡色譜峰計不低于5 000,而陰性樣品溶液中無相應的色譜峰,表明該方法專屬性良好。

圖1 高效液相色譜圖
Fig. 1 High performance liquid chromatography chart
2.4 線性方程與檢出限
在1.2色譜條件下,分別測定嗎啡對照品系列工作溶液,記錄色譜圖,以目標物的質量濃度為橫坐標(x),以色譜峰面積為縱坐標(y),繪制標準工作曲線,得線性方程為y=2.71×106x+1.05×104,相關系數為0.999 9。結果表明,嗎啡的質量濃度在0.24~23.70 μg/mL范圍內與色譜峰面積線性關系良好。
取嗎啡對照品溶液適量,用20%的甲醇溶液(含5%乙酸)逐級稀釋,在1.2色譜下進行測定,分別以3倍信噪比和10倍信噪比對應的質量濃度作為方法檢測限和定量限。該方法的檢測限為0.14 μg/mL,定量限為0.22 μg/mL。
2.5 精密度試驗
取熱感賽比斯坦顆粒樣品6份,每份3.0 g,精密稱定,按1.4方法制備樣品溶液,在1.2色譜條件下進行測定,記錄色譜峰面積,結果見表1。由表1可知,測定結果的相對標準偏差(RSD)為1.62%,表明該方法精密度良好。
表1 精密度試驗結果
Tab. 1 Results of precision test

2.6 樣品溶液穩定性試驗
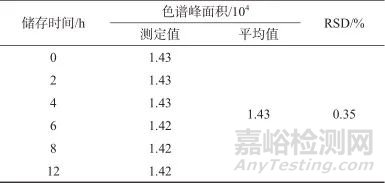
按1.4方法制備樣品溶液,于室溫下儲存,分別于第0、2、4、6、8、12 h進樣測定,記錄色譜峰面積,結果見表2。由表2可知,色譜峰面積測定結果的相對標準偏差為0.35%,表明樣品溶液在室溫下放置12 h穩定性良好。
表2 穩定性試驗結果
Tab. 2 Results of stability test
2.7 樣品加標回收試驗
取熱感賽比斯坦顆粒樣品9份,平均分為3組,每份3.0 g,精密稱定,按1.4方法制備樣品溶液,在1.2色譜條件下進樣測定。根據各組中嗎啡的平均含量,分別精密加入適量的嗎啡對照品溶液,使嗎啡的加入量分別相當于其含量的80%、100%、120%,在1.2色譜條件下進樣測定,結果見表3。由表3可知,樣品加標平均回收率為99.05%,表明該方法準確度良好。
表3 樣品加標回收試驗結果
Tab. 3 Sample spiked recovery test results

3、 結語
通過優化色譜條件和樣品處理條件,建立了高效液相色譜法測定熱感賽比斯坦顆粒中的嗎啡含量。該方法準確、簡單、方便,適用于熱感賽比斯坦顆粒及其處方原料藥材罌粟殼中嗎啡的含量測定,為該制劑的制備以及臨床用藥的安全性提供依據。
參考文獻:
1 國家中醫藥管理局《中華本草》編委會.中華本草:維吾爾藥卷[M].上海:上海科學技術出版社,2015:310.
Editorial Board of Chinese Materia Medica,State Administration of Traditional Chinese Medicine. Chinese herbal medicine:Uyghur medicine roll[M]. Shanghai:Shanghai Scientific and Technical Publishers,2015:310.
2 中華人民共和國衛生部藥典委員會.中華人民共和國藥典(2020年版):一部[M].北京:中國科技醫藥出版社,2020.
Pharmacopoeia Committee of the Ministry of Health of the People's Republic of China. Pharmacopoeia of the People's Republic of China(2020 Edition):Part One[M]. Beijing:China Medical Science and Technology Press,2020.
3 中國醫藥科學院藥用研究所.中藥志:第3冊[M].北京:人民衛生出版社,1984:685.
Institute of Medicinal Sciences. Chinese Academy of Medical Sciences. Journal of Traditional Chinese Medicine:Volume 3[M]. Beijing:People's Health Publishing House,1984:685.
4 鐘贛生.中藥學[M].北京:中國中醫藥出版社,2016:428.
ZHONG Gansheng. Chinese pharmac[M]. Beijing:China Press of Traditional Chinese Medicine,2016:428.
5 阿不都克熱木•阿不都熱合曼,馬麗,韓夢婷,等.祖卡木顆粒和罌粟殼提取液對小鼠行為學的影響[J].現代中藥研究與實踐,2019,33(4):33.
Abudoukeremu·Abudoureheman,MA Li,HAN Mengting,et al. Effects of Zukamu Granules and Poppy shell extract on behavior of mice[J]. Research and Practice on Chinese Medicines,2019,33(4):33.
6 薛楚,劉思雪,黃芳.罌粟科植物罌粟、延胡索和巖黃連鎮痛作用的研究進展[J].藥學研究,2019,38(5):290.
XUE Chu,LIU Sixue,HUANG Fang. Research progress on the analgesic effect of Poppy,Rhizoma Corydalis and Corydalis saxicola Bunting[J]. Journal of Pharmaceutical Research,2019,38(5):290.
7 譚為,楊秀穎,張莉,等.中藥罌粟殼毒的歷史認識與現代研究[J].中藥藥理與臨床,2019,35(2):159.
TAN wei,YANG Xiuying,ZHANG Li,et al. Historical understanding and modern research on Papaver shell poison in traditional chinese medicine[J]. Pharmacology and Clinics of Chinese Materia Medica,2019,35(2):159.
8 中華人民共和國衛生部藥典委員會.中華人民共和國衛生部 藥品標準 維吾爾藥分冊[M].新疆:新疆科技衛生出版社,1998:180.
Pharmacopoeia Committee of the Ministry of Health of the People's Republic of China. Drug Standards of the Ministry of Health of the People's Republic of China:Uigher Medicine[M]. Xinjiang:Xinjiang Science and Technology Health Publishing House,1998:180.
9 劉新豫,唐輝,翟欣,等. RP-HPLC法測定熱感賽比斯坦顆粒中3種生物堿成分的含量[J].藥物分析雜志,2017,37(5):897.
LIU Xinyu,TANG Hui,ZHAI Xin,et al. Determination of 3 alkaloids in Regan Saibisitan Granules by RP-HPLC method[J]. Chinese Journal of Pharmaceutical Analysis,2017,37(5):897.
10 周鋼,馬方圓,單蓮蓮,等.高效液相色譜法測定尿通卡克乃其片中嗎啡含量[J].中國藥業,2023,32(17):83.
ZHOU Gang,MA Fangyuan,SHAN Lianlian,et al. Content determination of morphine in Niaotongkakenaiqi Tablets by HPLC[J]. China Pharmaceuticals,2023,32(17):83.
11 鄢長余,趙月然,姜范成,等. HPLC法同時測定桂靈片中6種生物堿的含量[J].中國藥物評價,2019,36(3):184.
YAN Changyu,ZHAO Yueran,JIANG Fancheng,et al. Simultaneous determination of six alkaloids in Guiling Tablets by HPLC[J]. Chinese Journal of Drug Evaluation,2019,36(3):184.
12 楊麗蓉,隋海山,張筱,等.復方甘草片中可待因和嗎啡的含量測定及分析[J].中國藥品標準,2021,22(1):67.
YANG Lirong,SUI Haishan,ZHANG Xiao,et al. Determination and analysis of the contents of codeine and morphine in Compound Liquorice Tablets[J]. Drug Standards of China,2021,22(1):67.
13 劉學,劉歡歡,肖婷,等. HPLC同時測定咳清膠囊中嗎啡、磷酸可待因和巖白菜素含量[J].中國現代應用藥學,2022,39(6):783.
LIU Xue,LIU Huanhuan,XIAO Ting,et al. Simultaneous determination of morphine,codeine phosphate and bergenin in Keqing Capsules by HPLC[J]. Chinese Journal of Modern Applied Pharmacy,2022,39(6):783.
14 劉學,邱紅燕,彭靜,等.咳清膠囊的質量標準提高研究[J].中國藥房,2020,31(5):595.
LIU Xue,QIU Hongyan,PENG Jing,et al. Study on the improvement of quality standard for Keqing Capsules[J]. China Pharmacy,2020,31(5):595.
15 李晶,陳超,文萍,等.一測多評法測定枇杷止咳軟膠囊中硫酸嗎啡和磷酸可待因的含量及其應用拓展[J].江西中醫藥大學學報,2019,31(6):67.
LI jing,CHEN Chao,WEN Ping,et al. Simultaneous assay of morphin sulfate and codeine phosphate in Pipa Zhike Soft Capsule through quantitative analysis of multi-components by single marker and its application[J]. Journal of Jiangxi College of Traditional Chinese Medicine,2019,31(6):67.
16 袁鵬,李蕊,楊瑞春.高效液相色譜-熒光法測定罌粟殼中罌粟堿[J].中國衛生檢驗雜志,2020,30(13):1 562.
YUAN Peng,LI Rui,YANG Ruichun. Determination of papaverine in poppy shell by high performance liquid chromatography with fluorescence detection[J]. Chinese Journal of Health Laboratory Technology,2020,30(13):1 562.
17 黃硯,刁灝瑒,張雁.克咳片中8個成分的含量測定[J].藥物分析雜志,2020,40(2):337.
HUANG Yan,DIAO Haoyang,ZHANG Yan. Determination of 8 constituents in Keke Tablets[J]. Chinese Journal of Pharmaceutical Analysis,2020,40(2):337.
18 鮑實,孫春艷. HPLC法測定福爾可定原料中的嗎啡及可待因雜質[J].中國藥師,2019,22(12):2 361.
BAO Shi,SUN Chunyan. Determination of morphine and codeine in Pholcodine materials by HPLC[J]. China Pharmacist,2019,22(12):2 361.
引用本文: 蔡美玲,唐輝,龐克堅,等 . 高效液相色譜法測定熱感賽比斯坦顆粒中嗎啡含量[J]. 化學分析計量,2024,33(9):90. (CAI Meiling, TANG Hui, PANG Kejian, et al. Determination of morphine content in Regan Saibisitan Granules by high performance liquid chromatography[J]. Chemical Analysis and Meterage, 2024, 33(9): 90.)

來源:化學分析計量


