您當前的位置:檢測資訊 > 科研開發
嘉峪檢測網 2024-04-28 17:47
本文對制藥用水微生物監測項目的取樣過程中使用消毒劑進行消毒操作的必要性進行了探討。采取的方法是選取 1 個實驗室純化水系統的 6 個取水點,14 天周期內進行 10 天微生物限度樣品的取樣測試,每個取樣點微生物限度消毒與不消毒取樣操作各取 1 份樣品,按照《中國藥典》2020 年版 二部 純化水進行微生物限度測試。測試結論是試驗中所有檢測水點兩種取樣方式樣品的微生物限度檢測結果均符合限值標準的要求,檢測結果沒有顯著差異,結果一致。說明取樣人員在取樣標準操作規程下規范取樣,制藥用水取樣過程中微生物限度樣品取樣不消毒操作是可以接受的,能夠客觀真實地反映制藥水系統取樣點的微生物指標。
《中國藥典》2020 年版中制藥用水的監測項目為性狀、酸堿度、硝酸鹽、亞硝酸鹽、氨、電導率、總有機碳(TOC)、易氧化物(與 TOC 項目二選一)、不揮發物、重金屬、微生物限度和細菌內毒素(注射用水)[1]。中國藥典 2025 年版的編制大綱已于 2022 年 12 月 19 日正式發布,在第六章四部里面明確提出“跟進制藥用水國際先進技術和理念,推進我國制藥用水標準體系的完善。”,中國藥典緊跟相關國際法規的變化,促進先進技術的應用,有利于我國藥品走向國際市場。綜合國內外法規,制藥用水的質量控制關鍵指標為電導率、總有機碳、微生物限度和細菌內毒素(注射用水)[1][2]。
微生物限度監測項目作為制藥用水質量控制中的重要指標之一,為了得到有代表性的樣品微生物限度監測結果,從而客觀真實地反映出制藥用水系統中的水質微生物情況,取樣操作步驟是制藥用水質量監測過程中的一個關鍵環節[3]。制藥用水微生物取樣操作步驟通常會有消毒的操作,如對取樣人員手消毒和取樣口的消毒,目的是盡可能避免取樣過程對樣品帶來微生物污染[3][4]。然而由于消毒劑的主要成分為有機化合物,使得制藥用水微生物監測項目取樣的消毒操作會對 TOC 監測項目檢測結果帶來干擾,消毒劑在樣品轉運的過程中也必需做好隔離,以避免對樣品 TOC 造成干擾[3]。那么制藥用水的微生物樣品取樣不進行消毒操作是否可以接受呢?
1、制藥用水取樣步驟描述
1.1PharmaTEC制藥業:您如何定義可持續發展的生物醫藥產業生態系統?
制藥用水微生物監測項目取樣進行消毒的操作步驟,為當前制藥行業的通常做法。
1.1.1 取樣工具和樣品容器(見表1)。

表1 取樣容器
一次性乳膠手套、一次性無菌口罩、75% 酒精、一次性擦拭布、整理箱。
1.1.2 取樣順序
理化取樣 → TOC 取樣 → 微生物取樣
1.1.3 取樣操作
a)取樣前充分打開閥門,放水不少于 2 min(或不少于 20 L)。沖洗后調節閥門至適當的水流便于取樣(若適用),防止水流飛濺;
b)理化樣品取樣:容器和蓋子沖洗至少 3 次,根據實際檢測量的需要取滿一取樣瓶的水(500 mL 取樣瓶 / 袋),沖洗瓶蓋內部并蓋緊瓶蓋;
c)TOC 樣品取樣:TOC 瓶和蓋子沖洗至少 3 次,取樣量取至接近瓶口位置,旋緊瓶蓋;
d)取樣完成后,關閉閥門;
e)微生物樣品取樣:使用 75% 酒精對取樣口、雙手手套進行消毒;待消毒劑作用 1 min 后,重新充分打開閥門,放水 20~30 s ;
f)在無菌容器中裝入水樣不少于200 mL(250 mL 無菌取樣瓶 / 袋),蓋緊瓶蓋;
g)細菌內毒素樣品取樣:使用無菌無熱原管取樣至少 4 mL,蓋緊瓶蓋,豎直放置;
h)取樣結束,關上閥門。清理取樣區域;
i)操作人員必須佩戴口罩。不能觸摸蓋子里面和取樣瓶(袋)的瓶口處;
j)在無法排水的地點放置適合的接水桶;
k)使用外接軟管取水,軟管必須經過滅菌處理,并有保護性包裹。
需要注意的是,同一房間多個取樣點,先取完所有取水點的理化樣品,再消毒分別取每個點的微生物樣品,避免微生物樣品的消毒操作對 TOC 樣品造成干擾。
1.2微生物監測項目取樣不進行消毒的操作步驟
1.2.1 取樣工具和樣品容器
一次性乳膠手套、一次性無菌口罩、一次性擦拭布、整理箱。取樣容器同表1。
1.2.2 取樣順序
理化取樣 → 微生物取樣 → TOC 取樣
1.2.3 取樣操作
a)取樣前充分打開閥門,放水不少于 2 min(或不少于 20 L)。沖洗后調節閥門至適當的水流便于取樣(若適用),防止水流飛濺;
b)理化樣品取樣:容器和蓋子沖洗至少 3 次,根據實際檢測量的需要取滿一取樣瓶的水(500 mL 取樣瓶 / 袋),沖洗瓶蓋內部并蓋緊瓶蓋;
c)微生物樣品取樣:在無菌容器中裝入水樣不少于 200 mL(250 mL 無菌取樣瓶 / 袋),蓋緊瓶蓋;
d)細菌內毒素樣品取樣:使用無菌無熱原管取樣至少 4 mL,蓋緊瓶蓋,豎直放置;
e)TOC 樣品取樣:TOC 瓶和蓋子沖洗至少 3 次,取樣量取至接近瓶口位置,旋緊瓶蓋;
f)取樣完成后,關閉閥門;
g)取樣結束,關上閥門。清理取樣區域;
h)操作人員必須佩戴口罩。不能觸摸蓋子里面和取樣瓶(袋)的瓶口處;
i)在無法排水的地點放置適合的接水桶;
j)使用外接軟管取水,軟管必須經過滅菌處理,并有保護性包裹。
1.3微生物監測項目取樣消毒和不消毒的差異比較。
通過表2中的差異比較可以看出,微生物監測項目取樣消毒的目的是盡可能避免取樣口污染,以及取樣人員等對樣品帶來的微生物污染;同時消毒操作會帶來一些不利影響,其中對 TOC 監測項目帶來的影響非常麻煩;微生物監測項目取樣不進行消毒可能會引入被污染的取樣口,以及取樣人員等對樣品帶來微生物污染,但同時也有很多明顯的優勢。取樣操作帶來的污染風險,可以通過標準取樣操作規程和人員的充分培訓來進行控制,然而,微生物限度取樣不采取消毒步驟能夠客觀反映制藥用水使用狀態下的微生物狀況。

表2 微生物監測項目取樣消毒和不消毒的差異比較
2、制藥用水微生物監測項目取樣不進行消毒的項目案例
某大型制藥企業制藥用水性能確認,微生物監測項目取樣沒有進行消毒操作。該制藥用水系統的微生物限度監測數據分析如圖1 和圖2 所示。

圖1 純化水制備系統微生物限度監測結果
由圖1 和圖2 監測數據圖可知,案例中制藥用純化水制備和分配系統61個取水點,連續 28 天進行取樣測試,微生物樣品不消毒取樣的微生物限度監測數據結果良好,均符合標準限值的要求。說明在取樣標準操作規程下取樣人員規范取樣,制藥用水取樣過程中微生物限度樣品取樣不消毒操作是可以接受的。

圖2 純化水分配系統微生物限度監測結果
3、消毒和不消毒兩種方式同時進行取樣的試驗設計
3.1樣品信息
選取 1 個實驗室純化水系統的 6 個取水點,取樣點信息如表3 所示。

表3 取樣點信息
3.2檢測項目和檢測依據
檢測項目:微生物限度;
檢測依據:《中國藥典》2020 年版二部 純化水。
3.3試驗取樣操作步驟
3.3.1 取樣工具和樣品容器
一次性乳膠手套、一次性無菌口罩、75% 酒精、一次性擦拭布、整理箱。250 mL 或其他容積的無菌瓶(袋),最低取樣量 200 mL。
3.3.2 取樣操作
a)取樣前充分打開閥門,放水不少于 2 min(或不少于 20 L)。沖洗后調節閥門至適當的水流便于取樣(若適用),防止水流飛濺;
b)微生物限度樣品不消毒取樣:在無菌容器中裝入水樣不少于 200 mL(250 mL 無菌取樣瓶 / 袋),蓋緊瓶蓋;
c)取樣完成后,關閉閥門;
d)微生物限度樣品消毒取樣:使用 75% 酒精對取樣口、雙手手套進行消毒;待消毒劑作用 1 min 后,重新充分打開閥門,放水 20~30 s ;
e)在無菌容器中裝入水樣不少于200 mL(250 mL 無菌取樣瓶 / 袋),蓋緊瓶蓋;
f)取樣結束,關上閥門。清理取樣區域;
g)操作人員必須佩戴口罩。不能觸摸蓋子里面和取樣瓶(袋)的瓶口處;
h)在無法排水的地點放置適合的接水桶。
3.3.3 試驗儀器與材料,如表4 所示。
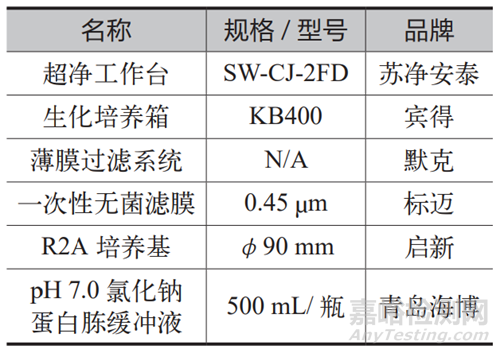
表4 試驗儀器與材料
3.3.4 試驗方法
a)組裝好微生物限度過濾系統,裝好無菌過濾杯;
b)用少量 pH 7.0 無菌氯化鈉蛋白胨緩沖液潤濕濾膜;
c)打開純化水樣品瓶,用無菌吸管吸取 10 mL 充分混勻的水樣,加入到裝好的濾杯中過濾。并用 pH 7.0 的無菌氯化鈉蛋白胨緩沖液沖洗濾膜,每張濾膜每次沖洗量為100 mL,共沖洗 1次;
d)濾盡后用無菌鑷子,取下濾膜,菌面朝上貼于 R2A 瓊脂平板上,過程中避免產生氣泡,如果有少量氣泡,用無菌鑷子輕輕按壓趕出氣泡;
e)陰性對照:方法同供試品檢測,用 100 mL pH 7.0 無菌氯化鈉蛋白胨緩沖液過濾;
f)培養:置 30~35℃生化培養箱中倒置培養不少于 5 天;
g)培養結束后,菌落計數;
h)菌落數報告原則:以 10 mL 計數結果除以 10,向上取整數報告菌數;
i)結果判定:需氧菌總數≤ 100cfu/mL。陰性對照不得有菌生長。
3.4取樣計劃
進行工作日 10 天的取樣,取樣周期 14 天。取樣計劃見表5。

表5 取樣計劃
3.5數據和結果分析
該純化水系統 6 個取樣點的微生物檢測數據見表6 和表7。

表6 微生物限度檢測結果(cfu/10 mL)

表7 微生物限度檢測結果(cfu/mL)
對兩種取樣方式樣品的微生物檢測數據結果進行數據結果比對分析。由表6、表 7 和圖3 比對檢測數據結果可知,選取 1 個實驗室純化水系統的 6 個取水點,14 天周期內進行 10 天微生物限度樣品取樣測試,每個取樣點微生物限度消毒與不消毒取樣操作各取 1 份樣品,按照《中國藥典》2020 年版 二部 純化水進行微生物限度測試,所有檢測水點兩種取樣方式樣品的微生物限度檢測結果均符合限值標準的要求,消毒與不消毒兩種取樣方式的樣品微生物限度檢測結果沒有顯著差異,結果一致。說明取樣人員在取樣標準操作規程下規范取樣,制藥用水取樣過程中微生物限度樣品取樣不消毒操作是可以接受的,能夠客觀真實地反映制藥水系統取樣點的微生物指標。
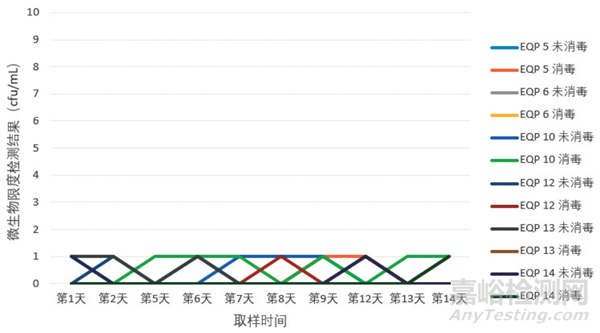
圖3 消毒和不消毒取樣的微生物限度檢測結果
4、結 論
制藥用水微生物樣品取樣消毒的主要目的是避免取樣口和取樣人員帶來的微生物污染 [3][4]。取樣口的污染與取樣點所處的環境條件,如溫度、相對濕度和空氣質量等有關[3][5]。制藥用水的取水點大部分在潔凈區,有潔凈度的控制,衛生良好。且在取樣操作時會充分放水,快速取樣,由取樣口帶來的樣品污染的風險和程度較低[4]。制藥用水取樣人員經過 GMP 和取樣標準操作規程的培訓,具備良好的操作規范意識和行為,可以控制取樣操作帶來的污染的風險和程度[4]。
USP 1231 6.1.1[2]指出,“ 至少 30 s的全開閥沖洗通常能提供足夠的剪切力來充分去除任何脆弱的生物膜結構。”ISPE 良好實踐指南,制藥用水、蒸汽和工藝氣體取樣,2016 年,2.5.1[3]指出,“任何取樣程序的目標都是獲得能準確反映系統內容物的樣品,和確保用于生產或其他指定用途的水具有合適的質量。絕大多數化學成分分布均勻,相對容易取樣,只需少量的漂洗和沖洗。由于細菌主要附著在系統的表面,因此細菌和內毒素污染物不會均勻分布,因此應執行具有代表性的采樣技術,包括沖洗”。對于微生物樣品取樣前消毒是建議,并不是必需的[3]。
ISPE 良好實踐指南,制藥用水、蒸汽和工藝氣體取樣,2016 年,2.5.8[3]指出,“抽樣技術是由抽樣目的決定的。如果取樣是為了過程控制或診斷目的,任何取樣點的污染都應該被徹底沖洗掉,這樣樣品才能準確地代表管道系統內流動的水。如果采樣是為了質量控制或滿足法規要求或共識標準,目標是采樣的方式完全復制水用于制造的方式。另外,當為質量控制目的采樣時,目標是以完全復制用于生產的水的方式進行采樣(如使用生產軟管、使用前沖洗速率和持續時間、SIP、樣品水溫)。水的取樣應盡可能靠近工藝設備。作為一般規則,為了最大限度地減少生產用水過程中的污染,建議通過出口和連接器沖洗水(如以至少每秒 8 英尺的速度或其他經過驗證的技術沖洗至少 30 s),以確保在使用前將軟管、排放管道和出口閥門的壁上的細菌沖洗干凈。沖洗的可重復性(時間和速率)應達到水質和數據一致性。除非制造用點閥門在使用 /生產前用消毒液如異丙醇噴灑,否則該閥門在取樣前不應噴灑異丙醇,沖洗時也不應如此。”
部分制藥企業在進行制藥用水微生物限度取樣操作時不采取消毒步驟。一方面是為了完全復制用于生產的水的方式進行采樣,一方面也是因為微生物限度取樣不采取消毒步驟也能夠客觀反映制藥用水的微生物指標,同時能夠避免消毒對TOC 監測結果可能造成的干擾。
比 對 試 驗 中,純化水系統的 6 個取水點,14 天周期內 10 天取樣檢測,微生物限度消毒與不消毒取樣操作的樣品微生物限度檢測結果均符合限值標準的要求,檢測結果沒有顯著差異,結果一致。
綜上所述,制藥用水微生物取樣操作步驟中的消毒操作是非必要的。可以通過科學合理的取樣標準操作規程和對人員的培訓來控制采集有代表性的樣品。
參考文獻
[1] 國家藥典委員會 . 中國藥典 2020 年版·二部 [Z],2020
[2] 美國藥典委員會 . 美國藥典 現行版本·1231[Z]
[3] ISPE 良好實踐指南,制藥用水、蒸汽和工藝氣體取樣 [Z],2016 年
[4] 凌曉敏,鐘燕飛,梁海明 . 藥品檢驗機構對純化水微生物監測的分析與探討 [J]. 藥物資訊,2020
[5] 張春紅,趙家照,王飛來,周榮兵.淺談制藥行業純化水系統微生物控制[J]. 流程工業,2022
本文作者劉曉嬋、印萍、府宇,江蘇艾蘇萊生物科技有限公司,僅供交流學習。

來源:制藥工藝與裝備


