今日頭條
來凱激活素受體II靶向抗體國內報IND。來凱醫藥1類生物藥LAE102注射液的臨床試驗申請獲CDE受理。LAE102是一款靶向激活素受體II的潛在“first-in-class”抗體藥物,其靶點對腫瘤生長、免疫激活、肌肉再生和造血發育等都有調控作用。來凱醫藥計劃在中國開展一項I/II期研究,評價LAE102的抗腫瘤活性和對于體重、肌肉量和脂肪量變化的影響。今年5月,該新藥已獲FDA臨床許可。
國內藥訊
1.神州細胞第3款新冠疫苗獲批緊急使用。神州細胞自主研發的重組新冠病毒Beta/Omicron(BA.1/BQ.1.1/XBB.1)S三聚體蛋白疫苗(SCTV01E-2)獲國家藥監局授權緊急使用。此前,神州細胞開發的重組新冠病毒2價(Alpha/Beta)S三聚體蛋白疫苗(安諾能®2)和4價(Alpha/Beta/Delta/Omicron)S三聚體蛋白疫苗(安諾能® 4)均已被國家藥監局納入緊急使用。
2.君實PD-1單抗出海澳大利亞報產。君實生物PD-1抑制劑特瑞普利單抗的上市申請獲澳大利亞藥品管理局(TGA)受理,聯合順鉑/吉西他濱一線治療轉移性或復發性局部晚期鼻咽癌成人患者,以及單藥治療復發性、不可切除或轉移性鼻咽癌經治患者。TGA同時授予特瑞普利單抗孤兒藥資格。在臨床試驗JUPITER-02中,特瑞普利單抗聯合化療使患者的疾病進展或死亡風險降低48%,死亡風險降低37%。
3.信達GLP-1R/GCGR激動劑啟動減重III期臨床。信達生物GLP-1R/GCGR激動劑瑪仕度肽(IBI362)登記啟動一項III期臨床,擬評估IBI362(9mg)用于中國肥胖受試者中減重的療效和安全性。該項試驗主要研究者為北京大學人民醫院醫學博士紀立農。Ⅱ期臨床48周治療數據顯示,瑪仕度肽(9mg)治療較安慰劑使患者體重降幅達到18.6%(減重17.8公斤);該組減重超過5%和10%的患者比例分別達到83.7%和69.8%。
4.塔吉瑞Bcr-Abl變構抑制劑擬納入突破性療法。塔吉瑞生物1類新藥TGRX-678片獲CDE擬納入突破性治療品種,用于治療經三代及以上酪氨酸激酶抑制劑(TKI)治療、加速期慢性粒細胞白血病(CML-AP)。TGRX-678是第四代TKI新藥,靶向作用于BCR-ABL融合基因的變構位點,有望解決CML患者耐藥或不耐受問題。據悉,塔吉瑞生物將于2023ASH年會公布TGRX-678兩項I期臨床研究最新結果。
5.聯拓生物收到Concentra公司并購邀約。聯拓生物宣布收到Tang Capital Partners控股的Concentra Biosciences的收購要求,該提案包括每股4.3美元現金加上一項或有價值權利(CVR)。Tang Capital Partners目前持有聯拓生物8.6%的股份。Tang Capital Partners的創始人為Kevin Tang,中文名為唐慶年,出自名門望族的無錫唐氏,父親是美籍華裔金融家唐騮千。Concentra要求聯拓生物在美國東部時間12月8日下午5點之前做出回應。
國際藥訊
1.禮來非共價BTK抑制劑獲批新適應癥。禮來非共價BTK抑制劑pirtobrutinib(Jaypirca,100mg和50mg片劑)獲FDA批準新適應癥,用于治療既往接受過至少兩種療法、慢性淋巴細胞白血病或小淋巴細胞淋巴瘤(CLL/SLL)成人患者。在I/II期BRUIN研究中,pirtobrutinib治療的總緩解率為72%。今年1月,Pirtobrutinib已獲FDA批準上市,用于治療復發或難治性套細胞淋巴瘤(MCL)。
2.K藥/ADC組合治療膀胱癌獲優先審評資格。安斯泰來/Seagen開發的Nectin-4-ADC藥物Padcev(enfortumab vedotin)與默沙東PD-1抗體Keytruda構成的組合療法獲FDA授予優先審評資格,一線治療局部晚期或轉移性尿路上皮癌(la/mUC)。PDUFA日期為明年5月9日。公布于ESMO大會上的Ⅲ期EV-302臨床數據顯示,中位隨訪為17.2個月時,與化療相比,聯合治療顯著延長患者的PFS(中位PFS:12.5個月vs6.3個月;HR=0.45,P<0.00001)和OS(中位OS:31.5個月vs16.1個月;HR=0.47,P<0.00001)。
3.NK3受體拮抗劑更年期Ⅲ期臨床成功。安斯泰來神經激肽3(NK3)受體拮抗劑Veozah(fezolinetant)治療由更年期引起的中重度血管舒縮癥狀(VMS)的Ⅲb期臨床DAYLIGHT達到主要和次要終點。與安慰劑相比,fezolinetant(45mg) 治療第24周時患者的中度至重度VMS頻率較基線顯著降低1.93(p<0.001);中重度VMS嚴重程度較基線變化顯著降低0.39(p<0.001);最常見的治療伴發不良反應(TEAE)是COVID-19感染和頭痛。詳細數據公布于ESG2023大會中。
4.雙機制肥胖癥新藥II期臨床成功。Altimmune公司GLP-1R/胰高血糖素受體雙激動劑pemvidutide治療肥胖或超重患者的Ⅱ期MOMENTUM臨床48周結果積極。與安慰劑相比,pemvidutide(1.2mg、1.8mg和2.4mg)治療組患者的平均體重減幅更大(10.3%、11.2%、和15.6%,vs2.2%),其中,2.4mg劑量組有超過50%的患者體重至少減輕15%;pemvidutide還顯著降低血脂并改善血壓;主要的不良事件為惡心和嘔吐。
5.氘代裸蓋菇素類似物抑郁癥II期臨床積極。Cybin公司氘代裸蓋菇素類似物CYB003治療重度抑郁癥(MDD)的II期臨床達到主要終點。與安慰劑相比,CYB003(12mg)治療組3周后患者的蒙哥馬利抑郁評定量表(MADRS)評分顯著改善,CYB003(12mg)組MADRS評分較基線下降14分(p=0.0005);第6周時,79%患者服用兩劑 CYB003(12mg)后抑郁癥狀緩解并且MADRS評分持續降低。臨床中未出現治療相關的嚴重不良事件。
6.艾伯維擬101億美元收購ImmunoGen。艾伯維宣布將以交易總金額高達101億美元收購ADC公司ImmunoGen,并獲得該公司FRα靶向ADC新藥Elahere、臨床早期下一代抗FRα-ADC資產IMGN-151,以及已處于Ⅱ期開發的CD123-ADC藥物Pivekimab sunirine。Elahere已于2022年獲FDA加速批準,用于治療既往接受過1-3種全身治療方案、FRα陽性、鉑類耐藥上皮性卵巢癌、輸卵管癌或原發性腹膜癌成人患者。華東醫藥擁有Elahere的中國權益。
醫藥熱點
1.贛南醫學院將更名為贛南醫科大學。贛南醫學院在贛南醫學院公眾號上宣布,經教育部黨組會議研究決定,教育部已同意贛南醫學院更名為“贛南醫科大學”。贛南醫學院前身是創辦于1941年的江西省立贛縣高級助產職業學校,1947年更名為江西省立贛縣高級醫事職業學校,1958年設置為專科建制的贛南醫學專科學校,1988年升格為本科院校并更名為贛南醫學院。
2.夏海鳴任南京鼓樓醫院黨委書記。12月1日下午,南京鼓樓醫院召開干部大會,宣布市委關于醫院黨委主要領導調整的決定,夏海鳴同志任醫院黨委書記,穆耕林同志不再擔任醫院黨委書記職務。公開資料顯示,夏海鳴,1970年6月生,醫學博士學位,曾任南京市第二醫院腫瘤科醫生、黨委書記等職。2019年1月,任南京市醫保局副局長、黨組成員;2021年8月,任南京市衛生健康委員會副主任、黨委副書記;2021年12月,任南京市衛生健康委員會主任。
3.2023年前10月基本醫保基金收入約2.6萬億元。國家醫療保障局27日發布數據顯示,2023年1至10月,基本醫療保險基金(含生育保險)總收入26187.73億元。其中,職工基本醫療保險基金(含生育保險)收入18504.19億元,城鄉居民基本醫療保險基金收入7683.55億元。基本醫療保險基金(含生育保險)總支出22531.36億元。職工基本醫療保險基金(含生育保險)支出14157.03億元,其中生育保險基金待遇支出883.93億元;城鄉居民基本醫療保險基金支出8374.33億元。
評審動態
1. CDE新藥受理情況(12月02日)
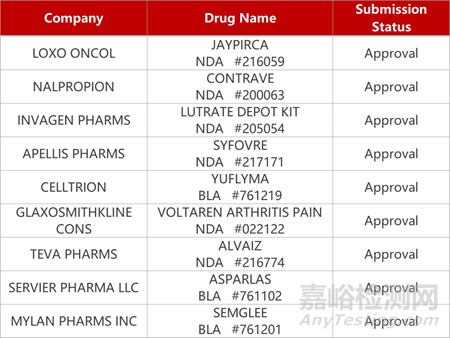
2. FDA新藥獲批情況(北美12月01日)