摘 要 / Abstract
真實世界研究是基于真實環境而非理想環境開展的科學研究。新型冠狀病毒流行期間,由于受毒株的高變異性、公共衛生政策的動態性等因素的影響,隨機對照臨床試驗難以準確及時地評估新冠病毒疫苗效果,真實世界研究受到廣泛重視。本文通過對2020年以來新冠病毒疫苗真實世界研究的系統梳理,總結不同研究類型及其設計與統計分析,比較了各種研究的優勢與劣勢,概括了新冠病毒疫苗真實世界研究面臨的挑戰和可能的解決途徑,以期為開展高質量疫苗真實世界研究提供參考。
Real world studies are scientific research conducted in real world settings rather than ideal conditions. During the COVID-19 pandemic, due to factors such as the high variability of viral strains and the dynamic nature of public health policies, randomized controlled clinical trials struggled to assess the effectiveness of COVID-19 vaccines accurately and timely.Consequently, real world studies have gained widespread attention in this context. This article provides a systematic review of real world studies on COVID-19 vaccines conducted since 2020, summarizing various study types, their designs, and statistical considerations. It compares the strengths and weaknesses of different study approaches, outlines the challenges faced by real world studies on COVID-19 vaccines, and suggests potential solutions. The aim is to provide insights for conducting highquality real world vaccine studies.
關 鍵 詞 / Key words
真實世界研究;新冠病毒疫苗;疫苗保護效果;檢測陰性設計;隊列研究;模仿目標試驗
real world study; COVID-19 vaccine; vaccine effectiveness; test-negative design; cohort study; target trial emulation
1、背 景
疫苗臨床研究與藥物臨床研究相比,在安全性和有效性臨床評價方面有所不同。(1)安全性評價:疫苗臨床研究的目標人群通常為暴露風險下的健康人群,因此對于安全性方面的考慮會更多,所需樣本量更大,以充分評估疫苗接種相關的罕見不良事件。(2)有效性評價:通常需要同時考慮免疫原性和疫苗保護效力(vaccine efficacy),并以保護效力作為評價疫苗有效性的直接證據。
隨機對照臨床試驗(randomized controlled clinical trial,RCT)普遍被認為是評價藥物有效性的“金標準”[1-4],無論是采用較為嚴格的入選或排除標準,還是基于隨機化分配治療干預,都能夠很好地減少各種偏倚(如混雜因素、信息偏倚、選擇偏倚等)和其他因素對有效性評估的影響,使得研究結論更為可靠。在疫苗的臨床研究中,這種觀念同樣被廣泛接受[5]。
然而,疫苗的RCT亦有其局限之處:(1) RCT嚴格的入選或排除標準使得臨床試驗人群不能充分代表目標人群,其研究結果對于真實世界的疫苗保護效果(vaccine effectiveness,VE)的外推性較差;(2)雖然疫苗RCT的樣本量較大,但對于在真實世界環境下發現罕見不良事件仍顯不足;(3)隨訪時間較短,所得到的有效性結論可能會受限于流行的病毒株和當前的公共衛生政策;(4)存在倫理問題,安慰劑組的受試人群仍然可能會受到傳染性疾病的影響;(5)如果進行頭對頭比較,RCT會花費高昂的時間和經濟成本[2-3]。
2019年以來新型冠狀病毒的大規模流行使上述問題更為突出[6]。新冠疫情期間,新冠病毒毒株變異所導致的流行特征變化、公共衛生政策及其變動、多種疫苗獲批上市等重要因素對疫苗保護效果產生的影響,僅靠RCT難以及時獲得不同疫苗在真實世界環境下的預估效果,從而影響公共衛生政策制定或修訂的準確性和及時性,進而影響對新冠疫情的防控效果。鑒于此,新冠病毒疫苗的真實世界研究(real world study,RWS)受到廣泛重視,并及時為公共衛生政策決策提供了依據。本文系統梳理近3年來不同新冠病毒疫苗的RWS,介紹不同研究類型及其設計與統計分析,對比各種研究設計的優勢與劣勢,以期為開展高質量疫苗RWS提供參考。
2、已發表新冠病毒疫苗RWS相關文獻分析
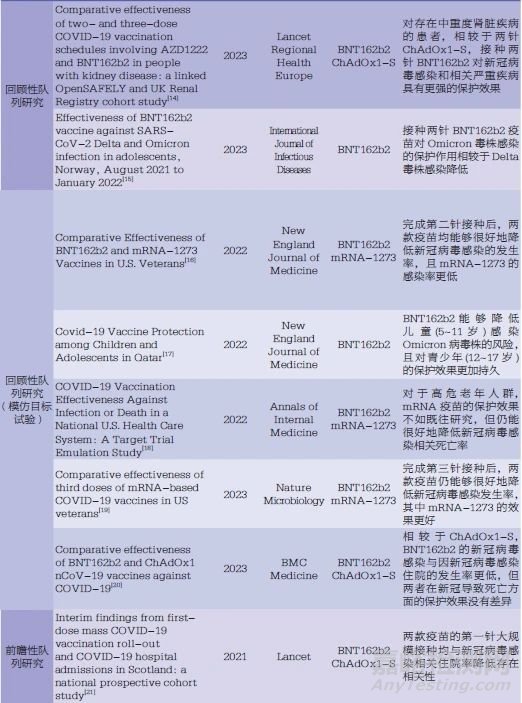
新冠病毒疫苗RWS均為觀察性研究,主要包括病例-對照研究(case-control study)、回顧性隊列研究(retrospective cohort study)和前瞻性隊列研究(prospective cohort study)。其中,病例-對照研究又以檢測陰性設計(testnegative design)為主。此外,近年來興起基于模仿目標試驗(target trial emulation)的思路設計隊列研究的研究方案,以達到模仿目標RCT,產生更加穩健的真實世界證據的目的。表1簡要匯總了近3年部分已發表新冠病毒疫苗RWS文獻的相關信息,筆者在后文針對各類研究類型的研究設計、優缺點以及分析策略進行了討論說明。
3、研究類型
(一)病例-對照研究及檢測陰性設計
1. 研究設計
病例-對照研究屬于回顧性研究,數據來源通常為現有醫療記錄和歷史數據,因此能夠以較少的時間和經濟成本得以開展。與此同時,由于采用的是既往已有數據,其質量往往較前瞻性研究所獲取的數據差。病例-對照研究通常在目標人群中先選擇病例組,然后采用匹配方法按一定比例選擇對照組,以盡可能縮小病例組與對照組在重要變量上的差異[25]。
檢測陰性設計屬于病例-對照研究,2005年首次被用于評估流感疫苗保護效果[26],并逐漸受到公共衛生領域的關注[27]。檢測陰性設計與一般的病例-對照研究設計不同之處在于,其病例組與對照組都來自于目標疾病的疑似病例(如表現出新冠病毒感染癥狀后前來醫院就診的人群),并對該人群進行檢測,根據檢測結果分配病例組與對照組,再回溯兩組人群的疫苗暴露歷史,最終得到疫苗的保護效果。
檢測陰性設計的主要優勢是可以減少目標人群異質性可能帶來的偏倚。例如,有研究者通過檢測陰性設計,對2021年4月至2022年1月的出現新冠病毒感染類似癥狀的住院患者進行檢測,根據檢測結果陽性或陰性確定病例組或對照組,進而分析新冠病毒疫苗對于Alpha、Delta和Omicron病毒株的保護效果[8]。另有研究者采用類似的設置,對2022年2月~6月期間巴西的因嚴重急性呼吸道綜合征住院的兒童進行分析,基于PCR或抗原的檢測結果劃分為病例組或對照組,發現在Omicron病毒株流行時期,即使完全接種了BNT162b2和科興的兩款疫苗,兒童的疫苗保護效果以及對危重癥的保護效果均有所降低[10]。上述兩項研究將研究對象限定為出現新冠病毒感染類似癥狀的住院患者,他們的健康尋求行為、接觸史和癥狀嚴重性等特征類似,因此可以降低產生偏倚的風險。
然而,檢測陰性設計所得到的疫苗保護效果容易受到檢測方法特異度的影響[27-28]。若檢測方法的特異度不足,假陽性病例分布在病例組的比例則會增加,進而導致疫苗保護效果被低估[29]。因此,在疫苗保護效果的評估中,檢測陰性設計通常會采用高特異度的檢測手段。同時也應注意,靈敏度不足亦會導致疫苗保護效果的估計產生偏倚[30]。
2. 統計分析
病例-對照研究,包括檢測陰性設計,多基于比值比(odds ratio,OR)評估疫苗保護效果。通常會通過Logistic回歸模型對OR進行估計,模型中會納入較為重要的協變量。求得OR后,可根據下式計算疫苗保護效果(VE)(%):
VE (%) = (1-OR) x100%
(二)回顧性與前瞻性隊列研究
1. 研究設計
根據數據來源,隊列研究可分為回顧性隊列研究、前瞻性隊列研究和回顧前瞻性隊列研究,后文主要針對前兩種類型進行討論。隊列研究根據從暴露到結局的順序產生的縱向數據進行因果推斷,故較病例-對照研究從結局到暴露的推斷更為可靠。
隊列研究設計首先根據暴露情況確定暴露組或隊列(如已接種某種疫苗的人群)和非暴露組或隊列(如未接種該疫苗的人群),并對這兩組人群進行長期隨訪觀察,直到發生感興趣的結局事件或研究結束。然后,通過比較兩組或隊列人群的結局事件發生情況,評估暴露(接種疫苗)是否與結局(感染)存在關系。
回顧性隊列研究主要具有兩個優點:(1)相較于病例-對照研究,能夠以相似的經濟與時間成本得到更強的因果關系;(2)相較于前瞻性隊列研究,能夠更好地研究特定情況下的暴露,因為可以在大量的歷史數據中找到足夠多的暴露人群,進而快速形成研究隊列[31]。
回顧性隊列研究的局限在于既往數據內容與質量不可控,如研究人群的特征無法反映真實世界的人群分布特征、關鍵的混雜因素存在遺漏情況等,從而影響研究結論的準確性、穩健性與外推性[11,32]。有研究者采用回顧性隊列研究比較了兩款獲得美國食品藥品監督管理局(FDA)批準上市的mRNA疫苗。該研究采用傾向性評分方法,分析得到這兩款疫苗預防新冠病毒感染的保護效果分別為86.1%(95%置信區間:82.4%~89.1%)和93.3%(95%置信區間:85.7%~97.4%)。然而,該研究的人口學特征與自然人群有較大差異,如研究人群的90%以上為白色人種,以及其中一款疫苗研究人群的50%年齡超過65歲等,因此該研究結論尚不足以外推至自然人群[11]。此外,在一項2023年5月的研究中,有研究者基于Open SAFELY平臺對英國國家醫療服務體系中患有慢性腎臟病的患者進行分析,以探究不同接種策略的疫苗保護效果,如兩針均為Ch Ad Ox1-S或BNT162b2,但在接種加強針時選擇另一種疫苗。盡管研究結果表明Ch Ad Ox1-S的疫苗保護效果(包括對危重癥患者的疫苗保護效果)不如BNT162b2,但研究者認為,分析數據中接種Ch Ad Ox1-S人群的特征(如年齡或疾病特征)可能難以代表真實世界中患有慢性腎臟病的人群,因此仍需要謹慎解釋兩種疫苗保護效果的差異[14]。
前瞻性隊列研究可以根據研究目的與實際情況確定數據收集方法、數據庫融合方式、研究變量和數據管理計劃等[22,33-34],因此能夠產生更高質量的觀察性研究證據。然而,高昂的經濟與時間成本、失訪、罕見結局的采集等也是研究者在設計階段需要著重考慮的問題。例如,隨著新冠病毒毒株的更替,可能較難出現Alpha病毒株的感染情況[35],如果盲目對其開展前瞻性隊列研究,則很可能無法得到感興趣的結局事件。此外,如果隨訪時間不足,研究結束時研究人群可能還未發生感興趣的結局事件(如住院或死亡),也會影響對于疫苗針對這類事件保護效果的評估[22,34]。
2. 統計分析
隊列研究主要基于相對危險度(relative risk,RR)評估暴露與結局的關系,由于研究人群的隨訪時間不一定完全一致,觀察期較長的人有更大概率發生事件。為避免由此產生偏倚,在疫苗RWS中,研究者更多會采用發生率比(incidence rate ratio,IRR)評估疫苗保護效果。
研究者一般采用Poisson回歸模型估計IRR,因為該模型在考慮發生率的基礎上,還會將每個人的觀察時間作為一個“偏移量”(offset),并將其包含在模型中進行調整,這時估計得到的是結局事件的發病速率,而不只是發病率。如果模型出現過度離散(overdispersion)的情況,即觀測到的數據的方差大于均值,則需要采用負二項回歸估計IRR。此外,Cox比例風險模型也能在考慮每個人的觀察時間的基礎上,通過估計風險比(hazard ratio,HR)評估暴露對于結局事件的影響。
對于IRR,VE(%)可通過下式計算:
VE (%)=(1-IRR) x100%
而對于HR,可以通過類似的公式計算得到相應的VE(%):
VE (%)=(1-HR) x100%
(三)模仿目標試驗
1. 研究設計
2016年有研究者提出模仿目標試驗采用RCT的視角設計觀察性研究,即基于大樣本RWD,模仿良好的目標RCT設計,繼而產生RWD的子集,進行因果推斷后得出研究結論[16,36]。該研究具體分為兩步,即制定目標RCT的研究方案和產生模仿數據及分析結果。
在制定目標RCT的研究方案方面,根據研究所需回答的臨床問題,按照RCT規范制定研究方案,即所謂的“目標試驗”,其核心要素包括但不限于:入排標準、治療策略、隨機治療分配、隨訪期限、隨訪時間點及時間窗、終點事件及其評價、統計分析計劃等。
在產生模仿數據及分析結果方面,根據RCT研究方案,在大樣本觀察性數據中抽取符合研究方案的數據構成分析數據子集,形成模仿的RCT數據,并基于該子集進行分析,產生因果推斷的研究結果。
在應用模仿目標試驗時,需要特別注意永恒時間偏倚(immortal-time bias)[36]。此類偏倚主要是由隨訪開始時間與暴露時間不統一導致。在RCT中,受試者通常會在隨機入組當天就接受研究藥物,因此不會受到此類偏倚的影響。然而在觀察性研究中,如果對研究人群采用統一的隨訪開始時間,可能存在部分研究對象的暴露時間晚于隨訪開始時間,這段時間內研究對象不會發生結局事件(若發生則不會被納入分析),因此被稱為永恒時間。若將永恒時間納入分析,很可能會使研究結論產生偏倚。例如,某研究采用觀察性數據分析新冠病毒疫苗的保護效果,并將隨訪開始時間統一設置在2022年10月1日。對于被分配至暴露組的研究對象,如果在接種疫苗前已發生新冠病毒感染,則不會被納入分析。某研究對象被納入分析,并在2022年11月1日接種第一針新冠病毒疫苗,被分配至暴露組;但是2022年10月1日至2022年11月1日期間疫苗并不會對其提供保護效果。如果僅通過結局事件(感染)與隨訪開始的發生時間間隔判斷疫苗的保護效果,將會導致錯誤地認為這1個月的“健康時間”屬于疫苗提供的保護效果,最終導致疫苗保護效果被高估(圖1)。此外,由于觀察性研究無法進行隨機化,需要基于較強且無法驗證的假設模仿隨機化過程[37],因此在模仿目標RCT時需要更加謹慎。
2. 應用實例
模仿目標試驗作為一種新方法,在新冠病毒疫苗RWS中得到了初步應用。2022年有研究者在《新英格蘭醫學雜志》上發表了模仿目標試驗的研究成果:研究者首先假想了目標試驗方案,然后基于該方案設計模仿目標試驗方案(表2),通過美國退伍軍人事務部的國家醫療保健數據庫(national health care databases of the department of veterans affair)中BNT162b2和m RNA-1273相關記錄,對兩款疫苗進行頭對頭比較,最后得到接種m RNA-1273后的感染風險比BNT162b2更低的結論[16]。此后,又有研究者于2023年基于上述同樣的研究思路,對完成上述兩款疫苗第三針加強針接種后的數據進行模仿目標試驗研究,也得到了相似結論[19]。此外,有研究者對接種了BNT162b2或m RNA-1273后存在多種高危合并疾病的老年人進行評估[18];還有研究者對接種了BNT162b2的兒童(5~11歲)和青少年(12~17歲)進行評估[17],都較好地估計了在模仿目標試驗框架下的疫苗保護效果,為評估新冠病毒疫苗在不同場景下的預防感染效果提供了新的證據。
4、挑戰與展望
新冠病毒疫苗RWS在回答真實世界環境下的新冠病毒疫苗保護效果方面起到了積極作用,為公共衛生政策決策和監管決策提供了重要依據,但同時也面臨著觀察性研究在因果推斷方面的挑戰。
由于觀察性研究具有一定的局限性,其研究結論的證據強度不及RCT。病例-對照研究(包括檢測陰性設計)是一個從結果到原因的回溯過程,且需要根據研究結局的定義選擇研究人群,因此僅能探索關聯關系,而不足以做出因果推斷。同時,雖然隊列研究比較適用于因果推斷,但回顧性隊列研究通常受限于數據質量,如果缺少某些關鍵變量,其研究結論的可靠性也會受到挑戰。前瞻性隊列研究證據強度最高,但也會受到失訪等因素的影響,尤其是對大樣本的研究人群進行長時間隨訪。因此,在設計RWS的研究方案時,務必更加謹慎,應盡可能規避觀察性研究的局限,以得到更高質量的研究結論。
即使是同類型研究,采用的評價指標、方法、納入模型的變量也不完全一致,因此研究者難以對不同研究的疫苗保護效果直接進行比較。例如,即便是針對同一類型的疫苗,有研究者基于HR評估疫苗保護效果[22],也有研究者基于IRR和HR進行評估[21]。如何看待不同真實世界場景下疫苗保護效果的差異,也是未來研究中需要正視的問題。另外,鑒于新冠病毒的高變異性,對于既往主流的新冠病毒感染臨床評價分析方法需要重新考慮,而這是否會影響目前已有的疫苗保護效果的結論,還需要進一步探索。
無論是監管部門還是學術界,都開始關注RWS與RCT的差異[38-39],包括模仿目標試驗方法。該方法可能會受到各類研究假設的影響,尤其是隨機分配的相關假設,因此需要辯證看待其結論。此外,對于疫苗RWS,如何構建真實世界環境下合理且完備的估計目標尚需深入研究。
引用本文
陳瑞,吳瑩,陳平雁*.新冠病毒疫苗真實世界研究現狀及統計學考慮[J].中國食品藥品監管,2023(10):32-41.