質(zhì)量研究的目的是通過對(duì)影響藥品質(zhì)量的各方面因素進(jìn)行研究,確定控制藥品質(zhì)量的項(xiàng)目、分析方法,并綜合藥學(xué)研究、藥理毒理和臨床研究的結(jié)果制定終產(chǎn)品的質(zhì)量標(biāo)準(zhǔn),主要關(guān)注以下幾方面:
1.手性雜質(zhì)的確定
在手性藥物質(zhì)量研究中的一個(gè)關(guān)鍵問題就是對(duì)藥物光學(xué)純度的控制。而影響藥物光學(xué)純度的手性雜質(zhì)主要來源于兩個(gè)方面:原料藥的制備工藝中引入的手性原料、手性試劑、反應(yīng)副產(chǎn)物及副反應(yīng)產(chǎn)物等工藝雜質(zhì);原料藥本身不穩(wěn)定,構(gòu)型發(fā)生翻轉(zhuǎn)而形成的立體異構(gòu)體。因此在研究之初, 就需根據(jù)原料藥的制備工藝與各手性中心的穩(wěn)定性確定需要控制的手性雜質(zhì)。在這方面存在的一個(gè)主要誤區(qū)即是:當(dāng)分子中存在多個(gè)手性中心時(shí), 不考慮制備工藝與各手性中心的穩(wěn)定性情況,不加區(qū)分地只對(duì)并不可能存在的對(duì)映異構(gòu)體雜質(zhì)進(jìn)行研究控制, 而對(duì)實(shí)際可能會(huì)存在的非對(duì)映異構(gòu)體雜質(zhì)卻毫無分析與研究。
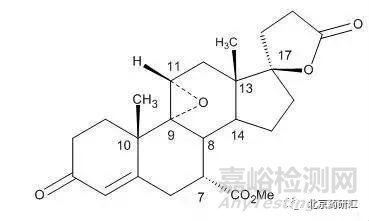
實(shí)例1:依普利酮分子中存在8個(gè)手性中心,結(jié)構(gòu)如下:
由結(jié)構(gòu)式可知:其中有些手性中心,如8、10、13位是處于甾體母核上,一般是天然形成的剛性結(jié)構(gòu),不太容易發(fā)生構(gòu)型的翻轉(zhuǎn);而有些手性中心,如7、9、11、17則大都是后續(xù)反應(yīng)中引入的,可能會(huì)產(chǎn)生相應(yīng)的立體異構(gòu)體雜質(zhì)。因此,該藥物中可能存在的立體異構(gòu)體雜質(zhì)只可能是非對(duì)映異構(gòu)體,而不可能存在對(duì)映異構(gòu)體雜質(zhì)。
2.方法的選擇及驗(yàn)證
目前常用于控制手性藥物光學(xué)純度的方法有兩種:比旋度法與手性色譜法。影響比旋度數(shù)值的因素較多, 該數(shù)值的變化并不一定能靈敏、準(zhǔn)確地反映出立體異構(gòu)體含量的變化, 當(dāng)比旋度數(shù)值較小時(shí)更是如此。例如,當(dāng)采用1 dm的旋光管, 濃度為1g·100mL-1的溶液進(jìn)行測(cè)定時(shí),假設(shè)某手性藥物僅含有一個(gè)手性中心, 該藥物的比旋度為+100o。則根據(jù)計(jì)算公式可知:當(dāng)該藥物中混有1.0%的左旋異構(gòu)體雜質(zhì)(假設(shè)其他雜質(zhì)忽略不計(jì))時(shí),此時(shí)藥物的旋光度將由+1.00o變?yōu)?0.98o而如果該手性藥物的比旋度僅為+10o, 則當(dāng)該藥物中同樣混有1.0%的左旋異構(gòu)體雜質(zhì)時(shí),此時(shí)藥物的旋光度將由+0.10o變?yōu)?0.098o, 旋光度的變化值僅為0.002o。此時(shí)如仍采用藥典附錄中提到的讀數(shù)至0.01o的旋光計(jì), 則兩者旋光度的差值超出了儀器的測(cè)量精度, 在該旋光計(jì)上將顯示相同的讀數(shù), 根本反映不出產(chǎn)品中混有1.0%的左旋異構(gòu)體雜質(zhì)。這也是為什么在制定質(zhì)量標(biāo)準(zhǔn)時(shí),當(dāng)手性藥物在不同溶劑中的比旋度相差較大時(shí), 一般選擇具有較大比旋度數(shù)值的溶劑作為標(biāo)準(zhǔn)中測(cè)定用溶劑, 以盡可能靈敏地反映手性藥物光學(xué)純度的變化情況。
實(shí)例2:甲基多巴在0.1N HCl中的比旋度為[α]25D-5.2(C=2.0), 在水中的比旋度為[ α] 20 D-14(C=1.09), 而在4.4% AlCl3水溶液中的比旋度為-25~-28。為保證該項(xiàng)目更能靈敏地反映甲基多巴光學(xué)純度的變化,在中國(guó)藥典收載的甲基多巴標(biāo)準(zhǔn)中,就采用了配置較復(fù)雜的4.4%AlCl3水溶液作為測(cè)定比旋度的溶劑, 而未采用常見的0.1N HCl或水作溶劑。
另外,當(dāng)手性藥物含有多個(gè)手性中心時(shí), 隨著立體異構(gòu)體數(shù)目的增多, 比旋度數(shù)值的變化將會(huì)受到更大的影響, 從而更加難以從比旋度的變化來獲知手性藥物光學(xué)純度的具體變化情況。
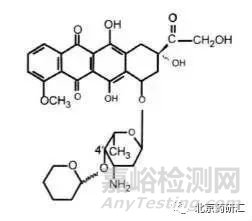
實(shí)例3:吡柔比星在4'位產(chǎn)生的2個(gè)差向異構(gòu)體在氯仿中的比旋度是相同的,均為+150(C=0.2)。此時(shí)如果僅用測(cè)定吡柔比星在氯仿中的比旋度來控制4'位差向異構(gòu)體的含量就變得毫無意義了。因?yàn)椴徽撛摬钕虍悩?gòu)體的含量如何變化,所測(cè)定的比旋度均不變。
基于以上原因,手性色譜法可以更為準(zhǔn)確直觀地反映各立體異構(gòu)體雜質(zhì)的變化情況。但是,在質(zhì)量研究中同樣需要對(duì)所采用的手性色譜法進(jìn)行充分的方法學(xué)驗(yàn)證, 以確保該方法確實(shí)能夠以足夠的靈敏度檢測(cè)到需控制的立體異構(gòu)體雜質(zhì)。為此, 在驗(yàn)證時(shí)需在以下兩方面加以注意:分析確定需控制的立體異構(gòu)體雜質(zhì);盡量采用雜質(zhì)對(duì)照品進(jìn)行專屬性和定量限的驗(yàn)證。在分析確定需控制的立體異構(gòu)體雜質(zhì)時(shí), 首先應(yīng)根據(jù)原料藥的制備工藝, 分析工藝中可能產(chǎn)生哪些立體異構(gòu)體雜質(zhì);其次, 需要設(shè)計(jì)一系列的降解試驗(yàn)來考察確定分子中各手性中心構(gòu)型的穩(wěn)定性, 以分析確定該手性藥物在哪些因素作用下可能降解產(chǎn)生哪些立體異構(gòu)體雜質(zhì)。這樣,在分析方法驗(yàn)證時(shí), 就能目的明確地考察該分析方法是否能分離并檢測(cè)出所有可能存在的立體異構(gòu)體雜質(zhì)。
實(shí)例4:恩替卡韋
抗乙肝病毒藥物恩替卡韋的合成,在引入手性中心的第1, 2, 4 步反應(yīng)中, 只要這些反應(yīng)不是采用立體專屬性的反應(yīng), 以百分之百地得到所需構(gòu)型的反應(yīng)產(chǎn)物, 且后續(xù)操作中不能有效地去除所產(chǎn)生的立體異構(gòu)體雜質(zhì), 則終產(chǎn)品中就可能混有恩替卡韋的所有其他7個(gè)立體異構(gòu)體雜質(zhì)。除非在反應(yīng)過程中已采用合適的純化手段去掉各步反應(yīng)中引入的立體異構(gòu)體雜質(zhì),并采用專屬有效的分析方法對(duì)各步反應(yīng)的中間體中的立體異構(gòu)體雜質(zhì)進(jìn)行監(jiān)控, 否則在終產(chǎn)品的質(zhì)量控制中,就應(yīng)采用合適的分析方法對(duì)這7個(gè)立體異構(gòu)體雜質(zhì)進(jìn)行控制。此時(shí)終產(chǎn)品的質(zhì)控難度是非常大的。
由此例可見,了解手性藥物的制備工藝, 并通過對(duì)引入手性中心的化學(xué)反應(yīng)的立體選擇性進(jìn)行分析, 可以全面了解工藝中可能引入的立體異構(gòu)體雜質(zhì),從而采取合適的分析手段分別在工藝過程中或終產(chǎn)品中進(jìn)行控制質(zhì)量標(biāo)準(zhǔn)的制定,在制定手性藥物的質(zhì)量標(biāo)準(zhǔn)時(shí)一定要結(jié)合手性藥物的特點(diǎn),重點(diǎn)關(guān)注能否切實(shí)控制手性藥物的光學(xué)純度。對(duì)于合成制備的手性原料藥,由于合成過程中會(huì)引入各種手性雜質(zhì),并且在放置過程中也可能會(huì)因?yàn)闃?gòu)型不穩(wěn)定而降解產(chǎn)生相應(yīng)的立體異構(gòu)體雜質(zhì),所以原料藥的質(zhì)量標(biāo)準(zhǔn)中一般均須設(shè)置專屬而靈敏的立體異構(gòu)體雜質(zhì)檢測(cè)項(xiàng)目。
對(duì)于發(fā)酵或提取制備的手性原料藥, 由于各手性中心均是天然形成的,一般都是立體專屬性的,產(chǎn)生立體異構(gòu)體雜質(zhì)的可能性不大,如果有充足的文獻(xiàn)或?qū)嶒?yàn)依據(jù)證明各手性中心在放置過程中構(gòu)型是穩(wěn)定的,則可以僅用比旋度項(xiàng)目來粗略控制該手性藥物的光學(xué)特性。
對(duì)于制劑而言:如果手性原料藥在放置過程中構(gòu)型是穩(wěn)定的, 且原料藥中所含立體異構(gòu)體雜質(zhì)不具生理活性,則制劑的質(zhì)量標(biāo)準(zhǔn)中可不納入立體異構(gòu)體雜質(zhì)控制項(xiàng)目。但是,隨著研究的深入,越來越多的已上市消旋體藥物被開發(fā)成單一的立體異構(gòu)體藥物。
實(shí)例5:在苯磺酸氨氯地平片的基礎(chǔ)上進(jìn)一步開發(fā)了苯磺酸左旋氨氯地平片。兩者的區(qū)別僅在于后者的規(guī)格較前者小一半。此時(shí)如果不根據(jù)苯磺酸左旋氨氯地平片的研究結(jié)果,在質(zhì)量標(biāo)準(zhǔn)中酌情制定立體異構(gòu)體雜質(zhì)檢查項(xiàng)或立體專屬性的鑒別項(xiàng),則在質(zhì)量標(biāo)準(zhǔn)中很難區(qū)分消旋體與左旋體片劑。因此有必要在單一的立體異構(gòu)體制劑的質(zhì)量標(biāo)準(zhǔn)中至少訂入立體專屬性的鑒別項(xiàng),以利于上市藥品的監(jiān)督管理。
3.穩(wěn)定性研究
手性藥物在一定條件下,手性中心可能會(huì)發(fā)生構(gòu)型反轉(zhuǎn),從而生產(chǎn)相應(yīng)的立體異構(gòu)體。正是由于構(gòu)型有可能發(fā)生翻轉(zhuǎn),所以在手性藥物的穩(wěn)定性研究中就應(yīng)該采取有效的分析方法監(jiān)控各手性中心構(gòu)型的穩(wěn)定性。在此需注意以下幾方面的問題:
① 如前所述, 基于比旋度法的局限性, 最好采用更為靈敏的手性色譜法來監(jiān)測(cè)各個(gè)立體異構(gòu)體的變化情況。
② 要注意考察制劑中的手性藥物構(gòu)型是否仍然穩(wěn)定, 尤其是一些液體制劑。
③ 要根據(jù)手性中心的多寡與各自的穩(wěn)定性, 選擇合適的立體異構(gòu)體進(jìn)行檢測(cè)。
實(shí)例6:在長(zhǎng)效酰胺類局麻藥--甲磺酸羅哌卡因的質(zhì)量標(biāo)準(zhǔn)中,為檢測(cè)手性HPLC法的系統(tǒng)適應(yīng)性,取甲磺酸羅哌卡因?qū)φ掌愤m量,加水制成每1mL含75μg的溶液,于90℃放置6h后,即可得到含有0.5%至1.0% R-(+)對(duì)映異構(gòu)體的對(duì)照溶液。由此可見,甲磺酸羅哌卡因分子中的手性中心在溶液中加熱即可發(fā)生構(gòu)型反轉(zhuǎn)而生成其對(duì)映異構(gòu)體。
由羅哌卡因的結(jié)構(gòu)可知,手性中心的鄰位有吸電子的羰基,從而使手性中心上的氫成為活性氫,部分活性氫原子在溶液中獲取一定的能量即可以氫離子的形式脫去,使手性中心成為平面結(jié)構(gòu)的負(fù)碳離子,根據(jù)進(jìn)攻方向立體位阻的大小,溶液中的氫離子再以一定的比例從平面的上、下兩個(gè)方向進(jìn)攻該負(fù)碳離子,從而分別得到甲磺酸羅哌卡因及少量的右旋體雜質(zhì)。
實(shí)例7:二氫膽固醇構(gòu)型的轉(zhuǎn)換
二氫膽固醇在堿的催化下, 其3位的α構(gòu)型的羥基會(huì)部分轉(zhuǎn)化為β 構(gòu)型,從而產(chǎn)生非對(duì)映異構(gòu)體。反應(yīng)示意圖見圖5。故在此情況下, 穩(wěn)定性考察時(shí)監(jiān)測(cè)的重點(diǎn)降解產(chǎn)物就應(yīng)該是非對(duì)映異構(gòu)體, 而不是對(duì)映異構(gòu)體。
此外,在考察手性藥物構(gòu)型的穩(wěn)定性時(shí), 考察條件不能局限于國(guó)內(nèi)穩(wěn)定性研究指導(dǎo)原則通常所采用的影響因素試驗(yàn)的條件。例如, 前面提到的甲磺酸羅哌卡因, 如采用一般的影響因素試驗(yàn)條件, 就可能觀察不到構(gòu)型的翻轉(zhuǎn)現(xiàn)象。
綜上所述, 在手性藥物的藥學(xué)研究中, 一定要結(jié)合手性藥物的特點(diǎn)開展相應(yīng)的研究,否則所作的研究難以真正反映手性藥物的穩(wěn)定性,也難以準(zhǔn)確控制其光學(xué)純度。另外,在具體的研究過程中,也不能拘泥于指導(dǎo)原則中的方法機(jī)械地執(zhí)行。而是要在遵循其基本原則的基礎(chǔ)上,根據(jù)具體情況靈活運(yùn)用。應(yīng)注意根據(jù)手性藥物的處方與制備拘泥工藝、手性中心的多寡與構(gòu)型的穩(wěn)定性、各立體異構(gòu)體雜質(zhì)生成的可能性與毒性等情況,采用合適的分析方法分別從起始原料、工藝過程與終產(chǎn)品的質(zhì)量標(biāo)準(zhǔn)等各個(gè)方面對(duì)手性藥物的光學(xué)純度進(jìn)行全程的監(jiān)控,以充分保證手性藥物的質(zhì)量是穩(wěn)定可控的。