常規C18色譜柱的pH耐受范圍為2-8,強酸性化合物的pKa一般小于2,強堿性化合物的pKa一般大于9,很難在常規C18上實現保留。拋開石墨碳色譜柱(pH耐受范圍0~14)、HILIC色譜柱、離子交換色譜柱不談,若要在常規C18上實現有效保留,對于強酸性化合物,可通過離子對色譜法實現保留;對于強堿性化合物,可通過離子對色譜法或離液劑實現保留。本文的目的旨在通過對兩者的保留機理進行淺析、并結合一些案例來闡明二者保留機理的異同。
圖1為RP-HPLC中離子對試劑的作用機理。首先,在流動相中添加一定量的兩親烷烴離子對試劑。若分析物為強堿性化合物(pKa一般大于9),通常會在流動相中添加烷基磺酸鹽離子對試劑,如己烷磺酸鈉、庚烷磺酸鈉、辛烷磺酸鈉等;若分析物為強酸性化合物(pKa一般小于2),通常流動相中會添加四烷基銨鹽或烷烴銨鹽離子對試劑,如四丁基溴化銨、四丁基碘化銨、四丁基氫氧化銨、己胺、辛胺等。而后,C18長鏈被流動相浸潤,經過長時間的柱平衡,流動相中離子對試劑的疏水(親脂)端,即烷基部分,與C18長鏈強力吸引;離子(親水)端,即磺酸陰離子或氮正離子則暴露于固定相與流動相的相界面上。當被分析離子化合物進入色譜柱時,強堿性化合物/強酸性化合物與相界面上的磺酸陰離子/氮正離子產生靜電作用,從而產生保留。
考慮到烷烴磺酸pKa約為1,強堿性化合物pKa約為9,為保證烷烴磺酸與強堿化合物均完全離子化,流動相的pKa應偏離二者的pKa至少2個單位,故在用離子對色譜法分析強堿性化合物時,流動相的pH應在3~7的范圍。考慮到四烷基銨鹽或烷烴銨鹽pKa約為10,強酸性化合物pKa約為2,同理可得,當在用離子對色譜法分析強酸性化合物時,流動相的pH應在4~8的范圍。如若要同時兼顧流動相的緩沖能力,可選的緩沖鹽有磷酸鹽(pKa3.2&7.2)、甲酸鹽(pKa3.8)、乙酸鹽(pKa4.7)。如若要在同一個分析方法中同時實現強酸與強堿化合物的保留時,可在流動相中同時添加烷基磺酸鹽離子對試劑以及四烷基銨鹽或烷烴銨鹽離子對試劑,同時維持流動相的pH在4~7即可。
需指出,離子對試劑中親脂的疏水端與C18長鏈的“吸附”往往是不可逆的,也就是說離子對試劑對色譜柱的改性難以避免的。“專柱專用”是避免離子對色譜法難以重現的有效辦法。
圖1 離子對試劑增加質子化堿性化合物保留因子的機理
圖2 離液陰離子增加質子化堿性化合物保留因子可能的機理
在開始闡述離液試劑的可能作用機理之前,需指明我們平常說的離液試劑一般為親脂性的無機陰離子,其僅對堿性化合物的保留有增益。根據范特霍夫(Franz Hofmeister)理論[1],離液型離子(英文名為Breaker/Chaotrope)有氯離子、硝酸根離子、三氟乙酸跟離子、四氟硼酸根離子、高氯酸根離子、六氟磷酸根離子等。上述離子離液序列依次為:氯離子<硝酸根離子<三氟乙酸跟離子<四氟硼酸根離子<高氯酸根離子<六氟磷酸根離子。隨著范特霍夫離液序列的增加,等當量的離液陰離子擾亂流動相中水-水、水-甲醇或水-四平呋喃之間氫鍵的能力增加,破壞堿性質子化分析物的溶劑化分子層的能力增強。
圖2為RP-HPLC中離液試劑的可能作用機理。使用離液劑進行堿性質子化合物分析時,首先在流動相中添加一定濃度的離液鹽試劑,常用的有三氟乙酸跟離子、四氟硼酸根離子、高氯酸根離子以及六氟磷酸根離子。隨著色譜柱的平衡,疏水C18表面會富集形成親脂的有機相層(如甲醇、乙腈、四氫呋喃)。隨后親脂的離液陰離子會在有幾層相界面富集,形成具有陽離子交換性質的“偽固定相”層。當被分析的堿性質子化合物進入色譜柱時,離液陰離子會破壞分析物的溶劑化分子層,通過靜電作用,形成“堿質子化合物-離液陰離子”中性化合物。從而產生或增強保留。
下面,將結合幾個案例來進行說明。
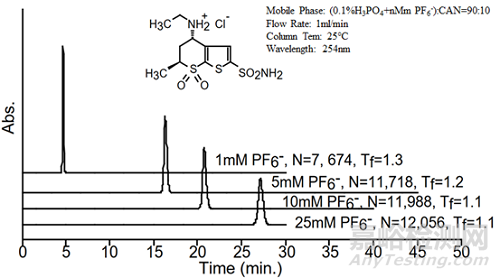
嘗試用不同摩爾濃度的六氟磷酸根進行鹽酸多佐胺的分析時[2],發現隨著六氟磷酸根濃度的增加行鹽酸多佐胺的保留時間顯著增加,且鹽酸多佐胺的對稱性及理論板數也同步增加,如圖3所示。
圖3 不同濃度六氟磷酸根對鹽酸多佐胺保留、對稱性及理論板數的影響
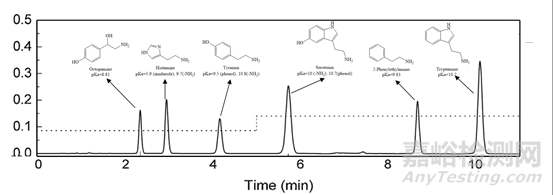
嘗試用含50mM六氟磷酸根的酸性流動相,對6種堿性毒性生物胺進行反相分離[3],六種質子化毒性生物胺均得到了有效保留,且實現了良好的RP-HPLC分離,如圖4所示。
圖4 含50mM六氟磷酸根的酸性流動相體系下,6種毒性生物胺的保留及分離情況
以上,筆者根據相關文獻及個人見解,分析了離子對試劑與離液劑試劑在作為添加劑時對化合物保留的機制。根據相關案例,可以得出相較與離子對試劑,離液劑的添加不會造成色譜柱的改性。隨著離液劑濃度的增加,目標堿性質子化合物的保留隨之增加,但需指出當離液劑達到一個臨界濃度時,對于保留因子k不會再有增益。此外,離液劑可以讓極弱疏水性堿性質子化合物在常規C18上產生保留,如案例2所示(Histamine: LogD(pH5.5) = -4.20,2-Phenylethylamine: LogD(pH5.5) = -1.52, Tyramine: LogD(pH5.5)=-2.5, Octopamine: LogD(pH5.5) = -3.45, Tryptamine: ACD/LogD(pH5.5) = -1.42,Serotonin: LogD(pH5.5) = -2.49)。個人看法,若有紕漏之處,望同行指正。
參考文獻
[1] Cecchi T, Passamonti P. Retention mechanism for ion-pair chromatography with chaotropic reagents. J Chromatogr A 2009; 1216:1789-97
[2] Li Pana, Rosario LoBruttoa. ThompsonIn?uence of inorganic mobile phase additives on the retention, ef?ciency and peak symmetry of protonated basic compounds in reversed-phase liquid chromatography. Journal of Chromatography A, 1049 (2004) 63–73
[3] JianJun Zhong, Ningbo Liao. Liquid chromatographic method for toxic biogenic amines in foods using a chaotropic salt. Journal of Chromatography A, 1406 (2015) 331–336。