今日頭條
歌禮PD-L1單抗艾滋病Ⅱ期臨床積極。歌禮皮下注射PD-L1抗體恩沃利單抗(ASC22)聯合西達本胺用于人類免疫缺陷病毒(HIV)感染的Ⅱ期臨床結果積極。第8周和第12周時,ASC22聯合治療顯著提高受試者細胞相關HIV RNA較基線變化,平均增幅分別為4.27倍和3.41倍;HIV細胞相關RNA與總DNA的比值也呈現改善趨勢。藥物總體耐受性良好。詳細結果公布于第12屆國際艾滋病協會HIV科學會議上。
國內藥訊
1.諾和諾德長效凝血素中國報產。諾和諾德長效凝血因子VIII注射用培圖羅凝血素α(turoctocog alfa pegol,N8-GP)的上市申請獲CDE受理。N8-GP是一款經聚乙二醇(PEG)修飾后半衰期得到顯著延長的凝血因子,與非修飾FVIII產品相比,N8-GP在成人/青少年中半衰期延長了1.6倍,在兒童中半衰期延長了1.9倍。在美國,該新藥已獲批用于成人和兒童血友病A患者的預防性治療和急性治療。
2.恒瑞PD-1單抗肝癌Ⅲ期臨床見刊柳葉刀。恒瑞醫藥PD-1抑制劑卡瑞利珠單抗聯合VEGFR2抑制劑甲磺酸阿帕替尼一線治療不可切除肝細胞癌的國際Ⅲ期CARES-310(SHR-1210-310)研究發表于《柳葉刀》。與sorafenib相比,卡瑞利珠單抗組合中位無進展生存期(mPFS)顯著改善(5.6個月vs3.7個月);兩組中位總生存期(mOS)分別為22.1個月和15.2個月。試驗中最常見的3級或4級治療相關不良事件是高血壓、手掌-足底紅血病綜合征、天冬氨酸轉氨酶升高和丙氨酸轉氨酶升高。
3.科笛「米諾環素泡沫劑」擬納入優先審評。科笛生物從Foamix公司引進的外用4%米諾環素泡沫劑(CU-10201)獲CDE擬納入優先審評,用于9歲及以上兒童和成人患者的非結節性中重度尋常痤瘡炎癥性病變的局部治療。米諾環素是一種用于治療細菌感染及尋常痤瘡的四環素抗生素,它通過阻止胺基酸進入核糖體,從而抑制細菌肽鏈的形成。科笛生物擁有CU-10201在大中華區的權益。
4.信念血友病A基因療法獲批臨床。信念醫藥旗下上海信致的AAV基因治療藥物“BBM-H803注射液”獲國家藥監局臨床許可,擬用于治療血友病A。BBM-H803旨在通過靜脈給藥將人凝血因子Ⅷ(Factor Ⅷ,FⅧ)基因導入血友病A患者體內,從而提高并長期維持患者體內凝血因子水平,以期達到“一次治療、長期有效”的治療及預防出血效果。在美國,FDA已授予該基因療法治療血友病A的孤兒藥資格。
5.阿斯利康ASO新藥中國獲批臨床。阿斯利康反義寡核苷酸(ASO)療法eplontersen注射液獲國家藥監局臨床許可,擬用于治療遺傳型和野生型轉甲狀腺素蛋白淀粉樣變性心肌病(ATTR-CM)成人患者,以減少心血管死亡和心血管相關住院。它被設計為一月一次,可由患者自己皮下注射,通過抑制TTR蛋白的生產,從而治療淀粉樣變性多發性神經病。目前,eplontersen治療淀粉樣蛋白TTR多發性神經病(ATTR-PN)的新藥申請在接受FDA審評。
國際藥訊
1.輝瑞GBS母體疫苗Ⅱ期臨床積極。輝瑞開發的由六價莢膜多糖(CPS)與基因解毒白喉毒素交叉反應物質(CRM)偶聯產生的B組鏈球菌(GBS)候選母體疫苗GBS6,在用于給母親接種以保護嬰兒免受侵襲性GBS疾病的Ⅱ期臨床獲積極結果。數據顯示,母親接種疫苗后所生嬰兒體內的抗CPS IgG濃度>0.184 µg/mL。免疫原性最強的制劑達到57%-97%的血清應答率。在母親和嬰兒中,疫苗組和安慰劑組的安全性特征相似。詳細結果發表在《新英格蘭醫學雜志》上。
2.創新RNAi療法高血壓早期臨床見刊NEJM。Alnylam公司靶向血管緊張素原(AGT)的RNAi(RNA interference)療法zilebesiran用于治療輕度至中度高血壓患者的Ⅰ期臨床積極結果發表在NEJM上。與安慰劑相比,zilebesiran劑量依賴性地降低血清AGT水平,且持續長達6個月;兩組不良事件(AE)的發生頻率分別為72%和88%。羅氏已以28億美元與Alnylam達成合作,聯合開發zilebesiran用于治療高血壓。
3.多特異性NK細胞接合器上臨床。Innate Pharma SA公司宣布,由賽諾菲資助的一項驗證多特異性NK細胞接合器SAR’514 / IPH6401用于復發/難治性多發性骨髓瘤(R/R MM)的Ⅰ/Ⅱ臨床 (NCT05839626)完成首例患者給藥。SAR’514/ IPH6401是一種以NKp46/CD16為基礎,靶向BCMA的NK細胞接合器,它還能同時結合兩種激活受體NKp46和CD16,充分利用NK細胞效應器功能的優勢來對抗癌細胞。該項目的推進將激活兩家公司于2016年簽署的相關合作條款。
4.安斯泰來布局新型蛋白降解劑。安斯泰來與日本PeptiDream公司將利用后者專有的PDPS(多肽發現平臺系統)技術,為安斯泰來選定的兩個靶點,合作開發新型蛋白質降解劑。根據協議,PeptiDream公司將獲得30億日元的預付款,發現、開發和商業銷售里程碑后期付款(每個目標最高可達206億日元),以及產品的銷售分成。安斯泰來還有權選擇另外三個靶點納入合作范圍。
5.Kodiak終止抗VEGF眼科新藥開發。Kodiak Sciences公司公布VEGF靶向抗體偶聯生物聚合物(ABC)tarcocimab tedromer(KSI-301)用于治療視網膜血管疾病的3項III期研究(DAYLIGHT、GLEAM和GLIMMER)的頂線結果。在DAYLIGHT研究中,與阿柏西普相比,KSI-301治療顯著改善濕性年齡相關性黃斑變性(AMD)患者的最佳矯正視力(BCVA)評分;且KSI-301總體耐受性良好。在KSI-301對比阿柏西普一線治療糖尿病性黃斑水腫(DME)患者的GLEAM和GLIMMER研究中,2項研究沒有達到主要終點,而且在KSI-301治療組中觀察到白內障發病率增加。Kodiak決定終止該藥物的臨床開發計劃。
6.KRAS抑制劑NSCLC適應癥未獲CHMP支持。歐洲藥品管理局(EMA)人用藥品委員會(CHMP)不支持Mirati公司口服KRAS G12C抑制劑Krazati(adagrasib)用于治療KRAS G12C突變晚期非小細胞肺癌 (NSCLC)的有條件上市申請。在注冊性KRYSTAL-1研究中,Adagrasib達到43%的客觀緩解率(ORR)和80%的疾病控制率(DCR)。基于該結果,FDA已于去年年底加速批準Krazati上市,用于治療攜帶KRAS G12C突變的NSCLC患者。
醫藥熱點
1.南京大學再添一家附屬醫院。7月22日,南京大學醫學院附屬蘇州醫院簽約揭牌。南京大學醫學院附屬蘇州醫院由蘇州高新區管委會與南京大學醫學院附屬鼓樓醫院合作共建,依托蘇州科技城醫院良好基礎,采用鼓樓醫院托管的模式,加快打造高水平醫院。此前,南京大學醫學院已有5所附屬醫院:附屬鼓樓醫院、附屬金陵醫院(東部戰區總醫院)、附屬口腔醫院、附屬泰康仙林鼓樓醫院和附屬鹽城第一醫院(鹽城市第一人民醫院)。
2.廣中醫一附院白云醫院啟動擴建項目。7月21日,廣州白云區啟動廣中醫一附院白云醫院擴建項目。廣中醫一附院白云醫院擴建項目計劃投入14億元全面升級改造白云醫院門急診醫技綜合樓、發熱門診樓、應急救治綜合樓等,項目預計2026年正式投入使用,建成后床位數將增至1000張以上,占地面積達87畝,成為白云北部最具規模的三級中醫醫院,進一步實現中醫藥服務質的提升。
3.全球男性美容市場規模高達800億美元。據德國斯塔蒂斯塔調查公司最新統計,2022年全球男性美容市場規模達到800億美元,有望在2028年達到1150億美元。男性美容業風靡全球的背后,是傳統觀念轉變、護膚品牌助推,以及社交媒體影響多重因素作用的結果。相關數據顯示,短視頻平臺TikTok上有關“男性護膚”等關鍵詞的短視頻瀏覽量年增長率為389%,和“男性美容”相關的短視頻瀏覽次數高達19億。
評審動態
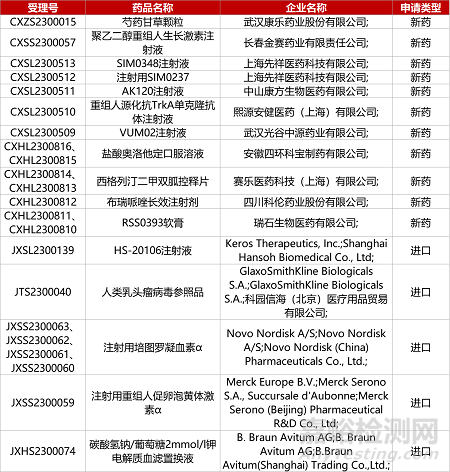
1. CDE新藥受理情況(07月25日)
2. FDA新藥獲批情況(北美07月24日)