本通則與《歐洲藥典》和/或《日本藥典》的相應文本相一致�。這些藥典承諾不對本統一章節進行任何單方面更改���。
本通用章文本中屬于USP國家文本的部分����,因此不是協調組織文本的一部分��,用符號(◆ ◆)來說明這一事實�。
本試驗旨在確定是否符合溶出度要求◆ 個別專論中所述◆ 用于口服給藥的劑型�。在本通用章中,劑量單位定義為1片或1?���;蛑付ǖ牧?��?��!粼诒疚乃龅钠餍翟O計類型中����,請使用單獨專論中指定的器械設計。如果標簽上注明某物品是腸溶的�����,而溶出或崩解試驗沒有明確說明它將用于緩釋物品�,并且包含在各論中,則適用緩釋劑型的程序和解釋�����,除非在各論中另有規定�����。◆
◆用于含有明膠或涂有明膠的劑型
如果含有明膠的劑型由于存在交聯的證據而不符合相應驗收表中的標準(見釋義�����、速釋制劑�����、緩釋制劑或延釋制劑)�,則應按照下文所述����,在介質中加入酶,重復溶出過程���,并從相應驗收表的第一階段開始評估溶出結果。如果在第一階段的測試中沒有達到標準���,并且觀察到交聯的證據,則沒有必要繼續測試到最后階段(最多24個單位)�����。
明膠在某些化合物存在和/或在某些儲存條件下��,包括但不限于高濕度和高溫度���,可能存在交聯��。明膠膠囊外殼的外表面和/或內表面或劑型上可能會形成薄膜,以防止藥物在溶出度測試過程中釋放(更多信息請參閱《膠囊-溶出度檢測和相關質量屬性》〈1094〉)�。
[注意:所有對〈1000〉以上章節的引用僅用于提供信息��,并作為一種有用的資源使用。這些章節并不是強制性的,除非明確要求用于此用途�。]
pH≤4.0的溶出介質
酶:胃蛋白酶,通過試劑規格部分中純化胃蛋白酶的程序確定的活性��。
用量:胃蛋白酶的量�,其活性不超過750000單位/L的溶出介質。
pH>4.0和<6.8的溶出介質
酶:木瓜蛋白酶���,通過木瓜蛋白酶專論中的含量測定試驗測定其活性;或菠蘿蛋白酶����,通過試劑規格章節中菠蘿蛋白酶的程序確定其活性�。
用量:木瓜蛋白酶的活性不超過550,000單位/升溶出介質的數量�����,或菠蘿蛋白酶的活性不超過30明膠消化單位(GDU)/升溶出介質的數量�。
pH≥6.8的溶出介質
酶:胰蛋白酶�����,蛋白酶活性通過胰蛋白酶專論中蛋白酶活性(酶蛋白消化能力)測定程序測定���。
用量:使蛋白酶活性不超過2000單位/L溶出介質的胰酶數量�。
含有表面活性劑或已知能使酶變性的其他成分的溶出介質
如果溶出介質含有表面活性劑或已知能使所用酶變性的其他成分�,則可以在劑型的溶解測試中進行預處理步驟。該預處理步驟使用不含表面活性劑或成分的特定溶出介質,并根據介質pH添加適量的酶�。添加的酶的量與預處理中使用的溶出介質的體積相適應���。為了達到用于最終溶解測試的指定介質體積��,可以用較小體積的不含成分的介質進行預處理步驟��,這樣在預處理步驟結束時加入成分就可以得到最終體積。試驗的所有其他條件(儀器、旋轉或流速)應保持如方法或專論中所述�。通常��,預處理步驟的持續時間不超過15分鐘。所需的預處理時間應根據具體情況進行評估,并應具有科學依據����。該時間應包含在測試的總時間中。例如��,如果測試的總時間為45分鐘���,并且在預處理步驟中使用了15分鐘��,則在添加成分后��,測試將繼續30分鐘。◆
更改為:
儀器
第1法(籃法)
組件由以下部分組成:有蓋或無蓋的溶出杯��,由玻璃或其他惰性透明材料1制成�;電動機;轉軸;轉籃。溶出杯部分浸沒在合適大小的水浴中,或通過合適的裝置(例如加熱套)加熱。水浴或加熱裝置允許在試驗期間將容器內的溫度保持在37±0.5°���,并且容許杯內液體保持恒定、平穩的運動��。整個儀器包括放置的環境���,除了平穩轉動的攪拌部件��,不得有明顯的運動�、攪拌或振動�。儀器最好能允許在檢測過程中能夠觀察到檢品和攪拌部件。溶出杯為圓柱形�����,底部為半球形◆具有以下尺寸和容量:◆ 容量為1L�����,高度為160–210 mm�,內徑為98–106 mm����;對于2L的容量���,高度為280–300 mm�,內徑為98–106 mm;和◆ 對于4 L的容量�,高度為280–300 mm���,內徑為145–155 mm◆. 它的側面在頂部有凸緣���。安裝好的蓋子可以用來延緩蒸發�。轉軸與溶出杯的垂直軸線在任何點處都不相差超過2 mm��,并且轉動平穩����,不會出現可能影響結果的明顯擺動�����。使用調速裝置�,可選擇軸轉速并將其保持在規定的轉速上◆ 在個別專論中給出◆ 的±4%范圍以內����。
轉軸和轉籃部件由316型不銹鋼或其他惰性材料制成,規格如圖1所示�?����?梢允褂镁哂屑s0.0001英寸(2.5µm)厚的鍍金籃子。在每次測試開始時,將一劑藥品放置在干燥的籃子中�����。試驗期間���,溶出杯底部和籃子底部之間的距離保持在25±2 mm�。



圖1.轉籃組成
第2法(槳法)
除了使用由葉片和軸形成的槳葉作為攪拌元件外,使用裝置1的組件���。軸的位置應確保其軸線在任何點與溶出杯垂直軸線的距離不超過2 mm,并且旋轉平穩�����,不會出現可能影響結果的明顯擺動�。葉片的垂直中心線穿過軸的軸線,使得葉片的底部與軸的底部齊平���。槳葉符合圖2所示的規格。試驗期間����,葉片底部和溶出杯底部之間的距離保持在25±2 mm��。金屬或適當惰性的剛性葉片和軸組成一個整體。可以使用合適的兩部分可拆卸設計�,前提是組件在測試過程中保持牢固接合����。槳葉和軸可以涂上合適的涂層�,以使兩者都是惰性的。在葉片開始旋轉之前,允許一劑藥品下沉到容器底部。一小塊松散的非反應性材料����,例如不超過幾圈的螺旋線�,可以連接到本來會漂浮的一劑藥品上���。另一種下沉裝置如圖2a所示����。也可以使用其他經過驗證的沉降片裝置���。
圖2.攪拌槳組成


圖2a.可選的沉降籃�����。所有尺寸均以毫米表示

◆沉降藍的另一種選擇是吊籃���。藥品被放置在一個由不銹鋼絲網制成的四邊形籃子中��,焊接在其上窄邊之一,并連接到不銹鋼連桿的末端(見圖2b)����。蓋子放置在籃子的水平對角線上����。桿組件通過可調節螺紋鋼桿連接到溶解容器的蓋子上�,并通過兩個聚四氟乙烯螺母固定,距離容器中心約3.2厘米����,或通過其他適當的方式固定����。將吊籃底部的下角調整到槳葉頂部上方約1cm處(見圖2c)����。連接桿的軸線沿著連接桿的垂直長度平行于槳軸的軸線,并且吊籃的最大面位于垂直于溶出杯圓柱體半徑的垂直平面內。
圖2b.固定吊籃
圖2c.溶出杯中吊籃的位置
第3法(往復筒法)3
該組件包括一組圓柱形平底玻璃容器�;一組玻璃往復缸�����;惰性配件(316型不銹鋼或其他合適的材料)����,以及由合適的非吸收性和非反應材料制成并設計成適合往復缸的頂部和底部的篩網��;以及馬達和驅動組件,使缸體在容器內垂直往復運動���;如果需要,將往復缸水平地分度到另一排容器上���。將容器部分浸入任何方便尺寸的合適水浴中,以便在試驗期間將溫度保持在37±0.5°��。儀器的任何部分�,包括儀器放置的環境,都不能產生顯著的運動��、攪動或振動�����,而這些運動����、攪動和振動是由于光滑的垂直往復氣缸造成的���。使用一種裝置����,允許選擇往復率并將其保持在個別專著中規定的浸透率◆的±5%范圍內。最好使用能夠觀察試樣和往復式圓筒的設備���。容器配備有蒸發帽����,在試驗期間保持在原位。除非另有規定�,否則部件應符合圖3所示的尺寸◆在個別專論中◆����。
圖3.第3法(往復筒法)設備.(所有測量值均以毫米為單位����,除非另有說明。)
第4法(流通池)
該組件包含一個用于溶出介質的儲液器和相應的泵�����;流通池和將溶出介質保持在37±0.5°的水浴����。使用◆如個別專論所述◆中規定的尺寸。
泵推動溶出介質向上通過流通池。該泵的輸送范圍在240至960毫升/小時之間,標準流速為4、8和16毫升/分鐘。泵必須提供恒定的流量(額定流量的±5%以內);流量分布為正弦曲線���,脈動為120±10脈沖/min。也可以使用無脈沖的泵��。使用流通池的溶出試驗程序必須在速率和任何脈動方面進行表征����。
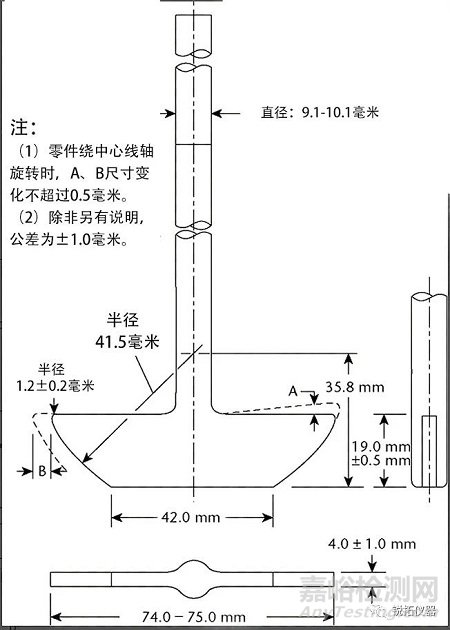
由透明和惰性材料制成的流通池(見圖4和圖5)垂直安裝有過濾系統(在個別專論中有規定),防止未溶解的顆粒從池頂部逸出�;標準流通池直徑分別為12毫米和22.6毫米��;底部錐體通常填充有直徑約為1mm的小玻璃珠,其中一個約為5mm的玻璃珠位于頂部以保護液體進入管�����;片劑支架(見圖4和圖5)可用于特殊劑型的定位�����,例如泡騰片。將流通池浸入溫度保持在37±0.5°的水浴中。
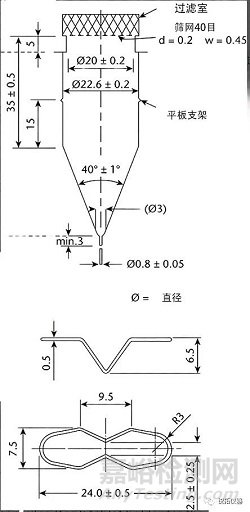
圖4.第4法設備:用于片劑和膠囊的大流通池(上);大流通池的片劑支架(下)��。(除非另有說明����,否則所有測量值均以毫米為單位�����。)
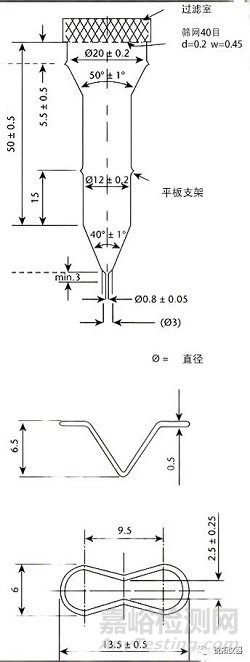
圖5.第4法設備:片劑和膠囊的小流通池(上);小流通池的藥片支架(下)。(除非另有說明,否則所有測量值均以毫米為單位�。)
該裝置使用一個夾緊機構和兩個O形環來組裝測試池����。泵與溶出單元分開�����,以保護溶出單元免受來自泵的任何振動的影響��。泵的水平位置不應高于溶出介質容器。管線連接應盡可能短����。使用適當的惰性管道�,如聚四氟乙烯�����,內徑約為1.6毫米�,用具有化學惰性的法蘭盤連接��。
設備適用性
確定設備是否適合進行溶出度測試必須包括是否符合上述儀器的尺寸和公差。此外����,在使用過程中必須定期監測的關鍵測試參數包括溶出介質的體積和溫度��、轉速(第1法和第2法)、浸沒頻率(第3法)和介質的流速(第4法)�。
定期確定溶出試驗設備的性能�?���!粜阅茯炞C試驗證明了單個設備的適用性。
?美國藥典參考標準〈11〉:
美國藥典潑尼松片RS▲, USP溶出性能驗證標準潑尼松RS▲ (IRA 2022年1月1日)
性能驗證試驗�����,裝置1和裝置2:試驗USP潑尼松片RS▲或USP溶出性能驗證標準潑尼松RS▲ (IRA 1-Sep-2022)根據規定的操作條件���。如果獲得的結果在所用批次和測試設備的技術數據表中規定的可接受范圍內�����,則該設備是合適的��。
性能驗證測試,裝置3:[即將推出]
性能驗證測試�,裝置4:[即將推出]◆
程序
第1法和第2法
速釋制劑
將◆在個別專論中給出◆ 的溶出介質(±1%)放入指定儀器的容器中, 組裝儀器��,將溶出介質平衡到37±0.5°,然后取下溫度計�。在儀器中放置1個單位劑量的藥品���,注意避免表面產生氣泡��,并立即以◆在個別專論中規定◆的速率操作儀器. 在規定的時間間隔內,或在規定的每個時間��,從溶出介質表面以下的旋轉籃或葉片頂部之間的中間區域取出樣品����,且距離容器壁不小于1cm����。
[注:如果規定了多次取樣時間,則將取出進行分析的等分試樣更換為37°下等體積的新鮮溶出介質��,或者��,如果可以證明不需要更換介質�����,則校正計算中的體積變化。在試驗期間�,將容器蓋上���,并在適當的時間驗證試驗混合物的溫度]
進行◆如個別專著中所述◆分析使用合適的測定方法�。4使用額外的劑型單位重新進行試驗。
如果使用自動化設備進行采樣或對儀器進行其他修改�����,則有必要驗證修改后的儀器將產生與本通用章所述標準儀器相同的結果��。
溶出介質:使用合適的溶出介質����。使用◆ 在個別專論中◆指定的溶劑��。指定的體積是指在20°到25°之間進行的測量�����。如果溶出介質是緩沖溶液����,則調整溶液,使其pH值在◆在各論中給出◆ 規定pH值的0.05以內。[注意:溶解氣體會導致氣泡形成�,這可能會改變測試結果�。如果溶解氣體影響溶出結果����,則應在測試前清除溶解氣體。5]
時間:在給出了單一的時間規定的情況下��,如果滿足最低溶解量的要求�����,則可以在更短的時間內完成測試�����。只能在規定的時間內,在±2%的時間誤差范圍內取出試樣����。
◆速釋劑型的合并樣品的程序:如果各論中規定了合并樣品的步驟�����,則使用該程序。按照程序部分第1法和第2法中的速釋制劑的指示進行操作���。將取出的6個或12個單獨樣本的等體積過濾溶液合并,并將合并的樣本用作試樣。測定合并樣品中的活性成分的平均溶出量���?�!?/span>
緩釋制劑
按照速釋制劑的方法進行操作���。
溶出介質:按照速釋制劑的方法進行制備����。
時間:測試時間點�,通常為三個,以小時為單位。
遲釋制劑3
使用方法A程序或方法B程序以及◆個別專論中◆規定的儀器。除另有規定外所有試驗時間與規定時間相差不超過±2%。
方法A程序◆(除非個別專論另有規定)◆
?酸階段
在容器中放入750 mL 0.1 N鹽酸���,然后組裝儀器。使介質平衡到37±0.5°。在儀器中放置1劑量單位的藥品�,蓋上容器��,并以◆個論中規定◆的速率操作儀器。
在0.1N鹽酸中攪拌2小時后,提取液體的等分試樣���,并按照緩沖液階段的說明繼續操作。
使用合適的分析方法對等分試樣進行分析?��!粼摲椒ㄔ诟髡撝杏性敿氄f明。◆
?緩沖液階段
[注:在5分鐘內完成添加緩沖液和調節pH的操作。]儀器以◆在個論中◆規定的速率運行, 向容器中的液體中加入250 mL已平衡至37±0.5°的0.20 M磷酸鈉�����。如有必要,用2 N鹽酸或2 N氫氧化鈉將pH調節至6.8±0.05。繼續操作設備45分鐘或◆ 在個別專論中給出◆指定時間。在該時間段結束時���,取出一份試樣溶液,并使用合適的分析方法進行分析?��!粼摮绦蛟诟髡撝杏性敿氄f明。如果在較早的時間滿足最低溶出量的要求,則試驗可以在比緩沖液階段規定的更短的時間內結束��?���!?/span>
方法B程序◆ (除非個別專論另有說明)◆
?酸性階段
在容器中放入1000 mL 0.1 N鹽酸��,然后組裝儀器��。使介質平衡至37±0.5°的溫度。在儀器中放置1劑量單位藥品�����,蓋上容器����,并以◆ 在專著中◆ 規定的速率操作儀器。在0.1N鹽酸中操作2小時后�����,提取液體的等分試樣����,并按照緩沖液階段的說明繼續進行。
使用合適的分析方法對等分試樣進行分析����?�!粼摲椒ㄔ诟髡撝杏性敿氄f明?!?/span>
?緩沖液階段
[注:在此階段����,使用之前已平衡到37±0.5°溫度的緩沖液�。]從容器中排出酸,并向容器中加入1000mL pH 6.8磷酸鹽緩沖液���,該緩沖液是通過將0.1N鹽酸與0.20M磷酸鈉(3:1)混合制備的,如有必要����,用2 N鹽酸或2 N氫氧化鈉將pH調節至6.8±0.05。[注:這也可以通過從設備中移除含有酸的容器�,然后用另一個含有緩沖液的容器替換����,并將藥品轉移到含有緩沖液的容器中����。]
繼續操作設備45分鐘或◆ 在個別專論中給出◆指定時間。在該時間段結束時���,取出等分的試樣,并使用合適的分析方法進行分析�����?���!粼摮绦蛟诟髡撝杏性敿氄f明。如果在較早的時間滿足最低溶解量的要求�����,則試驗可以在比緩沖階段規定的更短的時間內結束��?����!?/span>
第3法(往復桶法)
速釋制劑3
在儀器的每個容器中放入規定體積的溶出介質���,組裝儀器,將溶出介質平衡至37±0.5°�,然后取下溫度計����。在六個往復圓筒中的每個圓筒中放置一劑量藥品,注意將氣泡從每個藥品的表面排除�����,并立即按照◆在個別專論中◆ 的規定操作設備。在向上和向下的沖程中�����,往復式圓筒移動了9.9–10.1cm的總距離����。在規定的時間間隔內,或在規定的每個時間�����,升起往復式圓筒��,并從溶出介質液面至每個容器底部的中間區域提取一部分待測溶液���。按照◆ 在個別專論中◆的規定進行分析����。如有必要�����,使用更多的劑型單位重復測試���。
溶出介質:按照第1法和第2法中速釋制劑的說明進行制備���。
時間:按照第1法和第2法中速釋制劑的說明進行。
緩釋劑型
按照第3法中速釋制劑的說明進行操作。
溶出介質:按照第1法和第2法中緩釋劑型的說明進行制備。
時間:按照第1法和第2法中緩釋劑型的說明進行。
遲釋制劑
按照第1法和第2法中遲釋制劑方法B程序的說明進行操作�����,使用一排容器用于酸性階段介質��,下一排容器用作緩沖液階段����,并使用規定體積的介質(通常為300 mL)�����。
時間:按照第1法和第2法中速釋制劑的說明進行�。
第4法(流通池)
速釋制劑
根據◆在專著中◆的規定將玻璃珠放入流通池�。將1單位劑量藥品放在珠子上,或者�,如果◆ 在專著中◆另有規定, 也可置于載具上����。組裝過濾頭����,并使用合適的夾緊裝置將零件固定在一起。用泵將加熱至37±0.5°的溶出介質引入流通池�,以獲得◆ 在個別專論中◆ 規定的流速并且流速精度為5%���。在每個規定的時間收集浸出液��。按照◆ 在個別專論中◆規定進行分析。使用額外的劑型單位重復測試。
溶出介質:按照第1法和第2法中的速釋制劑的說明進行制備�。
時間:按照第1法和第2法中的速釋制劑的說明進行����。
緩釋劑型
按照第4法中速釋制劑型的說明進行操作����。
溶出介質:按照第4法中速釋制劑的說明進行制備。
時間:按照第4法中速釋制劑的說明進行操作�。
遲釋制劑
按照第1法和第2法中遲釋制劑的說明���,使用指定的介質進行操作�。
時間:按照第1法和第2法中遲釋制劑的說明進行操作����。
解釋
速釋制劑
除非◆在個別專論中◆另有規定,如果從測試的劑量單位中溶出的活性成分的量符合驗收表1,則滿足要求���。繼續進行三個階段測試,除非結果符合S1或S2���。數量(Q)指◆在個別專論中規定◆活性成分溶解量,以標示量的百分比表示;驗收表1中的5%�����、15%和25%的值是指標示量的百分比����,因此這些值和Q是相同的。
速釋制劑匯集樣品
除非個別專論中另有規定����,否則如果從混合樣品中溶出的活性成分的數量符合所附的混合樣品驗收表�,則滿足要求���。通過三個階段繼續測試�����,除非結果符合S1或S2。數量(Q)是專論中規定的活性成分的溶解量�,以標示量的百分比表示�����。
緩釋制劑
除非◆在個別專論中◆另有規定, 如果從測試的劑量單位中溶出的活性成分的量符合驗收表2,則認為合格����。繼續進行三個級別的測試�,除非結果符合L1或L2的限度����。活性成分溶解量的限制以標示量的百分比表示。極限包括Qi的每個值,即在每個指定的給藥間隔溶出的量。如果◆在個別專論中◆指定了多個范圍, 驗收標準將單獨適用適用于每個范圍。
遲釋制劑3
酸階段
除非◆在個別專論中◆另有規定,如果從測試單元中溶出的活性成分的數量(基于標示量的百分比)符合驗收表3���,則認為此階段結果合格。除非酸階段和緩沖液階段的結果都符合早期水平,否則連續測試全部等級��。
緩沖液階段
除非◆在個別專論中◆另有規定, 如果從測試的單元中溶出的活性成分的量符合驗收表4����,則滿足要求。連續進行三個級別的測試����,除非兩個階段的結果均符合更早的等級�����。除非◆在個別個人專論中◆另有規定,否則驗收表4中的Q值為75%�����?���!?在個別專論中規定◆ 數量(Q)是溶解在酸性階段和緩沖液階段中的活性成分的總量����,以標示量的百分比表示��。驗收表4中的5%、15%和25%值是標示量的百分比,因此這些值和Q是相同的�。
1.材料不應吸附���、反應或干擾被測樣品����。
2.如果使用蓋子��,須有開口����,以便隨時插入溫度計和取出樣品�����。
3.未被日本藥典接受�。
4.試樣取樣后應立即過濾�����,除非證明不需要過濾���。使用不會導致活性成分吸附或含有會干擾分析的可提取物質的惰性過濾器。
5.一種脫氣方法如下:在輕輕攪拌的同時�,將介質加熱至約41°�,立即使用孔隙率為0.45µm或更小的過濾器在真空下過濾����,劇烈攪拌,并在真空下繼續攪拌約5分鐘����?�?梢允褂闷渌涷炞C的脫氣技術來去除溶解氣體。