您當前的位置:檢測資訊 > 科研開發
嘉峪檢測網 2022-04-26 10:39
更多醫藥技術資訊,請點擊醫藥專欄:http://drug.anytesting.com/ 歡迎關注文末微信公眾號:藥研檢測drugtest
今日頭條
國內藥訊
1.京新藥業引進抗失眠新藥報產。浙江京新藥業1類新藥安達西尼膠囊上市申請獲國家藥監局受理,用于治療失眠障礙。安達西尼膠囊(EVT201)是Evotec公司開發的一款新型GABAa受體部分正向別構調節劑(pPAM),通過與α1-亞型結合導致GABAa受體的變構調節而中度激活該受體并導致下游信號轉導,從而抑制中樞神經系統,發生睡眠作用。京新藥業擁有EVT201在中國區域的獨家專利許可和開發權。
2.拜耳前列腺癌藥物新適應癥在華報產。拜耳雄激素受體抑制劑達羅他胺片的新適應癥上市申請獲國家藥監局受理,用于治療轉移性激素敏感性前列腺癌(mHSPC)。在關鍵性Ⅲ期臨床ARASENS中,與雄激素剝奪療法(ADT)加多西他賽相比,達羅他胺聯合ADT加多西他賽顯著改善mHSPC患者的OS,將患者的死亡風險降低了32.5%。2021年2月,該藥已在中國獲批用于治療非轉移性去勢抵抗性前列腺癌(nmCRPC)成年患者(商品名為諾倍戈)。
3.普米斯PD-L1/VEGF雙抗獲批肝癌臨床。普米斯生物1類生物新藥PM8002注射液獲國家藥監局臨床試驗默示許可,擬與標準化療聯用治療不可手術肝細胞癌(HCC)患者。PM8002是一款靶向PD-L1/VEGF的雙特異性抗體藥物,能夠同時發揮免疫抑制和抗血管生成的作用。此前,該產品于今年2月在中國獲批開展用于三陰性乳腺癌適應癥的臨床研究。
4.凌科新型激酶抑制劑獲批銀屑病臨床。凌科藥業新型激酶抑制劑LNK01004獲NMPA批準開展用于銀屑病治療的臨床試驗。LNK01004可同時抑制多個和銀屑病相關的多個炎癥細胞因子和疾病誘導信號通道。在臨床前試驗中,LNK01004主要分布在致病的皮膚組織中,有效避免由于藥物全身系統暴露而帶來的潛在的系統性免疫抑制造成的安全性問題;而且在動物試驗中具有較好的有效性和安全性。
5.上海美迪西2021年財報發布。4月24日,上海美迪西生物公布2021年財務報表。該公司2021年營收11.67億元,同比增長75.28%;歸母凈利潤為2.82億元,同比增長118.12%;研發投入7775.83萬元,同比增加65.57%。主營業務方面,藥物發現與藥學研究收入為6.1億元,同比增長72.68%;臨床前研究收入5.5億元,同比增長78.19%。2021年研發人數達到2117人,參與研發完成的新藥項目有85件通過NMPA批準進入臨床,同比增長107.3%。
國際藥訊
1.艾伯維IL-23抑制劑即將獲英國批準治療CD。艾伯維新型抗炎藥risankizumab獲英國藥品和保健品監管機構(MHRA)推薦納入早期獲得藥物計劃(EAMS),用于治療克羅恩病(CD)患者,MHRA同時也支持該藥在英國上市。risankizumab選擇性地結合IL-23的p19亞基并抑制IL-23與其受體的相互作用,從而阻斷IL-23刺激Th17細胞亞群誘導其產生IL-17A與IL-17F等細胞因子,抑制炎癥發生。該藥物已獲FDA和EMA批準用于治療銀屑病性關節炎和斑塊狀銀屑病。
2.長效肉毒桿菌毒素在美報BLA。Revance公司注射用daxibotulinumtoxinA(RT002)治療中重度眉間紋的生物制品許可申請(BLA)獲得FDA受理,PDUFA日期為今年9月8日。RT002是一種長效神經調節劑,藥物活性成分為A型肉毒桿菌毒素。發表在ASDS2021期刊上的數據顯示,用daxibotulinumtoxinA反復治療后,受試者靜態眉間紋嚴重程度得到快速和持續的改善。復星醫藥子公司擁有該新藥的中國獨家權益。
3.賽諾菲移植新藥臨床匯總數據積極。賽諾菲ROCK2抑制劑Rezurock(belumosudil)治療慢性移植物抗宿主病(cGVHD)的臨床試驗【ROCKstar(KD025-213)、KD025-028和Rezurock(KD025-213、KD025-208)】匯總數據積極。數據分析顯示,器官緩解率為:皮膚35%,關節68%,口腔57%,眼睛41%,上消化道73%,下消化道87%,肺部23%;總體緩解率為77%。Rezurock是FDA批準的首款ROCK2抑制劑,用于治療12歲以上、已接受過兩種前期全身性治療的cGVHD患者。在中國,燁輝醫藥為該新藥遞交的NDA已獲得CDE受理。
4.毛果蕓香堿眼藥水治療老花眼Ⅲ期臨床積極。Orasis公司開發的低劑量毛果蕓香堿(0.4%)眼科配方CSF-1在治療老花眼的兩項Ⅲ期臨床達到主要和關鍵性次要終點。試驗結果顯示,CSF-1治療第8天時顯著提高視力表多讀三行的患者比例;接受第一劑和第二劑治療后1小時內,患者多讀三行的比例由40%提高至50%(p<0.0001);而且CSF-1可在20分鐘起效,療效可持續達8小時。此外,CSF-1總體耐受性良好。該公司計劃今年下半年向FDA遞交新藥申請(NDA)。
5.渤健撤回Aβ單抗的歐洲上市申請。渤健宣布撤回其用于治療早期阿爾茨海默病的Aβ單抗Aduhelm(aducanumab)的歐洲上市許可申請(MAA)。此前該新藥未能獲得歐盟CHMP的支持,該機構認為Aduhelm提供的數據不足。今年3月,渤健與合作伙伴衛材為Aduhelm制定了一項新的商業安排,衛材退出市場銷售,自2022年3月14日起,Biogen對Aduhelm的開發、商業化和生產擁有唯一的決策權。預計今年下半年,兩家公司將公布合作的第二款Aβ抗體lecanemab的后期臨床結果。
6.勃林格殷格翰布局創新蛋白降解劑。勃林格殷格翰與VantAI公司將利用后者的幾何深度學習平臺,優化針對每個E3連接酶平臺的新分子設計,聚焦一項與多個獨特E3連接酶平臺結合的降解劑項目,合作開發降解傳統“不可成藥”靶點的創新降解劑候選療法。根據協議,VantAI將獲得未披露的前期付款以及臨床前、臨床期和商業化里程碑后期付款。勃林格殷格翰將獲得候選降解劑的全球開發和商業化。
醫藥熱點
1.同濟專家獲俄羅斯工程院金獎。華中科技大學同濟醫學院附屬同濟醫院日前在官網宣布,該院的92歲高齡的感染科專家、醫學博士趙燦熙教授因在中醫治療熱帶病的研究領域的突出成績,被俄羅斯工程院授予2021年金獎。趙燦熙致力于中醫治療熱帶病的研究并取得系列成就。他在全球首次發現中藥蕪荑中的成分亳菊具有良好的抗瘧作用,鑒于目前惡性瘧疾產生了普遍的抗藥性,該發現有望成為瘧疾治療的補充。
2.福建首個中醫專科護理門診落地社區中心。近日,福建省護理學會為福州市臺江區上海街道社區衛生服務中心的中醫專科護理門診正式授牌。據悉,這是福建省首家“中醫專科護理門診”在社區中心開設,該門診工作由中心的3位中醫師和多位護士配合完成,居民可根據醫囑來到康復理療室,由護士理療,通過拔罐、刮痧、艾灸等中醫適宜技術,達到調理亞健康狀態、防病治病的目的。
3.廣東增加老年護理供給。近日,廣東省衛健委聯合省中醫藥管理局制訂《廣東省老年醫療護理服務試點工作方案》,計劃通過1年時間,探索形成可復制可推廣的老年醫療護理服務做法。試點地區包括廣州市、珠海市、佛山市、惠州市、東莞市、中山市、湛江市7個地市。《方案》提出,將引導區域內部分一級、二級醫院轉型為護理院;增加老年護理專業護士數量;探索建立有利于老年醫療護理服務發展的價格和支付政策機制。
4.國內首次發現奧密克戎BA.2.3進化分支。4月24日0時至24時,山東煙臺市新增感染者36例,其中確診病例2例、均為普通型,無癥狀感染者34例,均已轉運至定點醫院。煙臺市第一時間開展病毒全基因組測序,分析發現為同一條傳播鏈,病例基因分型為奧密克戎BA.2.3進化分支。這也是奧密克戎BA.2.3進化分支在國內的首次出現,它具有更強的傳染性和更短的潛伏期。
評審動態

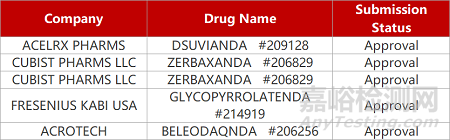

來源:藥研發


