您當前的位置:檢測資訊 > 監管召回
嘉峪檢測網 2022-02-07 20:05
藥監局突襲飛檢
近日,河南省藥品監督管理局發布《關于對2021年部分醫療器械生產企業飛行檢查情況的通告(2022年第3號)》(以下簡稱《通告》)。
據《通告》,依據《藥品醫療器械飛行檢查辦法》《醫療器械生產企業飛行檢查工作規范》,河南省藥品監督管理局組織對部分重點監管醫療器械生產企業開展了飛行檢查。
針對不同產品特點和風險類型企業,藥監局制定檢查方案,按照醫療器械生產質量管理規范及配套法規文件要求,重點檢查企業落實質量安全主體責任落實情況、產品質量安全管理情況,對采購、生產過程、產品檢驗和產品可追溯性等重點環節進行了全面檢查。
對檢查中發現的問題和線索,檢查組已移交醫療器械生產企業所在地監管部門根據《醫療器械監督管理條例》《醫療器械生產監督管理辦法》《醫療器械生產質量管理規范》等有關規定進行依法調查、處理。同時,督促企業對存在問題進行整改。
一批械企被限期整改,
安圖生物、駝人、明峰...
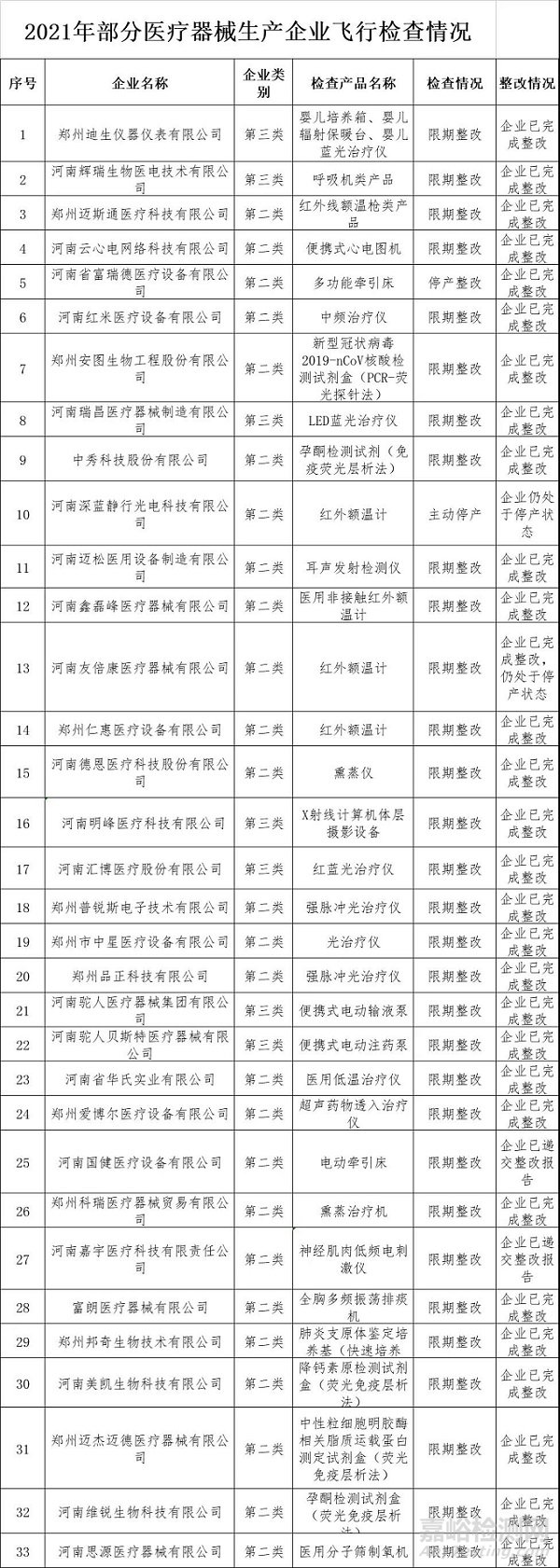
據悉,本次被飛檢的醫療器械企業共計33家,河南省富瑞德醫療設備有限公司被要求停產整改,河南深藍靜行光電科技有限公司被要求主動停產,而鄭州迪生儀器儀表有限公司等31家公司被要求限期整改。
其中,河南深藍靜行光電科技有限公司目前仍處于停產狀態,河南友倍康醫療器械有限公司已完成整改但仍處于停產狀態,河南國健醫療設備有限公司和河南嘉宇醫療科技有限責任公司已遞交整改報告。
另外,被限期整改的29家企業包括:鄭州迪生儀器儀表有限公司、河南輝瑞生物醫電技術有限公司、鄭州邁斯通醫療科技有限公司、河南云心電網絡科技有限公司、河南省富瑞德醫療設備有限公司、河南紅米醫療設備有限公司、鄭州安圖生物工程股份有限公司、河南瑞昌醫療器械制造有限公司、中秀科技股份有限公司、河南邁松醫用設備制造有限公司、河南鑫磊峰醫療器械有限公司、鄭州仁惠醫療設備有限公司、河南德恩醫療科技股份有限公司、 河南明峰醫療科技有限公司、河南匯博醫療股份有限公司、鄭州普銳斯電子技術有限公司、鄭州市中星醫療設備有限公司、鄭州品正科技有限公司、河南駝人醫療器械集團有限公司、河南駝人貝斯特醫療器械有限公司、河南省華氏實業有限公司、鄭州愛博爾醫療設備有限公司、鄭州科瑞醫療器械貿易有限公司、富朗醫療器械有限公司、鄭州邦奇生物技術有限公司、鄭州邁杰邁德醫療器械有限公司、河南維銳生物科技有限公司、河南思源醫療器械有限公司。目前已完成整改。
不難發現,在新版《醫療器械監督管理條例》落地后,全國各個地區對于醫療器械企業的檢查頻次在不斷增加。特別是在2021年第六批70名國家檢查員上任之后,從國家到地方各省,不打招呼直奔現場的檢查頻次也將越來越高。
按照上一年度的飛檢計劃,2022年開年以后,新一輪飛檢計劃想來也在醞釀之中。所以,不論企業大小,唯合法生產、經營是正道,時刻做好自查自糾,才能真正做到防患于未然!

來源:醫療器械經銷商聯盟


