您當前的位置:檢測資訊 > 科研開發
嘉峪檢測網 2022-01-06 11:51
更多醫藥技術資訊,請點擊醫藥專欄:http://drug.anytesting.com/ 歡迎關注文末微信公眾號:藥研檢測drugtest
今日頭條
榮昌HER2-ADC新適應癥獲批。榮昌生物注射用維迪西妥單抗的新適應癥上市申請獲NMPA批準,用于治療特定的尿路上皮癌患者。維迪西妥單抗(disitamab vedotin,RC48)是一款HER2-ADC新藥,已于去年6月獲NMPA附條件批準上市,用于治療至少接受過2種系統化療的HER2過表達、局部晚期或轉移性胃癌(包括胃食管結合部腺癌)患者,是首款由中國公司自主研發并獲批上市的ADC。
國內藥訊
1.百濟神州PD-1獲批第6項適應癥。百濟神州PD-1替雷利珠單抗注射液(百澤安)新適應癥獲NMPA批準,用于治療接受鉑類化療后出現疾病進展的二或三線局部晚期或轉移性非小細胞肺癌(NSCLC)患者。此前,百澤安已獲批5項適應癥,涉及治療的癌癥種類包括肝細胞癌(HCC)、尿路上皮癌(UC)、霍奇金淋巴瘤(cHL)、鱗狀和非鱗狀NSCLC。5項適應癥均被納入國家醫保談判目錄。
2.信立泰貧血新藥報NDA。信立泰腎性貧血新藥恩那司他片的上市申請獲CDE受理。恩那司他是日本煙草公司(JT)開發的一款口服活性低氧誘導因子脯氨酰羥化酶抑制劑(HIF-PHI),有望成為羅沙司他之后第2款上市的同類藥物。相較現有療法,恩那司他片改善貧血機制明確,既可促進內源性促紅細胞生成素的生成,也可改善鐵的利用;且具有良好的安全性和有效性。
3.開拓藥業防脫發新藥上Ⅲ期臨床。開拓藥業1類新藥福瑞他恩(KX-826)治療男性雄激素性脫發(AGA)的注冊性III期臨床完成首例患者入組及給藥。KX-826是一款FIC雄激素受體(AR)拮抗劑,擬開發用于治療雄激素性脫發和痤瘡。針對痤瘡適應癥,KX-826已完成I期臨床,II期臨床試驗即將開始。在美國,FDA已批準開展KX-826治療男性雄激素性脫發的II期臨床,目前正準備受試者入組。
4.康方PD-1/CTLA-4雙抗獲批III期臨床。康方生物新型PD-1/CTLA-4雙抗卡度尼利單抗(AK104)獲CDE批準,即將開展一項聯合同步放化療治療局部晚期宮頸癌的Ⅲ期臨床。AK104是康方生物腫瘤免疫治療骨干藥物,目前正在國內外多項臨床中治療腎細胞癌、胃癌等多種惡性腫瘤。去年9月,CDE已受理卡度尼利單抗治療復發/轉移宮頸癌的NDA申請,并給予優先審評資格。卡度尼利單抗有望成為全球首個獲批上市的PD-1雙抗。
5.基石ALK抑制劑獲批關鍵性臨床。基石藥業洛拉替尼(lorlatinib,曾用名:勞拉替尼)獲國家藥監局臨床試驗默示許可,即將開展用于ROS1陽性晚期非小細胞肺癌(NSCLC)的關鍵性臨床研究。洛拉替尼是輝瑞研發的一款第三代ALK/ROS1酪氨酸激酶抑制劑(TKI),已獲FDA批準用于一線治療ALK陽性轉移性NSCLC患者。在中國,洛拉替尼用于ALK陽性肺癌已開展多項臨床研究,其針對ALK陽性晚期NSCLC的上市申請已于2021年3月遞交。
6.三生國健PD-1單抗授權美國Syncromune。三生制藥旗下子公司三生國健與美國Syncromune公司簽署授權協議,將其PD-1單抗注射液609A用于腫瘤免疫聯合療法syncrovax™的全球開發及商業化權益授權給Syncromune公司。根據協議,三生國健將有望基于609A的臨床價值前景、重要監管及銷售里程碑,以及其他商業化價值,獲得數億美元的首付款、里程碑付款及其他的激勵。三生國健將繼續保有609A全球任何syncrovax™療法以外的權益。
7.君實終止與阿斯利康的PD-1推廣合作。君實發布公告宣布終止與阿斯利康的PD-1推廣合作。去年2月,君實將特瑞普利單抗(拓益®)泌尿腫瘤領域適應癥的獨家推廣權以及所有獲批適應癥在非核心城市區域的獨家推廣權授予阿斯利康。經雙方友好協商,原協議自 2022年1月1日起終止。根據公告,特瑞普利單抗目前已有兩項適應癥納入最新版國家醫保目錄。
國際藥訊
1.第二代mRNA新冠疫苗加強針臨床積極。Gritstone bio公司第二代T細胞增強型自我擴增mRNA(samRNA)新冠疫苗,在用于加強接種的Ⅰ期臨床中獲積極數據。60歲及以上健康成人在完全接種兩劑阿斯利康第一代新冠疫苗Vaxzevria(AZD1222)后再加強接種samRNA疫苗,受試者表現出對新冠病毒刺突蛋白的強大中和抗體應答,并有效提高針對非刺突蛋白抗原的CD8陽性T細胞水平。而且疫苗耐受性良好。
2.抑癌基因療法獲FDA快速通道資格。FDA授予Genprex公司基因療法Reqorsa快速通道資格,與默沙東PD-1抑制劑Keytruda(帕博利珠單抗)聯用,治療無法切除的III期或IV期非小細胞肺癌。Reqorsa由包裹在帶有正電荷脂質分子納米顆粒中的抑癌基因TUSC2組成,已在臨床前研究中顯示出與Keytruda具有協同作用。預計明年初啟動一項聯合治療的Ⅰ/Ⅱ期臨床。
3.EGFR抑制劑治療肺癌獲突破性療法認定。Cullinan Oncology公司EGFR抑制劑CLN-081獲FDA授予突破性療法認定,用于治療攜帶EGFR外顯子20插入突變、局部晚期或轉移性非小細胞肺癌(NSCLC)經治患者。CLN-081可選擇性靶向攻擊攜帶EGFR外顯子20插入突變的細胞,同時不影響表達野生型EGFR的細胞,主要針對攜帶EGFR外顯子20突變的經治NSCLC患者。該療法目前正在Ⅰ/Ⅱa期臨床中評估不同劑量的療效和安全性。
4.艾伯維c-Met-ADC獲突破性療法認定。FDA授予艾伯維c-Met靶向ADC藥物telisotuzumab vedotin(Teliso-V)突破性療法認定,用于治療c-Met+、EGFR野生型、局部晚期/轉移性非鱗狀非小細胞肺癌(NSCLC)經治患者。一項Ⅱ期臨床結果顯示,在這類患者中,Teliso-V單藥治療在c-Met高表達組的ORR為53.8%,c-Met表達水平中等組的ORR為25.0%。目前,Teliso-V聯合EGFR-TKI抑制劑奧希替尼治療經治c-Met過表達NSCLC患者的Ⅰ期臨床也正在進行中。
醫藥熱點
1.復旦大學附屬婦產科醫院青浦分院即將竣工。經過兩年多時間的建設,復旦大學附屬婦產科醫院青浦分院進入室內裝飾裝修與室外總體施工階段,預計今年6月份完成竣工交付。據悉,門急診醫技樓四層手術室建筑面積約3350平米,科室配置高標準層流凈化手術間27間,包含24間空氣潔凈等級為萬級的手術室、1間正負壓手術室、1間機器人手術室和1間空氣潔凈等級為百級的DSA手術室。
2.21個中藥大品種漲價。據財聯社消息,九芝堂1月1日已向客戶正式下發調價通知,稱考慮原材料漲價影響,將旗下包括安宮牛黃丸、六味地黃丸、逍遙丸等在內的21個品規中成藥供貨價或建議零售價上調,調價幅度在6%-30%不等,其中安宮牛黃丸三個品規的漲價幅度在12%-25%之間,九芝堂OTC產品營收占比最大的六味地黃丸則漲價10%。
3.JAMA子刊:間歇性禁食與健康關聯。美國猶他大學與威斯康星大學麥迪遜分校等聯合研究團隊在JAMA子刊JAMA Network Open發表的最新研究論文顯示,間歇性禁食可能在改善體重和心臟代謝結果方面發揮有益作用,尤其是對于超重或肥胖的成年人。研究人員對已發表的11項隨機臨床試驗的Meta分析進行了綜合分析,發現高質量數據支持1-2個月的改良版間歇性禁食與健康成人和超重、肥胖或非酒精性脂肪肝病人的體重指數適度降低有關。
4.陜西:新冠患者個人不用負擔醫療費用。陜西省新冠肺炎疫情防控工作領導小組在4日下午舉行的新聞發布會表示,目前各級財政共投入28.2億元用于抗擊本輪疫情,對確診患者發生的醫療費用,在基本醫保、大病保險、醫療救助等按規定支出后,個人負擔部分將由各級財政予以安排。
評審動態

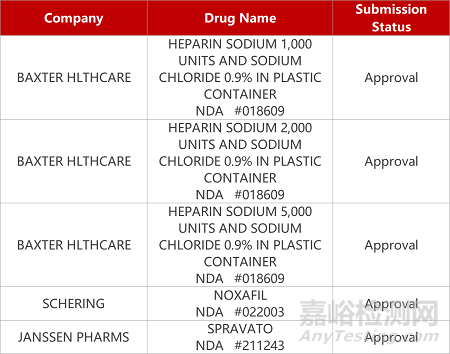

來源:藥研發


