您當前的位置:檢測資訊 > 監管召回
嘉峪檢測網 2021-11-23 15:15
迎接FDA現場審計前的相關準備工作
一、概述
FDA現場檢查主要目的:①檢查申報文件(ANDA與DMF)有原始數據支持與現行現場文件記錄中的數據是否一致,是否完整、準確、可靠;②是否違反cGMP現象,確保產品生產滿足cGMP要求;③檢查設施、設備是否適合生產合格產品,確保質量系統能夠正確正常運行;④檢查企業質量控制系統對數據完整性的實施以及如何對原始數據進行存儲;⑤檢查企業是否遵循文件中的承諾。
核查藥品注冊申報資料的真實性、一致性以及藥品上市商業化生產條件,檢查藥品研制的合規性、數據可靠性等,對研制現場和生產現場開展的核查活動。
現就仿制藥(ANDA)注冊現場審計經驗分享給藥學同行們,此次總結和歸納內容,主要分享如何迎接FDA現場檢查(審計)與批準前現場檢查整個過程2大部分展開。
二、迎接現場審計的流程框架
1、接到現場檢查通知
2、根據時限制定公司自查計劃
3、根據核查范圍與主要內容,企業自查與準備
三、主要內容
(1)迎接現場檢查通知
1、FDA官方對提交的電子資料審核通過后,根據制劑生產廠家申請會發函通知給API制藥公司。
2、根據發函內容翻譯成中文,組織相關部門進行會議,發放各個職能部門。
3、成立自查小組,以及迎檢小組,小組成員涉及:研發、生產、注冊、質量、QA、QC、倉儲、財務等相關部門人員。
(2)制定公司自查計劃并完成現場檢查前企業內部自查
1、公司自上而下1個星期進行全面檢查。
2、范圍與時間:倉庫1天、研發1天、生產2天、質量2天(QC、QA),根據情況各部門內部自己進行一次自查。
3、整理匯總自查報告,分發各個部門,各部門進行整改。
(3)檢查范圍與主要內容
1、檢查范圍:生產系統、物料與倉儲系統、質量系統、廠房設施設備系統、實驗室控制系統、文件系統、包裝標簽系統、發運系統。
2、檢查主要內容



(4)現場檢查準備
1、宗旨:重視現場檢查、尊重檢查官、本著學習不斷持續改進。
2、戰略為主,戰術為輔(戰略:一切以通過為最終目標;戰術:以檢查官為中心)。
3、準備英文稿,公司簡介PPT(公司具體位置、公司主特色、公司發展歷程、營業執照、藥品生產許可證、出口歐盟原料藥證明文件、組織架構圖、公司法定代表人履歷、公司布局全圖、全景(QA、辦公室、財務)、質量控制室簡介(主要檢測設備&部分主要房間)、質量管理部職責、QA保證主要職責、QC控制主要職責、質量控制架構、質量控制布局全圖、倉儲布局全圖與簡介、水系統&氮氣系統&HVAC系統簡介、生產區域布局及車間簡介、產品研發狀態、產品列表、檢查產品的生產工藝等。
4、成立迎檢小組:

5、任務劃分:

四、總結:
公司自查完成后,根據相應整改措施進行整改,并保持良好的公司全面運行狀態,迎接現場檢查;準備工作已做充足,接下來就是迎檢現場檢查以及準備,下篇內容詳細講解全程檢查活動,以及現場的應對答復。



一次性通過檢查的經驗分享
一、主要檢查經過內容
背景介紹
FDA現場審計專家組成:FDA檢查官(生產技術)、FDA化學家(QC實驗室);此組成模式和國內一致(如同中國組長制:組長為國家局、成員為各省抽調)。
現場檢查跟蹤與缺陷收集
1、準備工作,會議室現場布置;戰術-尊重檢查官,重視檢查。
2、公司法人致歡迎詞,企業發言代表(質量副總)進行ppt簡介介紹,最后注冊部經理進行簡單介紹注冊申報產品信息;最后FDA審計官發言主要介紹審計行程。
3、檢查時間:根據審計專家計劃來,一般一周左右;現場介紹審計流程,主要分:現場檢查、文件檢查。
4、重點之動態/靜態檢查:根據注冊申報產品工藝進行1~3批現場生產(也可根據工藝生產時間以及檢查時間進行溝通,具體生產)。在現場審計前1-2個星期進行物料采購生產前準備(全部物料,包括包材全部檢測待用;不管現場溝通情況如何,先根據3批生產進行準備;至于靜態檢查那就重心在現場、文件資料上。
5、現場記錄問題。需要記錄后面文件審查需要提供的文件資料(并記錄現場檢查審計老師提出的問題,以便后續學習與改進,建議指定2-3人進行現場記錄)。
6、現場檢查經過(匯總如下):
(1)倉儲系統
1)檢查倉庫整體布局與注冊申報是否一致,是否滿足cGMP要求,是否在使用中。
2)檢查倉庫是否有成品庫、輔料庫、合格品區、不合格品區、待驗區、退貨區、暫存區,檢查了標識;并特地檢查了旮旯和上鎖房間。
3)特別檢查陰涼庫儲存條件&房間溫濕度記錄,現場詢問了有做倉庫溫濕度分布驗證,是否有挑戰點分布圖;查看了現場滅蚊燈與粘鼠板&檢查記錄。
4)檢查了取樣間,并詢問倉庫主任:①取樣間的取樣工具是否有分產品和專有標識標簽以及怎么管理,清洗流程;②詢問了產品的儲存條件,并檢查了現場物料包裝包扎存放;③現場詢問倉庫主管進場物料流轉程序(也就是物料進倉庫、通知請驗、生產發料);④詢問倉庫管理員工作職責。
5)檢查了現場物料的帳、卡、物,以及工藝驗證和近半年的生產產品相關物料臺賬。
6)檢查了倉庫辦公室現場:文件夾標識、記錄臺賬分類、臺賬有無缺陷(無復核、無遺漏、無空缺);檢查了合格供應商臺賬,物料列表。
7)現場詢問倉庫主任與管理員:設備設施出現故障應急處理流程和應對措施(如溫濕度、空調、抽風系統)。倉庫清潔周期與清潔SOP。
8)檢查特殊&危險品庫現場,現場詢問:如何管理。
(2)QC控制實驗室
1)準備鞋套和貴重物品暫存盒(給審計專家準備)。
2)進入QC區域的門禁門一定是關閉正常使用的。
3)更衣柜檢查:審計專家讓打開男女更衣柜檢查(檢查是否有食品、圖譜、記錄),學習資料和筆記本可以有,審計專家現場翻看學習資料和筆記本(估計還是查看有無原始數據記錄條和圖譜記錄)。千萬不要掩耳盜鈴!
4)辦公室檢查:桌子上的文件資料要擺放整齊并要有文件標識(審計老師現場提出),審計專家現場打開文件資料柜檢查并自己翻看記錄和文件(有無超期限未處理的記錄和文件,老師建議在文件資料柜外貼上具體文件目錄和文件夾側面標識)。
5)常溫留樣室檢查:主要檢查了留樣臺賬及留樣觀察記錄,留樣標簽是否完整。
6)穩定性考察室檢查:重點檢查考察箱管理,檢查考察箱臺賬是否與穩定性留樣一致,留樣樣品來去記錄,并查看穩定性考察箱溫濕度記錄,最后當場詢問:穩定性考察箱使用管理(是否專人管理、溫濕度是否每天記錄、考察箱是否有預警系統/有無進行預警驗證、假期穩定性如何管理、異常情況如何應對與管理、是否經過設備溫度分布驗證/是否按照滿載熱空點進行放樣考察);建議-考察箱樣品有個清楚排列圖。
7)水分測定室檢查:主要檢查儀器使用記錄、水分標定記錄、現場溫濕度及房間溫濕度記錄。
8)稱量室檢查:①主要檢查儀器使用記錄、天平日校記錄、現場溫濕度及房間溫濕度記錄;②剛好有稱量活動,現場詢問分析員水平圈怎么調整?定量實驗用什么級別天平?天平最小稱量值,以及整個稱量過程。是否對稱量勺進行管理(已清潔與待清潔,清洗程序與周期)。
9)標準溶液室檢查:查看標準溶液(滴定液&標準溶液)目錄及滴定液使用領用記錄,審計老師現場逐個檢查滴定液標簽+晃動溶液觀察(現場抽查標定記錄);檢查了滴定管標定記錄和如何存放。
10)試劑庫檢查:現場核查試劑領用臺賬并核對物與臺賬是否一致,現場檢查劇毒品臺賬考核取樣整個流程,易制毒化學品臺賬,試劑分類擺放管理,房間環境如何管理,試劑出庫如何管理。
11)理化實驗室檢查:①現場試液抽查(配制記錄、標簽、有無過效期),檢查移液管架上移液管是否擺放正確,是否清洗干凈是否有隔塵處理,檢查玻璃器具(移液管、容量瓶、量筒)標定記錄和標簽,②詢問是否有標定計劃,同樣現場考核標定程序,查看現場開瓶試劑管理,查看pH計標定記錄和使用記錄(現場討論是否可以把2種記錄歸在一起);③特地查看電位滴定儀日常維護保養記錄并詢問怎么維護(估計是很少使用的緣故);④移液管分類使用(儀器分析、理化分析、生化分析、定量分析用),玻璃量器具的清洗規程及清洗記錄,就連恒溫水浴鍋的使用記錄和維護保養記錄都檢查。
12)冷藏室檢查:審計專家直接奔冰箱&冷藏箱檢查-查看是否有上鎖管理,冷藏層的物品(需冷藏的試液、對照品溶液、菌種接種傳代培養物)、冷凍層,給出建議-微生物檢測相關與化學檢測相關盡量分開存放(冰箱專用);藥品冷藏箱(對照品、標準品);分類定置管理。并詢問QC分析員對照品管理程序及領用流程。
13)普通儀器室檢查:檢查紅外、紫外、旋光儀器里是否有干燥劑以及干燥機的狀態(反過來查看變色硅膠的干燥處理記錄),查看紅外、紫外、旋光3臺儀器近3個月的校驗記錄(并對應翻看部門儀器管理規程),檢查抽提里是否有廢記錄和圖譜,詢問3臺儀器是否連接有計算機軟件(是否有權限管理、審計追蹤功能、計算機系統是否可以修改系統時間,審計老師現場測試的)。
14)培養室檢查:培養箱是否有經過熱分布驗證(特別是滿載冷點示意圖,并查看現場內部自校記錄)、檢查培養箱內部培養皿是否有標識以及與箱體外面示意表是否一致,檢查培養物觀察記錄(水系統微生物檢查記錄)、詢問培養箱是否有預警備用(沒有)。
15)滅菌滅活室檢查:審計老師是直接詢問微生物檢查員-滅菌滅活區別,怎么操作,培養基如何處理?后面直接翻看高壓滅菌鍋使用記錄。
16)微生物實驗室&潔凈區現場檢查:也是直接檢查培養基收發臺賬,詢問鱟試劑與內毒素檢查用水由誰管理?如何領用?檢查各類臺賬和使用記錄、配制記錄、檢查記錄,并現場考問檢查用物品如何轉移至潔凈區,菌種臺賬銷毀記錄、菌種接種傳代在哪里進行?如何傳代?潔凈區沉降菌、浮游菌、塵埃粒子檢測周期?潔凈區如何消毒以及消毒管理?提問進入潔凈區如何管理?培養基適用性驗證(當場查看是否有對照培養基?),檢查產生異常如何處理?
17)精密儀器室(HPLC&GC)檢查:審計老師圈1圈(估計查看儀器品牌、衛生)、查看溫濕度計和溫濕度記錄(工作環境),開始了最最重要的詢問-控制軟件是否是英文版(一定是)?儀器是否有4Q認證?是否有內部校驗(程序、周期)?計算機系統(是否經過驗證、是否有權限管理、審計追蹤功能、計算機系統是否可以修改系統時間,現場測試)?色譜柱使用如何管理?儀器使用如何管理?儀器上產品項目如何管理?儀器分析員上崗是否有進行培訓和考核?是否有數據完整性管理程序?查看電腦桌面管理(軟件,建議只能有化學控制軟件)?現場登錄操作調取文件數據?有無數據備份管理?有無進行過備份挑戰實驗?分析檢測設備是否有維護保養計劃?最后詢問實驗產生偏差OOS異常情況該如何處理,比如OOS處理程序?
18)取樣間檢查:取樣工具(取樣勺、取樣管、取樣杯)是否進行分產品分類別使用,是否有清洗程序與清洗記錄?是否進行有效標識?是否有效防止交叉污染和防塵處理?
19)樣品接收室檢查:詢問樣品就收程序?貼簽管理,樣品處置與銷毀程序?產品是否進行分類管理?
20)現場檢查:①理化實驗室特別是微生物實驗室的清洗池柜子下方檢查(有無是否漏水、臟亂雜現象);②著重打開檢查了儀器室(普通&精密)操作臺抽屜和柜子里的記錄和配件物品(無廢記錄和廢圖譜、未處理的元數據紙條);③實驗室廢液如何管理是否有處置記錄?④溫度計和儀表是否經過檢定?是否有檢定計劃?⑤開具COA的計算機是否有權限管理,由誰來管理?
(3)制水系統
1)工程供應部主管現場介紹制水系統,審計官現場詢問取樣流程,消毒程序和消毒周期,檢查各類檢測試劑是否在有效期內,檢測試劑由誰配制,是否有配制記錄和領用記錄?有無制水程序?純化水執行什么標準,純化水檢驗SOP。制水系統是否經過完整驗證?
(4)生產系統(動態與靜態結合)
1)根據第二天的動態生產對現場進行全程檢查:各項QA生產前現場檢查是否都做到位?檢查報告是否簽批發放?工藝操作員是否經過培訓和考核(檢查記錄)、生產前產品工藝規程培訓,生產指令單何時簽批流程?物料領用管理和流程,生產記錄是否準備齊全?
2)現場查看上一次設備清洗記錄,打開手電筒照看反應釜內壁,查看現場垃圾桶(是否有煙頭和廢記錄及食品垃圾)查看精烘包車間與潔凈區現場。
3)辦公室文件資料柜是否有上鎖管理,送風系統是否獨立,一個車間做幾個品種是否有交叉污染的風險,是否經過評估是否經過清潔驗證?檢查是否能滿足產能和生產出合格質量的產品;檢查生產設備設施是否與申報資料一致(設備清單)在現場一一核對。
4)有無設備維修改造報告,有無設備維護保養計劃?生產前現場檢查,要求合理安排潔凈區于生產前1天進行消毒、高效過濾除塵后,第二天進行現場潔凈區檢查(浮游菌、沉降菌、塵埃粒子)。
5)現場各類器具是否都有進行標識并分類管理使用。
6)生產設備設施是否進行了設備驗證。
7)各類管道各種閥門是否有標識,各類生產用工具是否定置定位管理。
8)動態檢查:①根據生產工藝和周期提前準備3批生產的物料(可以和審計官進行溝通);②往往3批同時進行現場生產審計官是要全部跟蹤的,現場生產取樣、質量檢測結果是否合格。③檢查生產記錄、檢驗記錄,核對工藝參數、質量參數是否與注冊資料一致,3批質量是否一致(工藝是否成熟是否重現、質量重現性)。
(5)總結
1)檢查重點在數據完整性與合規上,不要存在僥幸心理,凡事要做到合理合規;作假害企業,實事求是理由不掩飾;重點計算機系統&微生物實驗室管理及倉庫管理。
2)QC現場管理是重點(6S管理),QA日常監督檢查是關鍵。
3)實驗記錄和輔助記錄:一定要如實及時填寫完善,不要給審計官留不好印象(培訓不合格,監督不力)。
4)其他需要注意:更鞋柜處的工作鞋和生活鞋是否擺放整潔、更衣柜里的工作服是否整齊掛放、工作服是否有費圖譜費記錄、工作服是否有洗不掉的污漬(盡量常清洗常更換)。
5)對上述檢查范圍,各自對號入座列表應對。
6)如何答復審計官現場提問,我想應該是每個QC經理/QC主管應該具備的基本知識和技能儲備以及對質量控制工作的理解。
7)動態檢查可能是常態:根據工藝復雜度,與官方溝通選做批次與進行完成程度。
8)生產現場很關鍵,重重點,通過現場檢查,產品才能進入市場。
9)現場檢查重視合規性、現場管理、監督檢查。

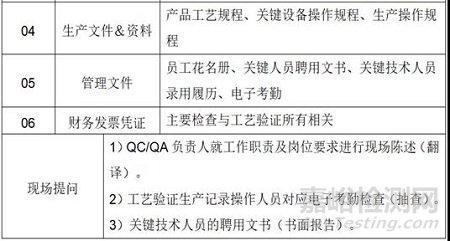
核查總結與缺陷整改
1、檢查完成后,FDA檢查官組織末次會議,檢查老師會根據現場檢查以及文件核查的問題與缺陷進行宣讀,并現場提出那些需要整改與改進。
2、企業自己進行總結,不管現場檢查是什么情況,首先企業是要感謝檢查官的指導與建議,也要感謝這幾天檢查官的辛苦,并進行承諾該如何進行改進落實。
二、總結
通過檢查并非難事也并非易事,只要企業做到合規合理合法,關鍵要做到真實,對待檢查要像放錄音帶一樣,還原現場。對待檢查一定要姿態放低,企業就是在學習和不斷持續改進中,現場檢查不要遮掩,也不要刻意去找理由去解釋,沒做好就是沒做好,這樣也會給檢查官好印象,表示企業是真心愿意去做好去改進,及時溝通反饋。咱們國家現在也逐步向歐美趕進,所以對待現場檢查我們只能從源頭開始,步步為營扎實做好每一步,希望上述經驗分享能給大家帶來啟發,我們各自對號模塊進行發掘進步。

來源:藥事縱橫


