您當前的位置:檢測資訊 > 科研開發
嘉峪檢測網 2020-08-31 10:36
目的 探討不同的樣品制備方法對殼聚糖創傷敷料細胞毒性實驗結果的影響。
方法 選擇6 cm²/ml和2 mg/ml,2種浸提比例,用1640、MEM和0.9% 氯化鈉注射液3種浸提介質進行MTT法實驗。
結果 用6 cm²/ml浸提比例的細胞存活率:0.9%氯化鈉注射液組>MEM組>1640組;用MEM浸提介質的細胞存活率:2 mg/ml組>6 cm²/ml 組。
結論 不同的樣品制備方法的細胞存活率差異顯著,建議統一殼聚糖創傷敷料樣品制備方法。
殼聚糖創傷敷料是以殼聚糖為主材料制造成的一種生物產品,具有抑菌消炎、止血止痛、促進創面愈合、滋養修復黏膜、免疫調節活性的作用。殼聚糖創傷敷料作為一種新型的創傷敷料,已經逐步取代傳統敷料,廣泛用于臨床創傷和傷口的愈合。細胞毒性實驗是進行生物學評價的重要檢測指標。GB/T 16886.5-2017《醫療器械生物學評價 第5部分:體外細胞毒性試驗》是最新的國家標準,其中MTT法是目前常用的細胞毒性檢測方法。由于該標準僅規定了共性的實驗方法,并沒有明確規定如何選擇合理的樣品制備方法,因此,針對殼聚糖創傷敷料這類可溶性產品,本研究結合YY 0953-2016《 醫用羧甲基殼聚糖》的行業標準,進行了一系列的對比實驗,以探討不同的樣品制備方法對殼聚糖創傷敷料細胞毒性實驗結果的影響。
1 材料與方法
1.1 一般材料
材料:殼聚糖創傷敷料,陽性對照材料為20%的二甲 基亞砜(dimethylsulfoxide,DMSO),陰性對照材料為高密度聚乙烯。
細胞:小鼠成纖維細胞L-929(中國科學院上海生命科學院細胞資源中心)。
主要試劑:1640培養基(北京Solarbio生物科技有限公司);MEM培養基[賽默飛世爾(蘇州)儀器有限公司];胎牛血清(Biological Industries Israel Beit Haemek Ltd);DMSO(SIGMA-ALDRICH);異丙醇(天津市百世化工有限公司);高密度聚乙烯膜(Hatano Research Institute, FDSC);0.9%氯化鈉注射液(石家莊四藥有限公司);MTT (Sigma公司),溶于不含酚紅的MEM中,濃度為1 mg/ml,溶液采用過濾器(孔徑≤0.22 μm)經無菌過濾法除菌,過濾后當天使用。
1.2 方法
材料浸提液制備(表1):將樣品按不同的浸提介質和浸提比例分為1~4組,其中按6 cm2/ml加入含10% 胎牛血清的MEM培養基,在5% CO2培養箱中37 ℃浸提24 h后作為浸提液1組;同法以含10%胎牛血清的1640培養基和 0.9%氯化鈉注射液制備浸提液2組和浸提液3組;每組設置100%浸提液和50%浸提液,分別標示為1a組、1b組、2a組、 2b組和3a組、3b組[1]。將樣品按2 mg/ml的比例加入含10%胎牛血清的MEM培養基,在5% CO2培養箱中37 ℃浸提24 h后作為浸提液4組[2]。
對照材料浸提液制備。陰性對照液:取高密度聚乙烯膜按表面積3 cm2/ml的比例加入含10%胎牛血清的MEM(1640或0.9%氯化鈉注射液)培養基,在5%CO2培養箱中37 ℃浸提24 h。陽性對照液:20%的DMSO。
表1 浸提液制備分組

細胞毒性實驗方法:將1×105/ml 細胞懸液接種于96孔板,每孔100 μl;置5% CO2培養箱中37 ℃培養24 h后,棄去原培養液;加入樣品浸提液、空白對照液、陰性對照液和陽性對照液,每孔100 μl置 CO2培養箱中37 ℃培養24 h;除去原培養液,每孔加入50μlMTT溶液;繼續培養2 h后 除去孔內MTT溶液,加入100μl異丙醇,振蕩10 min,在酶標儀570 nm和650 nm雙波長下測定吸光度(OD 值),按下式計算存活率:
存活率(%)=(100×OD570e)/OD570b
注:OD570e為實驗樣品組(陰性、陽性對照組)吸光度平均值,OD570b為空白對照組吸光度平均值[3]。
2 結果
細胞存活率結果顯示,3a組(80%)>1a組(69%)>2a組(18%);4組(93%)>1a組(69%),表明殼聚糖創傷敷料在不同的浸提介質和浸提比例下,細胞毒性結果差異顯著,見表2~5。
表2 GB/T 16886.5-2017 MTT法實驗結果(MEM組,6 cm2/ml)

 表3 GB/T 16886.5-2017 MTT法實驗結果(1640組,6 cm2/ml)
表3 GB/T 16886.5-2017 MTT法實驗結果(1640組,6 cm2/ml)

表4 GB/T 16886.5-2017 MTT法實驗結果(0.9%氯化鈉注射液組,6 cm2/ml)
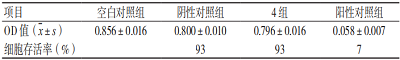
表5 GB/T 16886.5-2017 MTT法實驗結果 (MEM組,2 mg/ml)

3 討論
表2~4結果顯示,殼聚糖創傷敷料在其他方法相同,僅浸提介質不同的情況下,細胞存活率結果出現顯著差異,0.9%氯化鈉注射液組>MEM組>1640組。我們分析認為,殼聚糖創傷敷料在3種浸提介質中都能很好地溶解,0.9% 氯化鈉注射液的成分相對單一,而1640和MEM中含有多種氨基酸和葡萄糖等,成分相對復雜,在和樣品浸提的過程中,可能因不同成分和樣品相互作用,甚至發生反應,導致最終的浸提液差異,因此,不能簡單以細胞存活率的高低來判定哪種浸提介質是適宜的,應結合臨床實際應用,模擬創面體液環境,才能保證評價結果的臨床預期。
表2~5結果顯示,浸提介質均選擇含10%胎牛血清的MEM,按2 mg/ml浸提比例的細胞存活率結果明顯高于按6 cm2/ml浸提比例的結果。按 GB/T 16886.12-2017中規定選用面積比,根據產品厚度<0.5 mm,選擇6 cm2/ml;同時,YY 0953-2016標準中6.18.2規定,可用0.9%氯化鈉注射液配制成含羧甲基殼聚糖2 mg/ml溶液作為實驗液。對比2 mg/ml和6 cm2/ml浸提比例,按質量/體積同等換算為面積/體積比,浸提液相當于稀釋了8倍,雖然得到的細胞存活率結果較高,但是否與實際應用一致有待考證。
GB/T 16886.12-2017中規定,有質量比為0.2 g/ml和 0.1 g/ml兩種浸提比例。但是,對于殼聚糖創傷敷料這種可溶性產品,這兩種浸提比都難以使產品充分溶解,無法獲取浸提液,顯然這兩種浸提方法都不適用此類產品,因此,從臨床應用情況考慮,我們認為采用面積比更加貼合實際。
實驗樣品的前期制備對結果起著關鍵作用。GB/T 16886.122017雖然給出了樣品制備的原則,卻是對醫療器械的通用要求,針對具體品種,需要實驗者或者企業自己選擇。從本研究結果可知,對于殼聚糖創傷敷料這類產品,不同的樣品制備方法在同一實驗室內結果差異顯著,而且針對其可溶性這類特性,因為沒有統一的制備方法,即使相同的產品在不同的實驗室間也會出現很大差異,這不僅不利于國家對同類產品的監管評判,也對現有的標準方法提出了挑戰。隨著市場上醫療器械產品日益豐富,材質特性日益多元化,我們認為,有必要根據醫療器械產品特性,制定相關的產品標準,才能保障產品的安全有效。
【參考文獻】
[1]中華人民共和國國家質量監督檢驗檢疫總局.中國國家標準化管理委員會. GB/T 16886.12-2017 醫療器械生物學評價 第12部分:樣品制備與參照材料 [S].北京:中國標準出版社,2017.
[2]國家食品藥品監督管理總局.YY 0953-2015 醫用羧甲基殼聚糖[S].北京:中國標準出版社,2015.
[3]中華人民共和國國家質量監督檢驗檢疫總局.中國國家標準化管理委員會. GB/T 16886.5-2017 醫療器械生物學評價 第5部分:體外細胞毒性實驗[S].北京:中國國際出版社,2017.

來源:醫療裝備雜志


