您當前的位置:檢測資訊 > 法規標準
嘉峪檢測網 2019-07-24 14:41
01 臨床藥理學在藥物開發中的角色
臨床藥理學是研究藥物與人體相互作用規律的一門學科,特別是藥物對人體的治療作用,闡述了安全性、藥物代謝動力學、藥物效應動力學、毒副反應的性質和機制及藥物相互作用規律等。臨床藥理學的終極目標是為病人選擇合適的藥物,并選擇恰當的劑量及服藥周期。
臨床藥理學主要關注以下三個劑量相關的問題:
藥效研究的最佳劑量是多少?特定病人的最佳劑量是多少?不同暴露量下的推薦劑量是多少?

02 藥物代謝動力學&藥效動力學
藥代動力學簡稱PK,著重闡明機體對藥物的作用,即藥物在體內的吸收、分布、代謝和排泄及其經時過程;藥效動力學簡稱PD,描述藥物對機體的作用,即效應隨著時間和濃度而變化的動力學過程,更具臨床實際意義。PK-PD模型是綜合研究體內藥動學過程與藥效量化指標的動力學過程。
PK-PD模型把藥動學與藥效學所描述的時間、藥物濃度、藥物效應三者間關系有機地結合在一起進行研究,有助于更為全面和準確地了解藥物的效應隨劑量和時間而變化的規律。

03 劑量優化過程中治療窗口的確定
治療窗口是有效劑量和導致不可忍受副作用的劑量之間的范圍(safety index),處于該窗口范圍內的藥物濃度是安全而又有效的,如何保證體內的藥物濃度處于治療窗口內呢?這就需要界定影響體內藥物濃度的內在和外在的因素, 并因此來調整給藥劑量,進而選擇合適的服藥周期。
04 個體差異之間的劑量調整
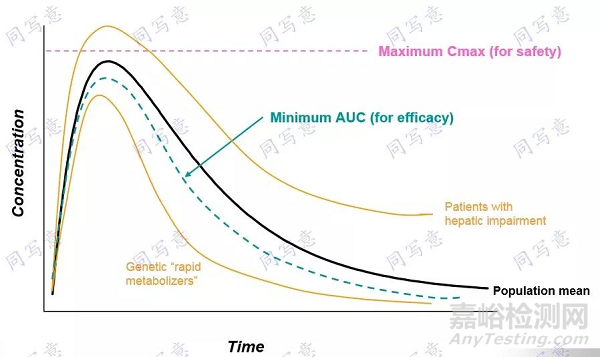
通過群體PK研究發現,相同服藥劑量下,對代謝比較快的用藥人群,體內藥物濃度會低于平均值,并且會低于最低有效暴露量;對代謝慢的用藥人群,體內藥物濃度會偏高,就可能產生一定的副反應。體內代謝速率的差異,導致體內藥物濃度的差異,這就需要對代謝程度不同的病人,合理調整給藥劑量。
05 不同藥物開發階段中藥理學的過渡路徑
隨著臨床試驗的展開,需要收集不同階段的有效信息,從臨床前體外到動物體內層面的研究,來確定藥物的有效性與安全性,以完成首次人體劑量的選擇。隨著IND研究的開展,不斷對劑量進行選擇及優化,以完成最終推薦劑量的選擇,最終完成藥品上市劑量的確定。
同時也要關注臨床開發階段,劑型改變對PK產生的影響。

06 從臨床藥理學角度需要關注的一般監管建議
IND階段的建議
以腫瘤藥為例,注冊臨床試驗前就需要有充足的研究數據來支撐劑量的選擇,FDA通常給與的建議有:
需要進行充足的劑量探索;
在活性和安全性之間要探索不同的劑量水平或劑量時間相關性;
對所有數據進行ER/DR分析,包括臨床PK、PD、活性和安全性數據,以及非臨床數據。
FDA鼓勵企業與審評機構進行溝通交流,像PreIND, EOP1, EOP2 等溝通會議窗口,探討數據研究的充分性。
NDA/BLA階段的建議
一般在Pre-NDA/BLA溝通會議上,FDA會與企業探討劑量選擇及臨床試驗數據是否足以滿足藥物上市申請,并結合藥物研究中獲得的信息來給與上市后的研究建議。
07 案例分析
大分子PD-1抗體藥物歐狄沃Nivolumab(OPDIVO®)
PD-1抗體藥物歐狄沃Nivolumab的一期爬坡試驗采用了傳統的3+3方案。測試的最高劑量10mg/kg每兩周給藥(Q2W), 沒有達到最高耐受劑量。擴展試驗采用了多劑量組合和多瘤種測試。獲批劑量3mg/kg Q2W的選擇是基于對PK、PD、藥效和安全性各項數據的綜合評估,包括體內藥物濃度能飽和PD-1的結合(RO%),和跨瘤種的最高應答率(ORR%)。后期獲批的固定劑量的調整(240 mg Q2W or 480 mg Q4W)是基于綜合的群體藥代動力學分析得出的結論,也就是調整后的劑量對體內藥物濃度差異的影響,不會產生有臨床意義的藥效或安全性的差異。

小分子靶向藥物帕唑帕尼pazopanib(VOTRIENT®)
帕唑帕尼三期臨床試驗的劑量選擇800mg QD,是基于一期臨床試驗的最好反應率(包括SD 和PR),一期臨床試驗最高測試劑量高達2000mg,最高耐受劑量(MTD)沒有達到。體內藥物濃度和藥效以及安全性的關聯性分析(ER)界定出體內濃度和主要臨床終點(PFS)無正向關聯, 然而和肝臟毒性成正相關。因此基于對體內藥物濃度產生影響的內在或外在因素而產生的劑量調整, 不會對藥效有影響,而能將肝臟毒性控制在可控范圍內。


來源:同寫意


